Актуальность. Сердечно-сосудистые заболевания продолжают занимать первое место среди причин смертности населения в большинстве стран мира [4]. Ишемическая болезнь сердца (ИБС) на протяжении многих лет остается главной причиной летальности, особенно среди социально значимой группы населения [3]. Пациенты, перенесшие операцию коронарного шунтирования (КШ), относятся к группе высокого риска, особенно в течение первого года, когда вероятность тромбоза шунтов и других тромбоэмболических осложнений (ТЭО) достаточно высока [6]. Большинство ТЭО связаны с наличием у пациента фибрилляции предсердий (ФП). ФП является вторым по частоте нарушением ритма после экстрасистолий [2]. Анатомическим субстратом ТЭО и роста смертности у пациентов с ФП являются тромбы в левом предсердии (ЛП) и его ушке [2,10].
Хирургические методы профилактики ТЭО можно разделить на 2 основные группы – хирургические методы выключения ушка ЛП и хирургические методы лечения ФП. Учитывая, что основным фактором риска ТЭО является тромбоз ЛП и его ушка, облитерация устья ушка является целесообразной для профилактики ТЭО.
Существует несколько методик выключения ушка левого предсердия:
- выключение ушка во время открытых операций на сердце (КШ, оперативное лечение на клапанах сердца и др.)
– прошивание, перевязка, клиппирование или резекция (элиминация);
- торакоскопическое клиппирование ушка ЛП или чрескожная имплантация окклюдеров.
Подобного плана вмешательства выполняются у пациентов с высоким риском ТЭО и противопоказаниями к терапии варфарином [9].
В отношении хирургического лечения фибрилляции предсердий можно сказать, что первая операция изоляции ЛП была выполнена J. Cox в 1980 году [7], изоляция обоих предсердий («коридор») предложена в 1985 году G. Guirandon [8]. При этом вмешательстве создавалась изолированная полоса миокарда и импульс достигал атриовентрикулярного соединения из синусового узла. В конце 80-х годов ХХ столетия была предложена принципиально другая схема хирургического лечения ФП – операция «лабиринт», которая претерпела множество модификаций, наиболее известная из которых Maze-3[11]. Основная суть операции заключалась в нанесении множественных насечек на предсердия для пресечения множественных кругов re-entry, в результате чего импульс проходил из синусового узла по лабиринту, при этом часть ЛП, прилегающая к легочным венам, оставалась изолированной электрически [1].
В последние годы большое распространение получило использование линейной моно- и биполярной радиочастотной эпикардиальной аблации при ФП для создания двунаправленного блока проведения электрического импульса как от легочных вен на предсердия, так и в обратном порядке.
Среди современных перспективных методов лечения ФП при операциях КШ в условиях ИК является эпикардиальная радиочастотная аблация устьев легочных вен (РЧА УЛВ) [5].
В связи с тем, что у пациентов с ИБС при выключении ушка ЛП из кровотока мы предотвращаем риск развития возможных ТЭО, таких как ишемический инсульт и/или системные тромбоэмболии, но при этом ФП как основная причина образования тромбов не устраняется, патогенетически обоснованным хирургическим лечением ИБС и ФП с профилактикой ТЭО является сочетанное выполнение КШ в сочетании с перевязкой ушка ЛП и РЧА УЛВ.
Цель: оценить ближайшие и отдаленные результаты хирургической профилактики тромбоэмболических осложнений и динамику сердечного ритма у пациентов после коронарного шунтирования.
Материалы и методы. В исследование включено 50 пациентов, находившихся на лечении в отделении хирургического лечения ИБС и нарушений ритма сердца Межтерриториального кардиохирургического центра БУЗ ВО «Воронежская областная клиническая больница №1». Пациенты разделены на 2 группы. В группу 1 вошли 25 пациенты с ИБС, которым было выполнено изолированное КШ в условиях ИК. В группу 2 вошло 25 пациентов, которым КШ в условиях ИК в сочетании с выключением УЛП из кровотока дополнялось эпикардиальной РЧА УЛВ.
Всем пациентам в предоперационном периоде проводилась первичная медикаментозная профилактика артериальных ТЭО общепринятыми дозами ацетилсалициловой кислоты (АСК). В послеоперационном периоде пациенты получали препараты АСК и низкомолекулярные гепарины. Кроме того, пациенты с ФП получали непрямые антикоагулянты в стандартных дозировках под контролем международного нормализованного отношения (МНО) и протромбинового времени.
Для оценки непосредственных и отдаленных результатов лечения пациентов нами использован критерий сохранения синусового ритма и отсутствия признаков острого нарушения мозгового кровообращения (ОНМК) и системных тромбоэмболий на момент выписки и через 1 год после операции.
Таблица 1. Сравнительная характеристика пациентов, включенных в исследование
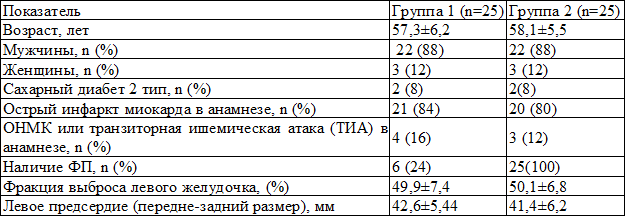
Результаты.
Тромбоэмболические осложнения. В раннем послеоперационном периоде в группе 1 зафиксирован один случай развития ТЭО - через 8 суток после операции - резкое ухудшение состояния, сопор, развитие транзиторной ишемической атаки (ТИА), падение АД, что потребовало перевода в реанимационное отделение. Развились явления тонкокишечной непроходимости. Повторно оперирован по поводу мезентериального тромбоза.
В отдаленном периоде в группе 1 зафиксировано 2 эпизода ТЭО:
- у пациента через год после операции на фоне нарушения ритма по типу пароксизмальной формы ФП возникла тромбоэмболия подколенной артерии, потребовавшая хирургического лечения в отделении сосудистой хирургии – тромбэмболэктомия.
- у пациента с постоянной формой ФП через 5 месяцев после операции на фоне повторных ТИА возникло нефатальное ОНМК (атеротромботический подтип) в бассейне правой СМА с развитием неврологического дефицита.
В группе 2 в раннем и отдаленном послеоперационном периоде ни у одного пациента каких-либо признаков тромбоэмболических осложнений не выявлено.
Динамика сердечного ритма. Как видно из табл. 2, в группе 1 в раннем послеоперационном периоде количество пациентов с постоянной формой ФП не изменилось, тогда как пароксизмальная и персистирующая ФП в данной группе увеличилась с 3 (12%) до 8 (36,4%) человек. Синусовый ритм в раннем послеоперационном периоде сохранялся у 11 пациентов (50%), р<0,05.
Через 12 месяцев после операции частота постоянной формы ФП также не изменилась и составила 3 случая (13,6%). При этом частота пароксизмальной и персистирующей формы ФП составила 4 случая или 18,2% (р<0,05), а синусовый ритм сохранялся у 15 пациентов (68,2%).
Таблица 2. Динамика сердечного ритма в группе 1

Таблица 3. Динамика сердечного ритма в группе 2

Как видно из табл. 3, в группе 2 синусовый ритм в раннем послеоперационном периоде сохранялся у 20 пациентов (80%). количество пациентов с постоянной формой ФП уменьшилось с 5 (20%) до 1 (4%) р<0,05, а пациентов с пароксизмальной и персистирующей формой ФП уменьшилось с 20 (80%) до 4 (16%) человек.
Через 12 месяцев синусовый ритм сохранялся в 18 случаях (72%), постоянная форма ФП выявлялась у 1 (4%) пациента (р<0,05), а пароксизмальная и персистирующая форма ФП у 6 (24%) человек.
Выводы. Применение хирургической профилактики – перевязки ушка левого предсердия и эпикардиальной радиочастотной аблации устьев легочных вен у пациентов с ИБС и фибрилляцией предсердий после коронарного шунтирования снижает риск развития артериальных тромбоэмболических осложнений и позволяет достоверно сохранить синусовый ритм в ближайшем и отдаленном послеоперационном периоде.
