Введение. Наличие ожирения у больных хронической обструктивной болезнью легких (ХОБЛ) потенцирует развитие сопутствующих сердечно-сосудистых заболеваний. По современным научным данным предполагается активное участие жировой ткани в процессах системного воспаления и формировании нарушений углеводного обмена у больных ХОБЛ. Ожирение является независимым фактором риска развития системных воспалительных реакций, результатом которого являются функциональные и структурные изменения других органов и систем [9, 4]. Наибольшая распространенность ожирения характерна для пациентов с начальными стадиями ХОБЛ и значительно уменьшается в терминальных стадиях [5].
По данным литературы, с ростом степени обструкции у пациентов с ХОБЛ увеличивается постнагрузка на правый желудочек (ПЖ), с формированием хронического легочного сердца (ХЛС) [3]. В настоящее время, активно изучается насосная способность сердца у здоровых лиц для выявления геометрических моделей левого желудочка (ЛЖ) [1].
У пациентов с ХОБЛ особый интерес вызывает влияние избыточного веса и ожирения на показатели производительности миокарда сердца.
Цель исследования. Изучить насосную функцию правого и левого желудочка у пациентов с ХОБЛ с разной массой тела.
Материалы и методы. Обследовано 72 пациента с ХОБЛ в возрасте 64,6±1,0 года, из них мужчин 60 человек (83,3 %). Всеми участниками подписано информированное согласие. Исследование одобрено этическим комитетом учреждения.
Критерии включения в исследование: пациенты в возрасте от 40 до 85 лет, страдающие ХОБЛ различной степени тяжести согласно классификации Global initiative for Obstructive Lung Disease (GOLD) 2017 [2]; показатель постбронходилатационного объема форсированного выдоха за первую секунду (ОФВ1пос) в пределах от 30 % до 75 % от должной величины. Степень ограничения воздушного потока определяли по результатам оценки ОФВ1пос и отношения данного показателя к форсированной жизненной емкости легких (ОФВ1пос /ФЖЕЛпос). Критерии исключения: возраст менее 40 лет, наличие онкозаболеваний, бронхоэктазов, туберкулёза лёгких в анамнезе; врожденные и приобретенные пороки сердца, клинически значимые нарушения ритма и внутрисердечной проводимости, митральная недостаточность ІІ степени и выше, сопутствующие заболевания в стадии декомпенсации.
Неинвазивную оценку степени насыщения крови кислородом проводили при помощи пульсоксиметра. За нормальную сатурацию (SpO2) принимали 95 % и более. Обследование включало измерение систолического (САД) и диастолического (ДАД) артериального давления по методу Короткова и подсчет частоты сердечных сокращений (ЧСС). Индекс курящего человека (ИКЧ) рассчитывали по формуле: ИКЧ (пачка-лет) = количество выкуриваемых сигарет в день умноженное на стаж курения (годы)/20 [2]. Пациенты разделены на 3 группы по индексу массы тела (ИМТ), согласно классификации Всемирной организации здравоохранения (ВОЗ),1998: 1-я группа - 31 пациент с ХОБЛ с нормальной массой тела; 2-я группа - 21 больной с повышенной массой тела; 3-я группа - 20 пациентов ХОБЛ в сочетании с ожирением І-ІІ степени. Клиническая характеристика групп представлена в табл. 1.
Статистическую обработку полученных данных проводили с помощью программы Statistica 6.0. Данные представляли в виде среднего и стандартной ошибки (М±m). Перед началом расчетов проверялись нормальность распределения с помощью двустороннего критерия согласия Колмогорова-Смирнова и равенства дисперсий методом Ливена. Поскольку выборки не соответствовали критериям нормальности, поэтому в дальнейшем использовались непараметрические статистические методы. Для выявления статистических различий между группами использовался критерий Краскела-Уоллиса. Для описания тесноты связи между количественными признаками использовали корреляционный анализ Спирмена. Для выявления ассоциаций между количественными признаками применяли факторный анализ. Статистически значимыми считали различия при p<0,05.
Таблица 1. Клиническая характеристика групп
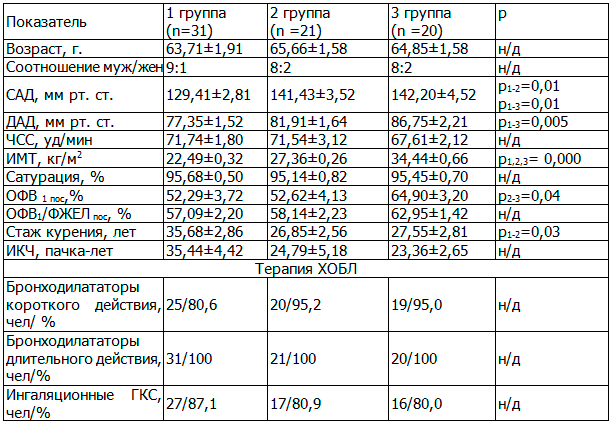
Как видно из табл. 1, группы сопоставимы по возрасту, полу, тяжести ХОБЛ и проводимой терапии. В 3-й и 2-й группах отмечается повышение САД и ДАД по сравнению с пациентами 1-й группы. Индекс курящего человека (ИКЧ), сатурация и ЧСС без групповых различий.
Всем пациентам проведено трансторакальное эхокардиографическое и допплерографическое исследование на ультразвуковом сканере «VIVID-7» (General Electric, CШA, 2010) с использованием матричного датчика с частотой 3,0 мГц (М3S) по стандартной методике согласно рекомендациям Американского эхокардиографического общества [7]. Для характеристики геометрической формы ЛЖ использовали следующие показатели: КДРлж - конечный диастолический размер ЛЖ, продольный диастолический размер ЛЖ (ДЛЖ), индекс сферичности ЛЖ как отношение КДРлж к Длж, конечный диастолический объем (КДОлж), массу миокарда ЛЖ (ММЛЖ), которую рассчитывали по формуле Devereux R.B: ММЛЖ=1,04·((ТМЖПд+ТЗСд+КДРлж)3-КДР лж3)-13,6, где ТМЖПд - толщина межжелудочковой перегородки ЛЖ в диастолу, ТЗСд - толщина задней стенки ЛЖ в диастолу. ММЛЖ индексировали к площади поверхности тела (ППТ) с вычислением индекса ММЛЖ (иММЛЖ). Относительную толщину стенок ЛЖ (ОТСлж) рассчитывали по формуле: ОТСлж=ТЗСд + ТМЖПд/ КДРлж. Оценивали минутную преднагрузку на ЛЖ, как произведение КДОлж и ЧСС. Напряжение стенки ЛЖ рассчитывали по формуле: систолическое напряжение (г/см2) = 0,334Pd/(h(1+(h/d))), где Р -САД, d - конечный систолический размер ЛЖ (КСРлж), h - толщина задней стенки левого желудочка в систолу (ТЗСс). Систолическую функцию ЛЖ оценивали в В - режиме с определением фракции выброса (ФВ) и ударного объема (УО) по методу Симпсон. Рассчитывали работу ЛЖ (А, Дж) и мощность (М, Дж/с) по формулам: А= АДср·133·УО·10-6, где АДср - среднее артериальное давление, УО - ударный объем ЛЖ; М=А/ЕТ, где ЕТ - продолжительность систолы в выносящем тракте ЛЖ (ВТЛЖ). Давление в левом предсердии (Р ЛП) или давление заклинивания легочной артерии (ДЗЛА) рассчитывали по формуле: ДЗЛА (мм рт.ст)=1,24Е/Еm+1,9, где Е-пиковая скорость раннего диастолического наполнения ЛЖ по данным импульсноволновой допплерэхокардиографии (ДэхоКГ); Еm - пиковая скорость раннего диастолического смещения митрального фиброзного кольца (МФК) со стороны боковой стенки ЛЖ по данным импульсноволновой тканевой миокардиальной допплерэхокардиографии (ТМДэхоКГ). Давление наполнения в ЛЖ оценивали по соотношению Е/Еm по данным ДэхоКГ и ТМДэхоКГ.
Для оценки структуры ПЖ измеряли толщину его свободной стенки из субкостальной позиции и поперечный базальный размер ПЖ в конце диастолы из апикальной четырехкамерной позиции. Измеряли конечный диастолический объем (КДОпж) ПЖ для оценки его преднагрузки. Для характеристики постнагрузки ПЖ мы использовали среднее давление в легочной артерии (Р ср. ЛА) и легочное сосудистое сопротивление (ЛСС). Р ср. ЛА рассчитывали по отношению времени ускорения (АТ) потока в выносящем тракте ПЖ (ВТПЖ) к времени выброса (ЕТ) [5]. ЛСС рассчитывали по формуле Франка-Пуазейля. ЛСС (дин·с·см-5) = (Рср. ЛА-Р ЛП)*1332*60/СВ, где Рср. ЛА- среднее давление в ЛА (мм рт.ст), Р ЛП- давление в ЛП или давление заклинивания ЛА (ДЗЛА), мм рт.ст, СВ-сердечный выброс (мл/с), 1332 - коэффициент для перевода в дин, 60 - коэффициент для перевода в секунду. Давление наполнения в ПЖ оценивали по соотношению Е/Еm, где Е-пиковая скорость раннего диастолического наполнения ПЖ по данным ДэхоКГ, Еm - пиковая скорость раннего диастолического смещения трикуспидального фиброзного кольца (ТФК) по данным ТМДэхоКГ.
Для оценки насосной функции ПЖ мы использовали показатели внешней работы и мощности. Рассчитывали работу ПЖ (А, Дж) по формуле: А=Рср.ЛА·133·УО·10-6. М=А/ЕТ, где ЕТ - продолжительность систолы в ВТПЖ.
Для характеристики питательного статуса определяли толщину подкожного (ПКЖ) и премезентериального жира (ПМЖ). Ультразвуковое исследование ПКЖ и ПМЖ выполнено по методике R. Suzuki et al. [8]. Сканирование проводилось у пациента, лежащего на спине, по средней линии живота между мечевидным отростком и пупком датчиком, расположенным перпендикулярно к поверхности кожи. Все ультразвуковые измерения проводились в фазу спокойного выдоха. Линейным датчиком высокого разрешения (5-12 МГц) в поперечном сечении измеряли толщину ПКЖ от внутренней поверхности кожи до наружной поверхности белой линии живота; на этих же срезах измеряли максимальную толщину ПМЖ от внутренней поверхности белой линии живота до передней поверхности печени. У пациентов с ожирением для измерения ПКЖ и ПМЖ использовали конвексный датчик (2-5 МГц) для лучшей визуализации.
Результаты и обсуждение. У пациентов с ХОБЛ с увеличением ИМТ увеличивается толщина ПКЖ и ПМЖ. Согласно таблице 2 выявлены достоверные межгрупповые различия по толщине ПКЖ и ПМЖ у пациентов с ХОБЛ с разной массой тела.
Таблица 2. Показатели подкожного и премезентериального жира у пациентов с ХОБЛ с разным индексом массы тела

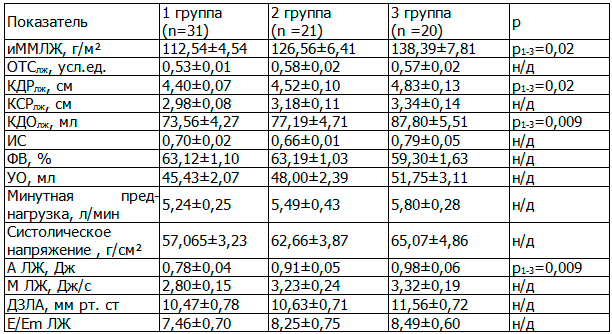
У больных ХОБЛ с ростом ИМТ увеличивается иММЛЖ. Выявлена концентрическая гипертрофия ЛЖ у пациентов с избыточным весом и ожирением. ОТСлж превышает норму во всех исследуемых группах. Все это сопровождается усилением систолического напряжения на стенку ЛЖ у пациентов с ХОБЛ с ростом ИМТ. У больных с ожирением форма ЛЖ представлена умеренным повышением ИС с увеличением преднагрузки на ЛЖ, что подтверждается достоверным повышением КДРлж и КДОлж, с тенденцией к увеличению минутной преднагрузки. Рост преднагрузки сопровождается увеличением венозного возврата, что отражается тенденцией к увеличению ДЗЛА, давления наполнения ЛЖ у пациентов 3-й группы по сравнению с больными 1-й группы. Возросшая преднагрузка на ЛЖ сопровождается усилением его производительности. Рост КДОлж приводит к увеличению работы (r=0,72, р=0,000) и мощности (r=0,64, р=0,000) левого желудочка. Повышение ИММ ЛЖ так же сопровождается большей работой ЛЖ (r=0,33, р=0,005). Нужно отметить, что систолическая функция ЛЖ в трех группах не нарушена: ФВ в диапазоне нормальных значений, но имеется тенденция к ее снижению у пациентов 3-й группы. Данные представлены в табл. 3.
Таблица 3. Эхокардиографические параметры левого желудочка у больных ХОБЛ с разной массой тела
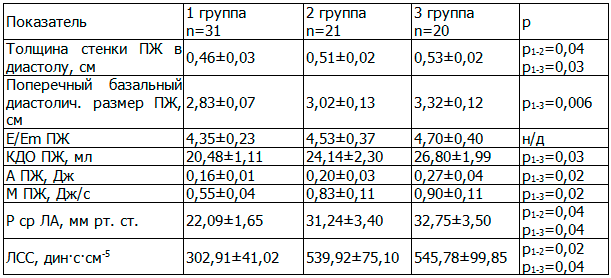
У больных с ожирением достоверно выше базальный диастолический размер и КДО ПЖ, а также имеется тенденция к повышению давления наполнения ПЖ по сравнению с больными 1-ой группы. Все это свидетельствует в пользу большей преднагрузки на ПЖ у больных 3-ей группы. У пациентов с ХОБЛ с избыточным весом и ожирением отмечается умеренная легочная гипертензия с увеличением ЛСС, что свидетельствует о повышении постнагрузки на ПЖ. У данных пациентов постнагрузка хроническая и проявляется гипертрофией свободной стенки ПЖ. У пациентов с ХОБЛ подъем ЛСС сопровождается уменьшением насыщения крови кислородом, вызывая вентиляционно-перфузионное несоответствие. Выявлены обратные корреляционные связи между ЛСС и сатурацией кислорода крови (r=-0,40, р=0,001). Таким образом, у пациентов с ХОБЛ с повышенной массой тела и ожирением увеличение ЛСС может быть фактором риска нарушения газообмена.
У пациентов с ХОБЛ повышение постнагрузки ПЖ сопровождается его большей производительностью. Чем выше Р ср ЛА, тем больше работа ПЖ (r=0,84, р=0,000) и его мощность (r=0,84, р=0,000). Подъем ЛСС так же сопровождается усилением работы ПЖ (r=0,73, р=0,000) и его мощности (r=0,74, р=0,000). С увеличением работы ПЖ уменьшается насыщение крови кислородом. Выявлены обратные корреляционные связи между показателями работы ПЖ и сатурацией кислорода крови (r=- 0,30, р=0,02). Данные представлены в табл. 4.
Таблица 4. Эхокардиографические показатели правого желудочка у больных ХОБЛ с разной массой тела
У больных ХОБЛ с увеличением ИМТ (F1=0,70) и толщины ПМЖ (F1=0,58) повышается работа (F1=0,75) и мощность (F1=0,68) ЛЖ, а также работа (F1=0,81) и мощность (F1=0,78) ПЖ. Увеличение производительности обоих желудочков ассоциировано уменьшением насыщения крови кислородом (F1=-0,51), что связано с возрастающей потребностью миокарда в кислороде.
У пациентов ХОБЛ увеличение иММЛЖ ассоциировано ростом производительности миокарда ЛЖ, в виде его работы (F1=0,83) и мощности (F1=0,71). По данным корреляционного анализа выявлено, что с ростом толщины свободной стенки ПЖ повышается его работа (r=0,33, р=0,008) и мощность (r=0,43, р=0,00006). Таким образом, гипертрофия стенок левого и правого желудочка усиливают насосную способность сердца, увеличивая потребность миокарда в кислороде.
Выводы. У больных ХОБЛ с ростом ИМТ увеличивается преднагрузка на ЛЖ и постнагрузка на ПЖ, что приводит к повышению производительности желудочков в виде работы и мощности. Для больных ХОБЛ в сочетании с избыточным весом и ожирением повышение ЛСС может быть фактором риска нарушения газообмена. Увеличение ИМТ и ПМЖ у пациентов с ХОБЛ приводит к росту производительности сердца, что характеризуется большей потребностью миокарда в кислороде.
