Сердечно - сосудистые заболевания занимают ведущие позиции в смертности населения, на долю которых приходится 54% и позволяет отнести их к неинфекционным заболеваниям. 90% приходится на ишемическую болезнь сердца, а одним из самых частых ее проявлений является острый коронарный синдром.
При остром коронарном синдроме возникает вначале ишемия, которая ведет к некрозу, если вовремя не восстановить коронарный кровоток. Поэтому очень важна ранняя реваскуляризация в пораженной артерии, что способствует ограничению зоны некроза миокарда и снижению частоты возникновения опасных для жизни аритмий [7].
Коронарный кровоток может восстановиться двумя путями: первый – это спонтанное восстановление происходит вследствие прекращения коронарного ангиоспазма и усиления коллатерального кровотока в ишемизированном участке миокарда. Второй – искусственная реперфузия (тромболитическая терапия или хирургические методы лечения – чрескожная транслюминальная баллонная ангиопластика, стентирование, аортокоронарное шунтирование) [8].
Но при проведении реперфузии остается риск развития нарушений ритма сердца, которые в данном случае являются осложнением инфаркта миокарда, но и являются маркерами реперфузии, что говорит о том, что кровоток в пораженной артерии восстановлен, и терапия эффективная. Появление нарушений ритма сердца связывают с несколькими механизмами, одними из которых, является кислородный и кальциевый парадоксы. Они заключаются в реоксигенации ишемизированной ткани с образованием свободных радикалов кислорода [1]. Возникает патологический автоматизм и повышается триггерная активность из-за возникновения поздних постдеполяризаций, связанных с перегрузкой ионами кальция [5]. В 25% случаев развиваются аритмии re-entry. Отмечается также зависимость длительности ишемизированного участка миокарда и повышения риска развития реперфузионных аритмий, связанные с вымыванием токсических веществ в кровь, что придает ткани гетерогенность и электрическую нестабильность [3].
Зафиксировать возникновение аритмий позволяет длительный мониторинг записи электрокардиографии после проведенного восстановления кровотока. К реперфузионным аритмиям относятся: синусовая брадикардия, ускоренный идиовентрикулярный ритм, желудочковая экстрасистолия, желудочковая тахикардия, фибрилляция желудочков.
Целью исследования является показать виды нарушений ритма сердца, их процентное количество после механической реваскуляризации и тромболитической терапии у больных с инфарктом миокарда без зубца Q и оценить являются ли реперфузионные аритмии осложнением.
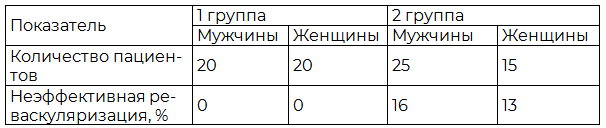
Материалы и методы. В исследовании было включено 80 пациентов с инфарктом миокарда без зубца Q. Исследование проводилось на базе БУЗ ВО «Воронежской областной клинической больницы №1» и БУЗ ВО «Городской клинической больницы №3» в период с 2012 по 2013 г. Больные были разделены на 2 группы. Первую группу составили пациенты, которым была проведена механическая реваскуляризация в первые 12 часов (баллонная ангиопластика и стентирование) – 40 человек (20 (50%) мужчины и 20 (50%) женщины), имевших средний возраст 55,7 ± 12,7 и 59,9 ± 11,9 лет, соответственно, и вторую группу – 40 человек (25 (62,5%) мужчин и 15 (37,5%) женщин) имевших средний возраст 56,3 ± 10,6 и 58,4 ± 12,2 лет, соответственно, которым была проведена тромболитическая терапия препаратом актилизе, который вводился сначала внутривенно болюсом, затем инфузионно, при этом доза препарата составила 1мг/кг (не более 100мг); вначале осуществлялось болюсное введение – 15 мг, а затем инфузия 0,75мг/кг в течение 30мин (не более 50мг) и 0,5мг/кг (не более 35мг) в течение последующего 1 часа (общая продолжительность инфузии составила 1,5 часа) [2]. Характеристика исходных групп пациентов представлена в табл. 1.
Таблица 1. Характеристика исходных групп пациентов с инфарктом миокарда без зубца Q

У всех пациентов исследовались общий анализ крови, мочи, биохимический анализ, биохимические маркеры некроза миокарда – креатинфосфокиназа, тропониновый тест. Использовались постоянный мониторинг электрокардиографии в течение первых суток и холтеровское мониторирование с использованием системы «Кардиотехника» (ИНКАРТ, Санкт-Петербург) на третьи сутки, где оценивались все виды нарушений ритма сердца, их тип и количество аритмий, взаимосвязь с сутками, интерпретация ишемических изменений сегмента ST.
Проводилась коронароангиография – инвазивный рентгенографический метод исследования коронарных артерий, их просвета после селективного интракоронарного введения контрастного вещества, оценки анатомического строения и степени обструкции их просвета [4, 6], с последующим их восстановлением, путем транслюминальной баллонной ангиопласики и постановкой стента в первые 12 часов. Коронароангиография выполнялась всем пациента в данном исследовании на ангиографической установке GE Innova 3100 и ангиографе фирмы Toshiba “Infinix” с функцией 3D моделирования.
Механическая реваскуляризация заключалась в проведении пункции стенки общей бедренной артерии под местной анестезией 0,5% - 20 мл новокаином, проведении катетера в нисходящую аорту.
Далее устанавливался интродьюссер специального размера, оценивалась зона поражения и проводилась транслюминальная баллонная ангиопласика с помощью специального баллончика, где измерялось внутрисосудистое давление в области стеноза и дистальнее места поражения, а затем двукратное раздувание баллончиком и снова измерение давления для постановки стента, где определялся остаточный стеноз и на баллоне-катетере раскрывался и ставился стент «Biomatrix» в область сужения.
Все пациенты получали стандартную антиишемическую и антитромботическую терапию, которая включала в себя бета-адреноблокаторы, статины, ингибиторы ангиотензин-превращающего фермента, плавикс, нитраты. В случае проведения тромболитической терапии больные получали вместо плавикса аспирин.
Статистическая обработка материала проводилась с помощью программы прикладной статистики StatPlus 2009.
Результаты и их обсуждение. Механическая реваскуляризация оказалась более эффективная, чем тромболитическая терапия в первые 12 часов, потому что в случае механической реваскуляризации (баллонная ангиопластика или баллонная ангиопластика со стентированием) проходимость пораженной коронарной артерии была восстановлена полностью. При проведении тромболитической терапии не всегда удавалось полностью восстановить кровоток с первого раза (в 15% - 6 человек (4 (16%) мужчин и 2 (13%) женщины) случаев, где тромболитическая терапия была недостаточно эффективна), что подтверждалось клинической симптоматикой, электрокардиографией, маркерами некроза миокарда, а также нарушением ритма сердца, результаты представлены в табл. 2.
Таблица 2. Эффективность проведения реваскуляризации в обеих группах
У пациентов обоих групп не было выявлено патологических сдвигов в общем анализе крови и мочи, а в биохимическом анализе у 58,7% были завышены показатели липидного спектра, а именно общего холестерина, липопротеидов низкой плотности и у 10% были повышены триглицериды, которые в последствие были скорригируемые приемом статинов и фибратов.
Уровни биомаркеров повреждения миокарда, а именно креатинфосфокиназа, имели высокие значения, тропониновый тест - положительный, на электрокардиографии не регистрировался патологический зубец Q в обеих группах пациентов, что позволило отнести данных пациентов к группе инфаркта миокарда без зубца Q.
По данным суточного мониторирования в первые сутки в 80% при тромболитической терапии наблюдались реперфузионные аритмии, что говорило об эффективности проведения тромболитической терапии, которые проявлялись в виде желудочковой экстрасистолии – одиночной, парной, групповой, частой. В 25% случаев были зафиксированы эпизоды групповых экстрасистол «R на T» (наслоение преждевременного желудочкового комплекса на зубец Т), которые могут способствовать развитию жизненно опасных аритмий и внезапной смерти.
В 70% случаев регистрировалась желудочковая тахикардия после восстановления коронарного кровотока и у 20% больных с сохраненной окклюзией. В 25% случаев развитию желудочковой тахикардии способствует формирование петли re-entry в зонах миокарда с негомогенными свойствами рефрактерности и проводимости. Желудочковая тахикардия имела различную морфологию и продолжительность. Она регистрировалась в виде мономорфной (желудочковые комплексы одинаковой формы) и полиморфной (морфология комплексов различная). Желудочковая тахикардия, длящаяся более 30 секунд сопровождалась нарушением гемодинамики и в 2,5% случаев трансформировалась в фибрилляцию желудочков.
При восстановлении коронарного кровотока фибрилляция желудочков развивалась достаточно редко – у 5% пациентов. Она возникла у 1 пациента после проведенной тромболитичекой терапии через 2,5 часа от начала симптомов инфаркта миокарда, и у 1 пациента трансформировалась из желудочковой тахикардии в фибрилляцию желудочков через 4 часа после начала острого инфаркта миокарда. В данном случае тромболизис был проведен через 1 час от начала острого инфаркта миокарда (зона ишемии была 1 час, что является предиктором развития ранней фибрилляции желудочков). В последующем угрожающие жизни аритмии развиваются реже, так как большинство клеток в зоне инфаркта некротизированы.
У 70% больных после восстановления кровотока тромболитической терапией регистрировался ускоренный идиовентрикулярный ритм в первые 6 часов и у 25% пациентов, которым провели тромболизис, где окклюзия сохранялась.
Анализируя данные механической реваскуляризации, которая была эффективна в 100% случаев, были зафиксированы реперфузионные аритмии в 75% после проведения баллонной ангиопластики и стентирования. Аритмический синдром проявлялся в виде желудочковых экстрасистол – мономорфных, полиморфных, одиночных, парных, групповых в 20%, эпизоды групповых желудочковые экстрасистол «R на T» в 10%, которые считаются наиболее неблагоприятными, так как способствуют трансформации в желудочковую тахикардию.
Желудочковая тахикардия была зарегистрирована у 14-и больных после восстановления коронарного кровотока в виде мономорфной, длящейся несколько секунд и не сопровождающаяся нарушением гемодинамики и у 2-х в виде мономорфной, сопровождающейся нарушением гемодинамики и длящейся более 30 секунд.
Фибрилляция желудочков развивалась у 1 пациента и была быстро купирована. Ускоренный идиовентрикулярный ритм зафиксировали у 11 больных инфарктом миокарда без зубца Q.
Выводы
1. Реперфузионные аритмии являются результатом метаболических изменений миокарда, вследствие ишемии и некроза сердечной мышцы при восстановлении кровотока, поэтому их можно считать осложнением, но появление в первые часы после реваскуляризации ускоренного идиовентрикулярного ритма, желудочковой экстрасистолии, желудочковой тахикардии и фибрилляции желудочков можно отнести к неинвазивным маркерам подтверждения наличия успешной реперфузии.
2. Оценивая механическую реваскуляризацию и тромболитическую терапию, предпочтение отдается первой, т.к. возникновение реперфузионных аритмий значительно ниже, а эффективность ее в 100% случаев, чего нельзя сказать о тромболитической терапии, но которую можно проводить на догоспитальном этапе.
3. Возможность купирования аритмического синдрома на догоспитальном этапе ниже, а проведение механической реваскуляризаци возможно только в стационарных условиях, где оказание высокоспециализированной помощи значительно эффективнее.
