С клинической точки зрения определение вариабельности ритма сердца (ВСР) является неинвазивным методом количественной оценки вегетативной регуляции сердечного ритма. Считается, что снижение показателей ВСР свидетельствует о нарушении вегетативного контроля сердечной деятельности и неблагоприятно для прогноза.
Показатель SDNN (суммарный эффект вегетативной регуляции кровообращения) отражает все периодические составляющие вариабельности ритма, т.е. позволяет оценить суммарный эффект вегетативной регуляции кровообращения в процессе лечения.
Цель исследования: смоделировать динамику SDNN на основании исследуемых показателей.
Материалы и методы. Основной комплекс исследований, представленный в работе, выполнен на базе «Воронежской областной клинической больницы № 1». Под наблюдением находилось 120 пациентов ишемической болезнью сердца (ИБС), стабильной стенокардией напряжения II-III функциональных классов (ФК). Хроническая сердечная недостаточность (ХСН) I-II А стадии, в сочетании с легкой хронической обструктивной болезнью легких (ХОБЛ). Средний возраст больных, включенных в исследование, составлял от 50 до 60 лет. Половой состав пациентов, включенных в исследование: 100 % мужчин. Диагноз стабильной стенокардии напряжения был подтвержден клинически и результатами суточного мониторирования электрокардиограммы (ЭКГ). У 102 больных (88 %) отмечена гипертоническая болезнь 1-2 степени, II стадии, медикаментозно корригированная до целевых значений артериального давления (АД).
Критерии включения: пациенты со стабильной стенокардией напряжения II-III ФК, ХОБЛ, подписавших информированное согласие на участие в исследование.
Не включены пациенты с анамнезом инфаркта миокарда, инсульта, сахарного диабета, хронической почечной недостаточности, тяжелой артериальной гипертензией, тяжелых нарушений бронхо-легочной системы, фибрилляцией предсердий, частой экстрасистолией; не подписавших протокол информированного согласия.
При амбулаторном обследовании всем пациентам проводились клинико-лабораторные исследования – общий анализ крови, общий анализ мочи, биохимия крови, ЭКГ в 12 отведениях, заполнение опросника SF-36. На аппарате «ЭТОН» оценивалась ФВД (функция внешнего дыхания): - ФЖЕЛ выд. (форсированная жизненная емкость легких), ОФВ 1 выд. (объем форсированного выдоха за 1 сек), ПОС выд. (пиковая объемная скорость), МОС 25 выд. (максимальная объемная скорость при выдохе 25 %), МОС 50 выд., МОС 75 выд., СОС 0,2-1,2 выд., СОС 25-75 выд. (средняя объемная скорость), СОС 75-85 выд., ТФЖЕЛ выд. (время выполнение форсированного выдоха) и др.
Классификация больных по общему состоянию проводилась на основе алгоритма классификации на базе линейных дискриминантных функций в виде ИС (индекса состояния) с учетом удельных весов признаков, реальных значений признаков и пороговых значений [1].
Диапазон значений ИС от 1 до 10.
1-2 – норма, 2-4 условная норма, 4-6 умеренное нарушение , 6-8-значительное, 8-10 резкое. Осуществлялась также суточная запись ЭКГ на аппарате «Холтер-ДМС» и оценка параметров ВРС.
При этом оценивались: Частоты пульса - Средний уровень функционирования системы кровообращении; SDNN - Суммарный эффект вегетативной регуляции кровообращения; RMSSD - Активность парасимпатического звена вегетативной регуляции; pNN50 - Показатель степени преобладания парасимпатического звена регуляции над симпатическим (относительное значение); СВВР – средняя взвешенная вариация ритмограммы. После оценки функции внешнего дыхания были выделены: - 36 человек с увеличенным ИС с ХОБЛ после аортокоронарного шунтирования (АКШ) возрастом 53±2 года с выявленным ускоренным синусовым ритмом- 87 ± 3 уд/мин.
Пациенты рандомизированы в две группы: 1) получавших стандартную терапию ИБС (сиднофарм 2 мг/2 р. в день/кардикет 1 кап 1 р. в день, кардиомагнил 75/150 мг 1 р./в день триметазидин 35 мг 2р. в день и аторвастатин 20-40 мг в сутки) и терапию, направленную на улучшение бронхиальной проходимости - бронхолитики (тиотропия бромид или его комбинацию с β-2 агонистами длительного действия), муколитики; 2) с добавлением ивабрадина в дозе 10 мг/сут (по 5 мг 2 раза в сутки) первый месяц, по 7,5 мг 2 раза в сутки в течение последующих 2 месяцев; - 40 человек с увеличенным ИС больных ИБС с ХОБЛ возрастом 55±2 года с выявленным ускоренным синусовым ритмом. Случайным образом пациенты поделены в две подгруппы: 3) получавших стандартную терапию ИБС 4) с добавлением ивабрадина в дозе 10 мг/сут (по 5 мг 2 раза в сутки) первый месяц, по 7,5 мг 2 раза в сутки в течение последующих 2 месяцев. Клинико-лабораторные данные не свидетельствовали об обострении ХОБЛ. Динамическое наблюдение осуществлялось каждый месяц (4 визита). Таким образом, сформированы группы: ИБС+ББ (ИБС+β-блокатор), ИБС+ХОБЛ, ИБС+ХОБЛ+кораксан, АКШ+ББ, АКШ+ХОБЛ, АКШ+ХОБЛ+кораксан. Пациенты групп АКШ+ББ и ИБС+ББ в связи с максимальной дозой препарата и остающимися болями в сердце требовали коррекции лечения с добавлением к терапии кораксана (5 визит). Ивабрадин не влияет на артериальное давление, поэтому риск гипотензии при его применении в виде монотерапии или в составе комбинированной терапии отсутствует.
Результаты и их обсуждение. Назначение кораксана в группах исследования: усиливает антиангинальный эффект базисного лечения, снижает количество экстрасистол и число приступов стенокардии по данным ЭКГ, суточного мониторирования ЭКГ, улучшает качество жизни пациентов, по шкалам GH, SF, BP, снижает суммарное количество и время ишемической депрессии, расширяет диапазон вариабельности ритма сердца, способствует увеличению SDNN и СВВР. Не оказывает отрицательного воздействия на гемодинамические и электрофизиологические показатели [2].
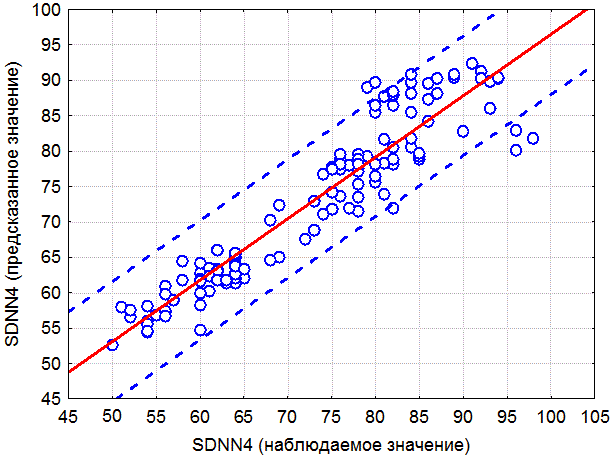
Рис. 1. Скатерограмма эффективности прогнозирования суммарного эффекта вегетативной регуляции кровообращения в процессе лечения на 4 визите.
На рис. 1 по абсциссе отложены значения реально наблюдаемого значения SDNN на 4 визите. По ординате – SDNN прогнозируемый с помощью, разработанной нами математической модели. На пересечении абсциссы и ординаты помещен маркер для каждого из 120 наблюдений из 6 групп. При 100% совпадении наблюдаемого и предсказанного значений SDNN, маркеры легли бы на одну прямую. В данном случае они образуют облако, рассеянное вокруг этой прямой, пунктиром обозначен 95% доверительный интервал.
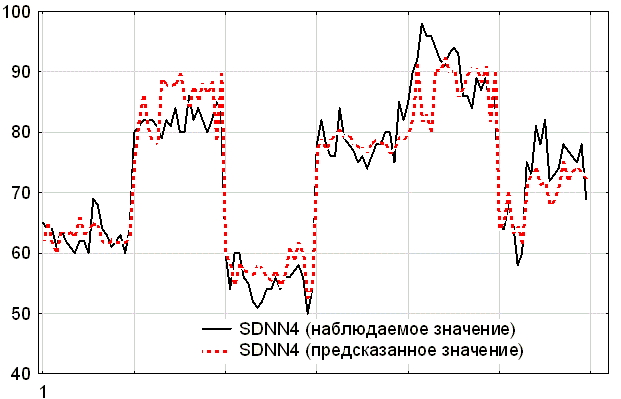
Рис. 2. График эффективности прогнозирования суммарного эффекта вегетативной регуляции кровообращения для 6 исследуемых групп на 4 визите.
На рис. 2 можно выделить шесть участков (отмечены на абсциссе линиями сетки), соответствующих 6 группам пациентов. Внутри каждой группы различия между наблюдаемым и предсказанным значением не достигают клинически значимого уровня (табл. 1). Средняя ошибка предсказания SDNN4 составляет от сотых долей (в группе ИБС+ББ), до 2,9 (в группе ИБС+кораксан+ХОБЛ).
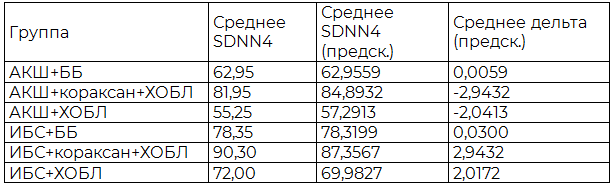
Таблица 1. Средняя погрешность модельного прогнозирования SDNN4
Известным «слабым местом» регрессионных моделей является их «переобучаемость». То есть, такие модели способны показывать превосходные результаты на обучающем множестве, на котором было сгенерировано уравнение регрессии. В то же время в реальной работе качество предсказания оказывается не таким высоким. Поэтому целесообразно тестирование регрессионной модели на «экзаменационном» наборе данных. То есть на таких данных, которые не использовались при создании решающего уравнения.
В качестве экзаменационного набора данных мы использовали показатели SDNN на 5 визите (табл. 2; рис. 3, 4).
Таблица 2. Средняя погрешность модельного прогнозирования SDNN5

Средняя погрешность работы прогностической модели на экзаменационном наборе данных не отличается от таковой на обучающем множестве, что позволяет сделать вывод о достаточной стабильности полученной регрессионной модели.
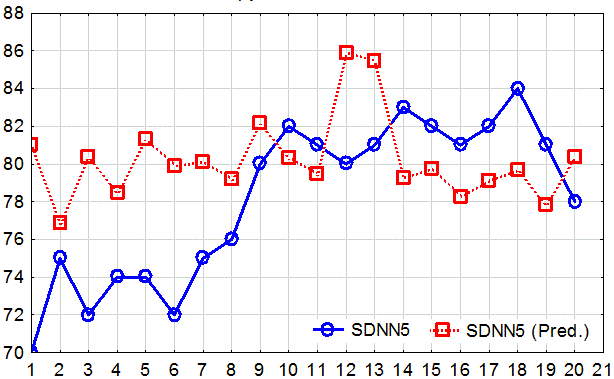
Рис. 3. График эффективности прогнозирования суммарного эффекта вегетативной регуляции кровообращения в группе АКШ+ББ на 5 визите.
На графике (рис. 3) круглыми маркерами отмечены значения показателя SDNN на 5 визите, пунктирным графиком с квадратными маркерами показаны предсказанные величины показателя SDNN на 5 визите. Можно отметить, что и наблюдаемые, и предсказанные значения превышают клинически значимый рубеж в 70 мс. Таким образом, прогностическая модель утверждает, что на фоне приема кораксана произойдет нормализация показателя SDNN, и мы реально наблюдаем это у пациентов, принимающих кораксан. Аналогичная картина отмечается и в группе ИБС+ББ (рис. 4).
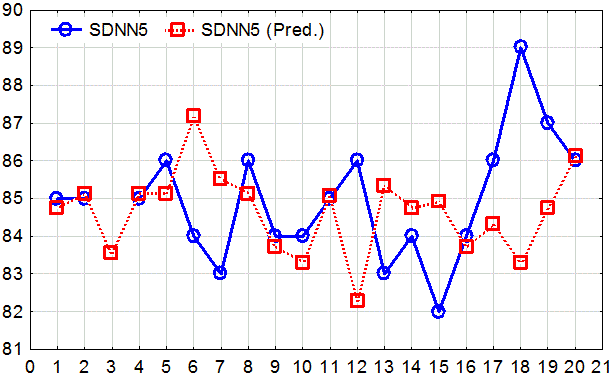
Рис. 4. График эффективности прогнозирования суммарного эффекта вегетативной регуляции кровообращения в группе ИБС+ББ на 5 визите.
Выводы. Таким образом, нами построена модель, позволяющая оценить воздействие кораксана при его использовании в лечении больных ИБС после АКШ и условиях консервативной терапии. Практическое значение этой модели в том, что она помогает предсказать будущее значение SDNN при наличии известных значений SDNN, СВВР, ИС и отсутствия или наличия кораксана.
