Введение. Изменения, развивающиеся в сердечно-сосудистой системе при дисфункции щитовидной железы, являются результатом как прямого действия тиреоидных гормонов на миокард, так и косвенного влияния, опосредованного через гемодинамические нарушения. Прямое действие трийодтиронина (Т3) на кардиомиоциты осуществляется с помощью экстрануклеарных и нуклеарных механизмов. Первый регулирует транспорт аминокислот, глюкозы, катионов через плазматическую мембрану клетки. Второй механизм заключается в связывании Т3 со специфическими рецепторами ядра кардиомиоцита. Т3 способствует транскрипции генома тяжелых цепей миозина с перераспределением его изоформ. При гипотиреозе возрастает пропорция бета-изоформы тяжелых цепей миозина, понижается аденозинтрифосфатазная активность миозина и, соответственно, ослабляется сила и скорость сокращения миокарда желудочков. Так же состояние гипотиреоза характеризуется уменьшением числа бета-адренорецепторов, этим объясняют более низкую частоту развития аритмий при гипофункции щитовидной железы. Установлено, что у лиц с гипотиреозом секреция норадреналина и содержание его в плазме крови повышено. Норадреналин, являясь, в основном, стимулятором альфа-адренорецепторов, может способствовать спазму коронарных артерий. Гипотиреоз, характеризуется снижением сократительной способности миокарда, уменьшением фракции выброса левого желудочка. Состояние гипотиреоза сопровождается пролонгацией диастолы, увеличением времени изоволюметрической релаксации левого желудочка.
Проанализировав литературные данные с 1970-2001 г., касающиеся влияния субклинического гипотиреоза (СГ) на сердечно-сосудистую систему, автор [5] делает заключение, что СГ обуславливает систолическую дисфункцию левого желудочка при физической нагрузке, диастолическую дисфункцию - в покое.
Нарушение диастолической функции миокарда левого желудочка при СГ подтверждается результатами целого ряда исследований. У пациентов с субклиническим гипотиреозом наблюдаются более продолжительный период изоволемической релаксации и снижение скорости наполнения левого желудочка, что свидетельствует о нарушении диастолической функции [4, 6, 8, 9]. Эти изменения могут рассматриваться как фактор неблагоприятного прогноза, поскольку в общей популяции диастолическая дисфункция левого желудочка ассоциируется с более высоким риском смертности [6, 10].
Целью работы [1] было оценить особенности показателей гемодинамики и геометрические параметры по данным эхокардиографии у пациентов с различными клиническими вариантами аутоиммунного тиреоидита (АИТ). Все больные были разделена на 3 группы в зависимости от функции щитовидной железы. Согласно полученным результатам авторы сделали заключение, что снижение функции щитовидной железы является фактором риска гипертрофии левого желудочка и диастолической дисфункции миокарда. При СГ и манифестном гипотиреозе (МГ) возрастает частота развития эксцентрической гипертрофии миокарда – 25,9 и 60% соответственно (р<0,04). Для больных с СГ и МГ характерны умеренные изменения морфофункциональных параметров сердца в виде увеличения размера и дилатации полости левого предсердия и толщины стенок миокарда левого желудочка (относительная гипертрофия), формирование систолической и диастолической дисфункции миокарда левого желудочка (10, 7,4 и 25% соответственно) по сравнению с контрольной группой. Снижение концентрации тиреоидных гормонов при СГ и МГ приводит к уменьшению сократительной способности сердца.
Состояние диастолической функции миокарда при аутоиммунном тиреоидите и субклиническом гипотиреозе оценивались в работе отечественных ученых [2]. Авторы сделали заключение, что субклинический гипотиреоз ассоциируется с нарушениями глобальной и сегментарной диастолических функций левого и правого желудочков и увеличением жесткости артериальных стенок.
Особого внимания заслуживают данные об исследовании [3]. Были изучены состояние диастолической функции сердца у пациентов с аутоиммунным тиреоидитом и уровнем тиреотропного гормона гипофиза (ТТГ), лежащим в разных частях референсного интервала и субклинического диапазона, также оценивалась ее взаимосвязь со степенью тиреоидной недостаточности и другими метаболическими и функциональными показателями. Среди пациенток с ТТГ≥6 мЕд/л отмечены самые высокие показатели индекса массы миокарда левого желудочка (ИММЛЖ). Изменения диастолы являлись бивентрикулярными и наиболее значимыми также при уровне ТТГ>6 мЕд/л. Авторы делают заключение, что нарушения диастолической функции сердца при АИТ определяются выраженностью тиреоидной недостаточности и отчасти опосредованы характерными для нее сдвигами в виде структурных изменений миокарда, нарушений липидного обмена и окислительного стресса.
Цель исследования. Оценить особенности показателей гемодинамики и геометрические параметры по данным эхокардиографии (ЭхоКГ) у пациентов с субклиническим гипотиреозом и ишемической болезнью сердца (ИБС).
Материал и методы исследования. В исследование были включены 80 больных с верифицированным диагнозом ИБС. У 40 пациентов выявлен субклинический гипотиреоз: 33 (82,5%) женщины и 7 (17,5%) мужчин. Аутоиммунный тиреоидит был у 27 пациентов (67,5%), узловой зоб у 5 (12,5%), у 4 (10%) гипоплазия щитовидной железы и у 4 (10%) СГ, с неизмененной структурой при ультразвуковом исследовании щитовидной железы. Все больные с СГ были разделены по уровню ТТГ на две группы: 1-я – 25 пациентов с субклиническим гипотиреозом с уровнем ТТГ 4-10 мЕд/л, 2-я – 15 больных с уровнем тиреотропного гормона гипофиза более 10 мЕд/л.
В контрольной группе обследовано 40 пациентов с ИБС без изменения гормонального статуса щитовидной железы (32 женщины и 8 мужчин) сопоставимых по возрасту (средний возраст в контрольной группе 57,93±7,26 лет и 60,5±7,74 лет в группе с субклиническим гипотиреозом соответственно) и индексу массы тела (ИМТ 28,74±5,94 кг/м2 в контрольной группе и 29,72±5,46 кг/м2 в группе СГ соответственно), данных анамнеза, функциональному классу (ФК) хронической сердечной недостаточности.
Критерии включения: стабильная стенокардия I, II, III ФК, перенесенный в прошлом инфаркт миокарда (ПИМ). Критерии исключения: сопутствующие онкологические заболевания в стадии раковой интоксикации, гематологические заболевания в активной стадии, сахарный диабет, тяжелая почечная, печеночная, дыхательная недостаточности, нарушение ритма сердца: пароксизмальная и хроническая формы фибрилляции предсердий, неконтролируемая артериальная гипертензия, стенокардия напряжения IV ФК. Общая характеристика больных ИБС и СГ представлена в табл. 1.
С целью верификации диагноза СГ, помимо сбора анамнеза, оценки объективного статуса, использовались лабораторные и инструментальные методы: определение концентрации тиреотропного гормона (ТТГ), свободного тироксина (св. Т4) и антител к тиреопероксидазе (АТ-ТПО) в сыворотки крови использовали набор реактивов «Architect», Германия, ультразвуковое исследование щитовидной железы. Результаты клинико-лабораторных исследований пациентов с субклиническим гипотиреозом представлены в табл. 2.
Таблица 1. Общая характеристика больных ИБС
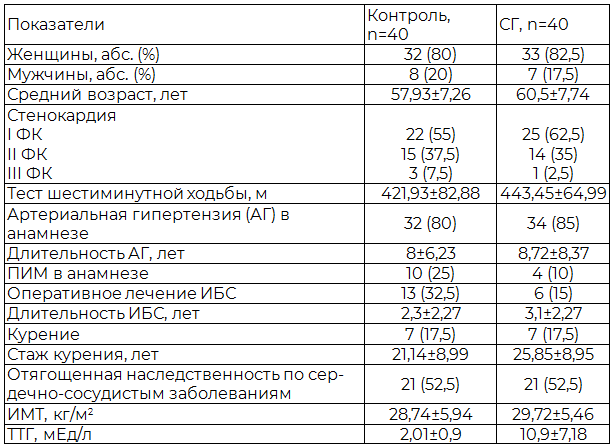
Примечание: здесь и далее значения приведены в М±m и абс. (%). Все различия между группами недостоверны, кроме уровня ТТГ (p<0,0001) и длительности ИБС (p<0,05).
Таблица 2. Общая характеристика больных ИБС в сочетании СГ
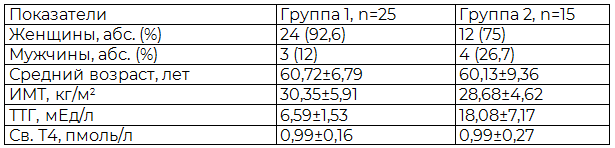
Примечание: все различия между группами недостоверны, кроме уровня ТТГ (p<0,0001).
Всем больным выполняли ЭхоКГ ультразвуковое исследование сердца на аппарате ультразвукового диагностического сканера General Electric — GE Vivid 7 Pro (США) с датчиком 4V2с 2-4 МГц с регистрацией результатов на магнито-оптических дисках в соответствии стандартной методике, рекомендованной Ассоциацией американских кардиологов (1987). Изучались структурные параметры сердца: переднезадний размер левого предсердия (ЛП, см), полости правого предсердия (ПП, см), полости правого желудочка в конце диастолы (ПЖ, см), конечный систолический размер левого желудочка (КСР ЛЖ, см), конечный диастолический размер левого желудочка (КДР ЛЖ, см), толщина задней стенки левого желудочка в диастолу (ТЗСЛЖд, см), толщина межжелудочковой перегородки в диастолу (ТМЖПд, см), конечный систолический объем левого желудочка (КСО, мл) и конечный диастолический объем левого желудочка (КДО, мл), фракция выброса левого желудочка (ФВ ЛЖ, %), ударный объем (УО, мл). Массу миокарда левого желудочка (ММЛЖ) рассчитывали по кубической формуле, рекомендованной Американским обществом эхокардиографии (American Society of Echocardiography – ASE), первоначально предложенной B.L. Troy и соавт. [11] и соавторами и модифицированной R.B. Devereux [7].
ММЛЖ (в граммах) = 0,8*(1,04*(ТМЖПД + КДР + ТЗСЛЖД)3–КДР3)+0,6;
где КДР - конечный диастолический размер, ТЗСЛЖД - толщина задней стенки левого желудочка в диастолу, ТМЖПД - толщина межжелудочковой перегородки в диастолу, выраженные в сантиметрах.
Также рассчитывали индекс массы миокарда левого желудочка (ИММЛЖ, г/м2) как отношение ММЛЖ к площади поверхности тела. Гипертрофию миокарда левого желудочка диагностировали при ИММЛЖ 134 г/м2 и более у мужчин и 110 г/м2 и более у женщин. Относительную толщину стенки (ОТС) левого желудочка рассчитывали по формуле: ОТС = 2 х ЗСЛЖ/КДР. Нормальной геометрией считали ОТС<0,45 при нормальном ИММЛЖ, концентрическое ремоделирование диагностировали при ОТС>0,45 и нормальном ИММЛЖ, концентрическую гипертрофию левого желудочка – при ОТС>0,45 и увеличенном ИММЛЖ, эксцентрическую гипертрофию левого желудочка – при ОТС<0,45 и увеличенном ИММЛЖ. Для оценки диастолической функции левого желудочка рассчитывали следующие показатели трансмитрального кровотока: максимальную скорость раннего диастолического наполнения (пик Е), максимальную скорость наполнения левого желудочка во время систолы предсердий (пик А), отношение этих скоростей E/A и время изоволюметрического расслабления (ВИР, с). Признаками нарушения диастолической функции считали увеличении ВИР более 100 мс, уменьшение отношения данных скоростей Е/А менее 1,0.
Систематизация материала была выполнена с применением программного пакета электронных таблиц Microsoft EXCEL, статистические расчеты с применением пакета программ «Statictica 8.0». Для оценки межгрупповых различий использован критерий Манна-Уитни, для оценки качественных различий – критерий c2 Пирсона. Анализ взаимосвязей переменных проводился методом ранговой корреляции Спирмена (rs). Различия считали статистически значимые при p<0,05.
Результаты и их обсуждение. Сопоставление показателей ЭхоКГ у больных ИБС с субклиническим гипотиреозом в сравнении с группой контроля позволило уточнить структурно-функциональные показатели сердца у данных категорий больных (табл. 3).
Таблица 3. Эхо-кардиографическая характеристика обследованных пациентов
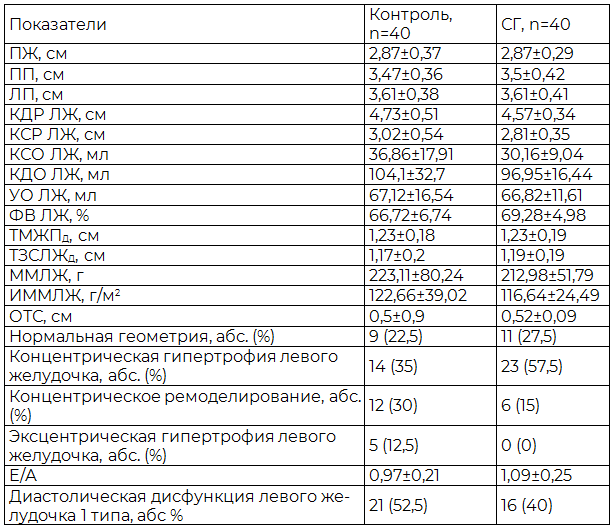
Примечание: все различия между группами недостоверны, кроме ЛП (p<0,0001), КСО ЛЖ (p-0,05), КДР ЛЖ (p<0,0001), ФВ ЛЖ (p-0,044), Е/А (p-0,026).
Таблица 4. Эхо-кардиографическая характеристика больных ИБС в сочетании СГ
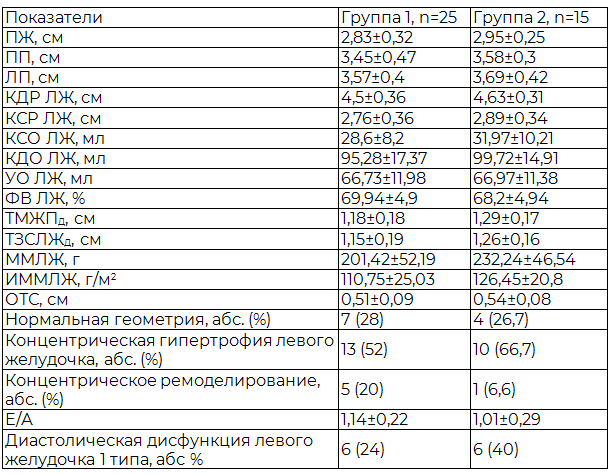
Примечание: все различия между группами недостоверны кроме ИММЛЖ (p-0,043).
Передне-задний размер левого предсердия у больных субклиническим гипотиреозом был больше на 3,4% (p<0,0001) по сравнению с контрольной группой. КСО ЛЖ больше на 11,8% (p-0,05), КДР ЛЖ больше на 2,9% (p<0,0001), а ФВ ЛЖ меньше на 2,5% (p-0,044), чем в группе контроль соответственно.
Достоверной корреляционной связи между сократительной способностью левого желудочка и уровнем ТТГ и св. Т4 не обнаружено (p-0,27 и p-0,25 соответственно). Обнаружена положительная корреляционная связь средней силы между уровнем ТТГ и ПП (r-0,33, p-0,037).
При сравнении показателей в группе с субклиническим гипотиреозом с уровнем ТТГ 4-10 мЕд/л и в группе больных с уровнем тиреотропного гормона гипофиза более 10 мЕд/л (табл. 4) также не выявлены достоверные различия по данным эхокардиографии, за исключением ИММЛЖ (p-0,043). В группе пациентов с уровнем ТТГ более 10 мЕд/л выявлена относительная гипертрофия левого желудочка: ТМЖПД 1,29±0,17 см, ТЗСЛЖД 1,26±0,16 см.
Обнаружены положительные корреляционные связи средней силы между уровнем св. Т4 и ПЖ (r-0,49, p-0,048), ТЗСЛЖД (r-0,53, p-0,033), ММЛЖ (r-0,5, p-0,047).
Признаки диастолической дисфункции левого желудочка с уменьшением Е/А были выявлены у 6 (40%) больных с уровнем ТТГ 4-10 мЕд/л и у 6 (24%) больных с уровнем ТТГ более 10 мЕд/л. При корреляционном анализе не было выявлено достоверной связи между диастолической дисфункцией левого желудочка 1 типа и уровнем ТТГ.
Анализ структуры миокарда выявил, что при субклиническом гипотиреозе концентрическое ремоделирование миокарда было обнаружено у 6 (15%) и 12 (30%) группы контроль. ИММЛЖ в группе пациентов с субклиническим гипотиреозом с уровнем ТТГ > 10 мЕд/л был на 14,2% больше, чем в группе с уровнем ТТГ 4-10 мЕд/л. Оценка эхокардиографических критериев гипертрофии левого желудочка свидетельствовала о следующих особенностях: 23 (57,5%) имели концентрическую гипертрофию, а эксцентрическая гипертрофия в группе СГ не встречалась. Типы ремоделирования левого желудочка у больных ИБС представлены на рис. 1.
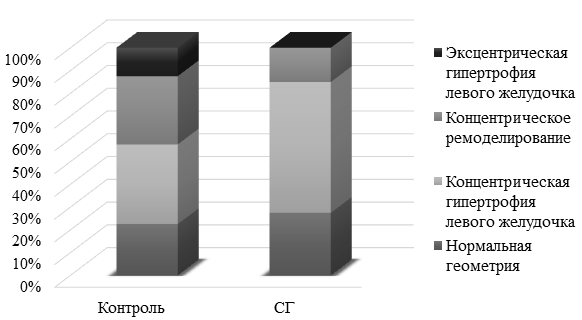
Рис. 1. Распределение типов геометрических моделей левого желудочка у больных ИБС.
В группе с уровнем ТТГ более 10 мЕд/л 10 (66,7%) пациентов имели концентрическую гипертрофию левого желудочка и 1 (6,6%) пациент концентрическое ремоделирование левого желудочка, в группе с уровнем тиреотропного гормона 4-10 мЕд/л 13 (52%) больных имели концентрическую гипертрофию левого желудочка и 5 (20%) концентрическое ремоделирование соответственно. Типы ремоделирования левого желудочка у больных ИБС и СГ представлены на рис. 2.
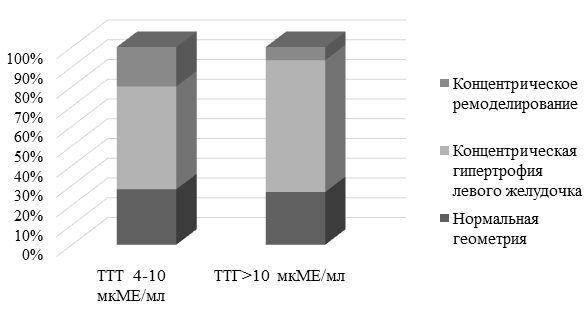
Рис. 2. Распределение типов геометрических моделей левого желудочка у больных ИБС с сочетанием СГ.
При корреляционном анализе не было выявлено достоверной связи между выраженностью концентрической гипертрофии левого желудочка и уровнем ТТГ, возрастом. Обнаружена положительная корреляционная связь средней силы между уровнем ТТГ и ОТС (r-0,32, p-0,042).
Таким образом, можно предположить, что субклинический гипотиреоз предрасполагает к концентрической гипертрофии левого желудочка и диастолической дисфункции миокарда. Для больных СГ и ИБС характерно умеренное изменения морфофункциональных особенностей сердца в виде увеличения ИММЛЖ (p-0,043) в группе с уровнем ТТГ > 10 мЕд/л.
Выводы
1. Данные полученные ЭхоКГ у больных с сочетанием ИБС и субклиническим гипотиреозом выявили умеренные изменения морфофункциональных параметров сердца в виде увеличения размера полости левого предсердия и левого желудочка, незначительного снижения фракции выброса левого желудочка. Передне-задний размер левого предсердия у больных субклиническим гипотиреозом был больше на 3,4% (p<0,0001) по сравнению с контрольной группой. КСО ЛЖ больше на 11,8% (p-0,05), КДР ЛЖ больше на 2,9% (p<0,0001), а ФВ ЛЖ меньше на 2,5% (p-0,044), чем в группе контроль соответственно.
2. Гипертрофия левого желудочка концентрического типа была отмечена в группе с уровнем ТТГ более 10 мЕд/л у 10 (66,7%) пациентов и в группе с уровнем тиреотропного гормона 4-10 мЕд/л у 13 (52%) больных. При корреляционном анализе не было выявлено достоверной связи между выраженностью концентрической гипертрофии левого желудочка и уровнем ТТГ.
3. Признаки диастолической дисфункции левого желудочка с уменьшением Е/А были выявлены у 6 (24%) больных с уровнем ТТГ 4-10 мЕд/л и у 6 (40%) больных с уровнем ТТГ более 10 мЕд/л. При корреляционном анализе не было выявлено достоверной связи между диастолической дисфункцией левого желудочка 1 типа и уровнем ТТГ.
