Введение. Многочисленные работы в последние десятилетия посвящены исследованию клинической, в том числе прогностической, значимости микроальбуминурии (МАУ), методов ее выявления и количественного определения, а также лечебных мер, направленных на борьбу с данным патологическим состоянием. Интерес к проблеме объясняется тем, что МАУ расценивается как один из ранних неблагоприятных прогностических признаков и факторов риска развития поражения органов-мишеней при таких широко распространенных заболеваниях, как артериальная гипертензия (АГ) и сахарный диабет (СД). В то же время, по данным исследованиям Copenhagen City Heart Study-3 [7,8], и более низкая экскреция альбумина с мочой также может указывать на повышенный риск заболеваний сердечно-сосудистой системы (ССС) и кардиоваскулярной смерти.
МАУ является важнейшим ранним признаком поражения почек, отражающим начальные стадии патологии сосудов (эндотелиальной дисфункции, атеросклероза), и неизменно коррелирует с увеличением заболеваемости ССС и смертности. По данным клинических исследований, даже небольшое повышение экскреции альбумина с мочой ассоциируется со значительным ростом риска кардиоваскулярных событий, в том числе фатальных. Прогрессирующее увеличение уровня МАУ однозначно указывает на ухудшение состояния сосудов и, соответственно, обуславливает дополнительное повышение риска [6,9]. В связи с этим МАУ признана независимым фактором сердечно-сосудистого риска и наиболее ранним (доклиническим) признаком поражения таких уязвимых органов-мишеней, как почки.
МАУ – следствие повышенной потери альбумина из плазмы крови через эндотелий и потому определяется как маркер развития системной эндотелиальной дисфункции. А эндотелиальная дисфункция характерна для ранних стадий атеросклероза и непосредственно связанна с повышением сердечно-сосудистого риска [5,6,9,15]. Недавно установлена связь микроальбуминурии с выраженным коронарным атеросклерозом по данным ангиографии [10]. В одном из субисследований LIFE (Losartan Intervention For Endpoint reduction in hypertension) [15] было выявлено, что повышенная экскреция белка с мочой четко ассоциировано с левожелудочковой гипертрофией, причем независимо от возраста, пола, расы, уровня артериального давления (АД), наличия СД, курения, уровня креатинина в крови. Особенно часто выявляется МАУ при СД и АГ. По разным данным МАУ встречается у 10-40% больных СД 1-го типа и у 15-40% больных СД 2-го типа [6,9,14]. Так, например, в исследовании EUCLID (EURODIAB controlled trial of lisinopril in insulin dependent diabetes) МАУ определялась примерно у 15% из 530 больных СД 1-го типа [11]. Частота обнаружения МАУ возрастает с увеличением длительности заболевания при СД обеих типов. В крупном британском исследовании UKPDS (United Kingdom Prospective Diabetes Study) МАУ выявлялась у 12% больных с впервые выявленным СД 2-го типа и почти у 30% больных с длительностью заболевания более 12 лет [12]. Выявляемость новых случаев МАУ у больных СД может колебаться от 1 до 3 % в год. Под наблюдением большинства исследований, среди нелеченных больных с мягкой и умеренной АГ распространенность МАУ варьирует от 15 до 40%, составляя в среднем около 25%. Частота обнаружения МАУ выше у больных с впервые выявленной АГ и при неадекватной гипотензивной терапии. В крупномасштабном исследовании i-SEARCH (2007) с участием около 22 тыс. больных из 1750 центров МАУ встречалась у большинства пациентов с АГ: в 53-71% случаев, при этом самые высокие уровни экскреции белка с мочой регистрировались при неконтролируемой АГ [2]. В исследовании DIABHYCAR (2003) достоверно продемонстрировано, чти выявление МАУ ассоциировано с высоким риском развития сердечной недостаточности [13]. В исследовании MICROHOPE (Microalbuminuria, Cardiovascular and Renal Outcomes Heart Outcomes Prevention Evaluation) пациенты с исходной микроальбуминурией имели достоверно выше риск больших кардиоваскулярных проявлений, общей смертности и госпитализаций, связанных с сердечной недостаточностью по сравнению с больными, не имевшими исходно МАУ, причем независимо от наличия сахарного диабета [4].
По данным исследования Johan Arnlov и соавт.(2005) микроальбуминурия увеличивает риск сердечно-сосудистых заболеваний и сердечно-сосудистой смертности более, чем в 3 раза [1]. Результаты исследования PREVEND (Prevention of Renal and Vascular Endstage Disease) дали убедительные доказательства того, что МАУ – мощный предиктор сердечно-сосудистой смертности в популяции, независимо от других факторов риска [3].
Любопытно, что взаимосвязь между микроальбуминурией и сердечно-сосудистой заболеваемостью удавалось обнаружить даже при очень низких показателях экскреции белка с мочой. Так, в исследовании Copenhagen City Heart-3 риск ишемической болезни сердца и сердечно-сосудистой смерти повышался (причем независимо от наличия АГ, СД и патологии почек) уже при уровне альбуминурии > 4.8 мкг/мин, что значительно меньше общепринятого нижнего порога для диагносцирования микроальбуминурии (20 мкг/мин) [7]. Многочисленные экспериментальные, клинические и эпидемиологические исследования указывают на то, что микроальбуминурия является одним из важнейших независимых факторов риска сердечно-сосудистых и цереброваскулярных событий, также смерти от них.
Материалы и методы. Под МАУ понимают уровень экскреции альбумина с мочoй от 30 до 300 мг/сут (или от 20 до 200 мкг/мин). В европейских странах для определения потерь белка с мочoй нередко используют величину отношения альбумин/креатинин в моче – на микроальбуминурию соответственно указывают цифры 2,5 – 30 мг/ммоль у мужчин и 3,5 – 30 мг/ммоль у женщин [6]. Определение экскреции альбумина с мочой проводится в утренней или суточной порции мочи. Уровень альбуминурии имеет высокую вариабельность - до 30%, на которую влияют: физическая активность, лихорадка, а также сопутствующая патология: неконтролируемая гипертензия и гипергликемия, сердечная недостаточность. Уровни альбуминурии, расцениваемые как микроальбуминурия, используются для диагностики состояния всех категорий больных и здоровых лиц.
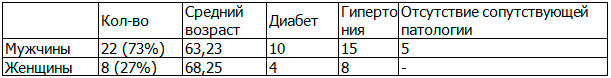
В исследовании принимало участие 30 больных (22 мужчин и 8 женщин), находящихся на стационарном лечении в отделении кардиопульмонологии МЦ “Эребуни” по поводу сердечной недостаточности (III – IV класс по New York Heart Association (NYHA)) (табл. 1). Средний возраст пациентов составил 66,5 лет. Сахарный диабет отмечался у 14 больных (46,7%), артериальная гипертензия у 23 пациентов (76,7%). У 5 больных (16.7%) не было ни сахарного диабета, ни артериальной гипертензии.
Таблица 1. Распределение больных по полу, возрасту и сопутствующим патологиям
Обследование включало электрокардиографию (ЭКГ), эхокардиографию (ЭхоКГ), биохимический анализ крови и определение микроальбуминурии в утренней моче (в мкг/мин). Определение уровня альбуминурии производился турбодиметрическин методом на биохимическом анализаторе “HITACI cobaс c 311” (Roche) с использованием диагностических наборов Tina-Qant.
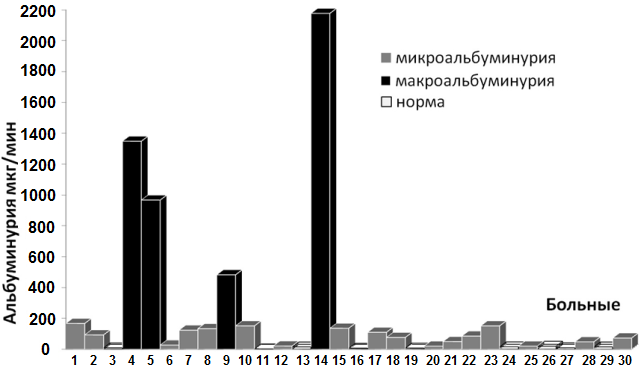
Рис 1. Уровень альбумина в моче пациентов
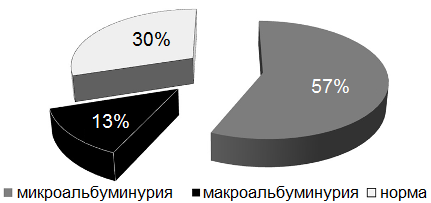
Рис. 2. Процентное соотношение больных с различным уровнем альбумина в моче
Результаты исследований. Количество больных с микроальбуминурией составило 17 человек (57%). У 9 больных уровень альбумина в моче не превышал уровень 20 мкг/мин - норма (30%). 4 пациента имели макроальбуминурию - уровень выше 200 мкг/мин (13%) (рис. 1-2). Повторная госпитализация наблюдалась у 8 больных с микроальбуминурией и у 1 больного с макроальбуминурией. Летальный исход зарегистрирован у 1 пациента с микроальбуминурией и у 2 пациентов с макроальбуминурией.
Обсуждение. Таким образом, проведенные исследования еще раз подтвердили, что пациенты с исходной МАУ имели более высокий риск общей смертности, повторных госпитализаций, связанных с сердечной недостаточностью, чем пациенты без МАУ. На основании этих данных можно заключить, что МАУ является ранним доклиническим признаком эндотелиальной дисфункции сосудов и достоверным маркером высокого сердечно-сосудистого риска.
