Реализация выбора эффективного медикаментозного лечения больных артериальной гипертензией (АГ) существенным образом зависит от адекватности, как самой прогностической модели, так и процедур ее использования реальному процессу лечения и роли врача в этом процессе [1-3]. В большинстве случаев для этих целей с использованием методов статистической обработки данных строится регрессионная модель. Однако, адекватность этой модели подтверждается только на той выборке ретроспективной информации, на которой она построена, затруднена ее коррекция по текущей информации [4-6]. В тех случаях, когда основное назначение модели имитировать выходные показатели процесса при заданных параметрах, более эффективной считается нейросетевая модель [7].
Структурная схема модель-ориентированного подхода к выбору антигипертензивной терапии приведена на рис.1.
Для построения нейросетевой модели [7] использованы статистические данные наблюдения больных АГ в отделении кардиологии клиники Саратовского государственного медицинского университета.
Количество наблюдений выборки – 71, в контрольной – 14.
Для построения нейросетевой модели используется пакет STATISTICA. Модуль NeuralNetworks системы STATISTICA включает в себя процедуру, организующую поиск нужной конфигурации сети. Эта процедура заключается в построении и тестировании большого количества сетей с разными архитектурами и последующем выборе из них той сети, которая лучше всего подходит для решения поставленной задачи прогнозирования.
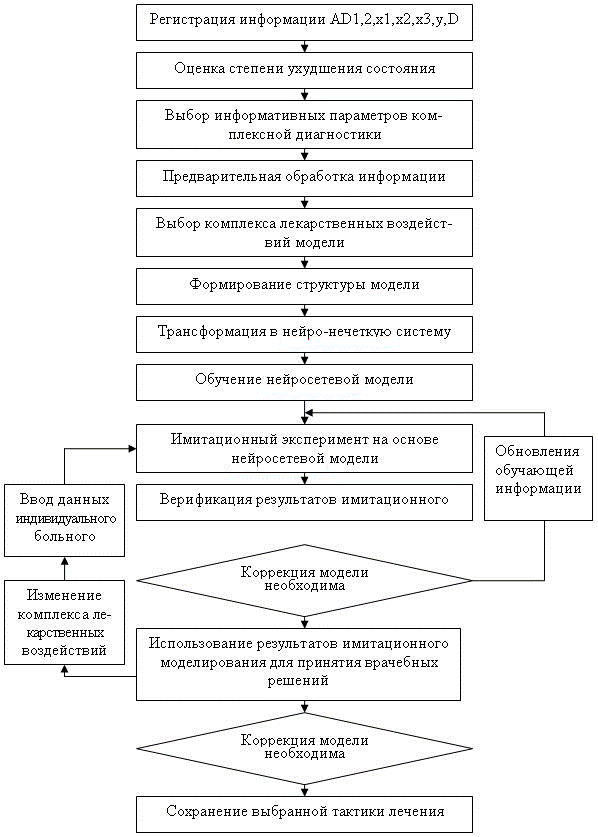
Рис. 1. Структурная схема модель-ориентированного подхода к выбору антигипертензивной терапии.
Для окончательного выбора единственной наилучшей сети сравним эти сети по значениям различных ошибок.
После выделения какой-либо сети в списке и нажатия кнопки Descriptive statistics появляется окно с характеристиками данной нейросетевой модели (рис. 2). В нем приводятся значения Data Меаn (среднее данных) для каждого прогнозируемого параметра, Data S.D. (среднеквадратическое отклонение данных), Еrror Mean (средняя ошибка прогноза), Еrror S.D. (среднеквадратическое отклонение ошибки прогноза), Аbs E. Mean (средняя абсолютная ошибка прогноза), SD Ratio (отношение среднеквадратического отклонения ошибки прогноза к среднеквадратическому отклонению данных), Сorrelation (величина корреляции между реальными и спрогнозированными данными.)
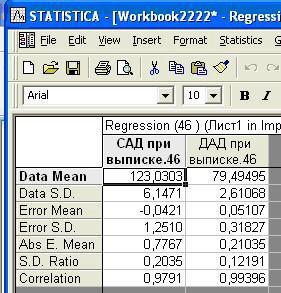
Рис. 2. Таблица ошибок регрессии, построенной выбранной сетью.
Значение ошибки «SD Ratio» является наиболее пригодной для целей сравнения, потому как представляет собой число между 0 и 1, зависит лишь от величины каждой составляющей ошибки (не зависит от знака), а также довольно восприимчиво к выбросам. Эмпирическое правило гласит, что если SD Ratio не превышает значения 0,2, сеть подобрана хорошо, если SD Ratio находится в пределах от 0,2 до 0,4 – то удовлетворительно, а если больше 0,4 – то неудовлетворительно.
В нашем примере лишь одна сеть из 10, сохраненных программой, оказалась близка к хорошему качеству прогнозирования по обоим параметрам (на рис. 2 величина SD Ratio для систолического артериального давления (САД) при выписке равна 0,2035, а для диастолического артериального давления (ДАД) при выписке 0,12191).
Исследуем подробнее выбранную сеть (она имеет номер 46, то есть она в процессе тестирования была сформирована 46-й). Архитектура этой сети проведена на рис. 3. Эта сеть имеет 54 входа, 21 нейрон в первом слое, 2 нейрона во втором слое и 2 выхода.
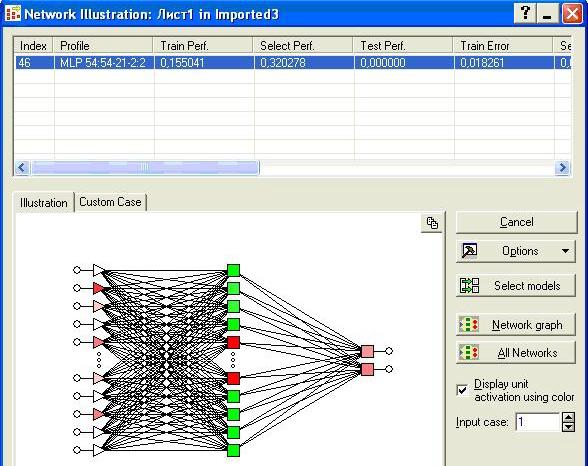
Рис. 3. Архитектура лучшей сети.
При построении этой сети 12 из 66 имеющихся входов были отброшены, как малозначимые. Посмотрим, какую значимость имеют оставшиеся входы.
К 10 значимым входным параметрам из 54 отобранных для данной архитектуры прогнозирования САД и ДАД при выписке, оказались: ТМЖП, прием в стационаре препаратов центрального действия, ФКХСН, прием в стационаре и АПФ/АРА, БКК, кардиалгия на фоне гипертонии лечение до поступления и – АПФ/АРА, сахарный диабет, прием в стационаре диуретиков.
Гистограммы частот остатков для каждого из входов выбранной модели нейронной сети (рис. 4) показывают, с какой частотой встречаются те или иные ошибки при аппроксимации зависимости САД и ДАД при выписке от имеющихся входных параметров. Например, величина ошибки прогнозирования ДАД при выписке не превосходит по модулю 1.4 мм рт. ст. А чаще всего (в 48 случаях из 99 рассмотренных) это давление предсказывается абсолютно точно. Величина ошибки прогнозирования САД при выписке не превосходит по модулю 6 мм рт. ст.(причем 6 мм – это единичный выброс, подавляющая масса предсказаний имеет абсолютную погрешность не более 2 мм рт. столба).
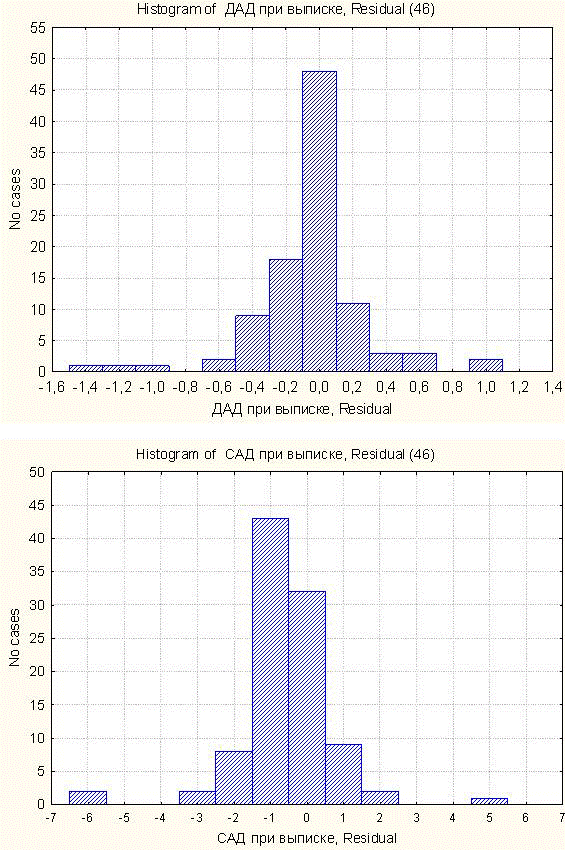
Рис. 4. Гистограммы частот остатков для каждого из входов выбранной модели нейронной сети.
На рис. 5 приводятся графики зависимости предсказанных значений САД и ДАД от наблюдаемых. По этим графикам, например, видно, что наблюдаемое значение ДАД при выписке 70 мм.рт.ст. сеть всегда предсказывает в диапазоне от 70 до 71; наблюдаемое значение ДАД при выписке 80 мм.рт.ст. - в диапазоне от 79 до 82 и т.д.
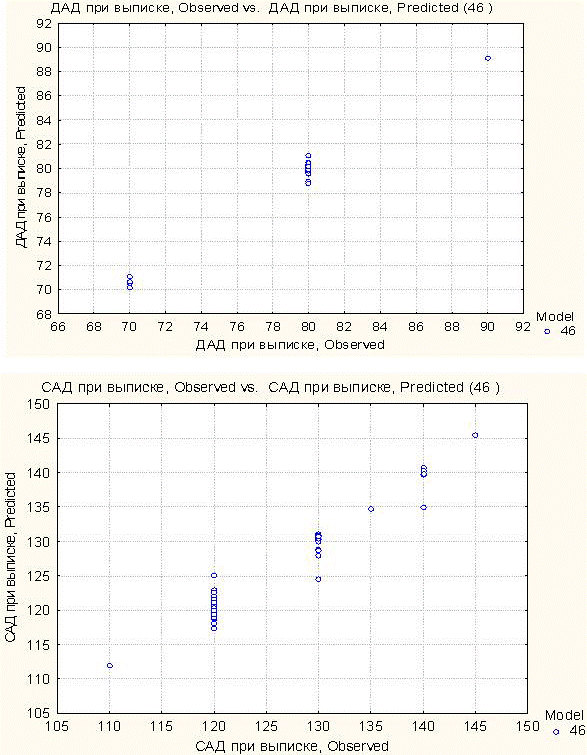
Рис. 5. Зависимость предсказанных (Predicted) значений САД и ДАД от наблюдаемых(Observed).
Проведенный анализ позволяет сделать вывод о том, что качество прогнозирования данной сетью действительно высоко.
Если учитывать значения давления на 3-й день лечения (иначе говоря, прогноз результатов лечения делать только после 3-го дня пребывания в стационаре), то качество прогноза можно еще улучшить.
На рис. 6 приводятся результаты тестирования сетей, которые рассматривали 72 входа.
Как видно из рис. 6, эти сети имеют номера 41, 44, 48, 49, 50 и 51. Правда, ни одна из этих сетей не имеет оба показателя SD Ratio меньшие, чем 0,2. Однако, можно заметить, что сеть с номером 50 хорошо предсказывает САД при выписке (SD Ratio =0,1143), а сеть с номером 51 хорошо предсказывает ДАД при выписке (SD Ratio =0,1171). Из этих двух сетей можно организовать “комитет” [8], и значение прогноза САД при выписке получать у первой сети, а прогноза ДАД при выписке – у второй.
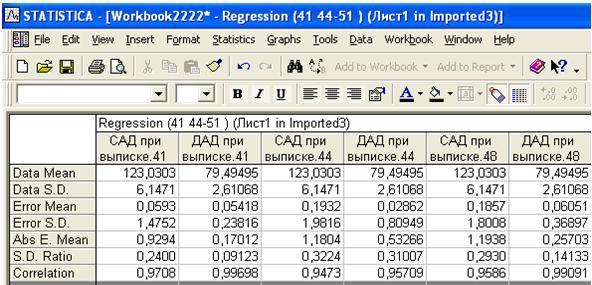
Рис. 6. Таблица ошибок регрессий, построенных сетями, учитывающими значения давления на 3-й день лечения.
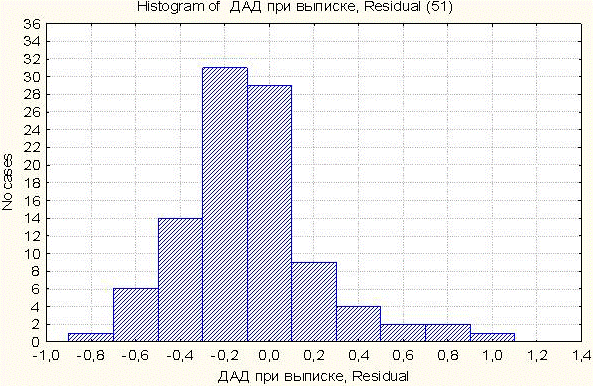
Рис. 7. Гистограммы частот остатков для каждого из входов 50 и 51-й моделей нейронной сети.
Из рис. 7 видно, что в этом случае величина ошибки прогнозирования ДАД при выписке не превзойдет по модулю 1.4 мм рт. ст., а величина ошибки прогнозирования САД при выписке не превзойдет по модулю 5 мм рт. ст. (причем подавляющая масса предсказаний будет иметь абсолютную погрешность не более 1 мм рт. столба).
Отметим, что при анализе значимости входов для 50 и 51 сетей самыми значимыми оказываются САД и ДАД на 3-й день лечения.
Рассмотренные нейросетевые модели позволяют прогнозировать значения САД и ДАД при выписке в случае назначения врачом комбинации лекарственных средств. В ряде случаев врачу важно иметь прогностическую оценку влияния отдельного лекарственного воздействия на АД. Для построения нейросетевых моделей этого класса предварительно осуществлена кластеризация обучающей выборки методов k-средних на 3 класса. В рамках наблюдений, попавших в кластер 1, определены нейросетевые структуры для каждой группы лекарственных воздействий с ошибкой, не превышающей 0,2 (табл. 1).
Построенные нейросетевые модели предлагается использовать в качестве интеллектуальной поддержки врача при выборе лечения в стационаре на основе САД и ДАД при выписке [9]. Алгоритм выбора включает следующие шаги:
1) в системе STATISTICA вносятся исходные данные больного, поступившего на стационарное лечение;
2) столбцы «прием в стационаре» заполняются врачом в зависимости от выбранного лечения;
3) для предварительной оценки влияния на САД и ДАД при выписке отдельной группы лекарственных воздействий прогнозирование осуществляется с использованием нейросетевых моделей, приведенных в таблице;
4) предварительный анализ предложенного варианта комплексного лекарственного воздействия;
5) прогнозирование значение САД и ДАД при выписке для предложенного воздействия;
6) если врач не удовлетворен прогностической оценкой, то переход к новому варианту комплексного лекарственного воздействия и прогнозированию САД и ДАД при выписке, в противном случае – принятие решения о назначении лечения;
7) внесение в исходные данные значений САД и ДАД на 3-й день лечения;
8) прогнозирование значений САД и ДАД при выписке для дополнительных исходных данных;
9) если врач не удовлетворен прогностической оценкой, то он корректирует лечение и рассматривает новую прогностическую оценку, в противном случае – назначенное лечение не меняется.
Таблица 1. Значение отношения среднеквадратичного отклонения ошибки прогноза к среднеквадратичному отклонению данных для нейросетевого моделирования приема в стационаре отдельных групп препаратов

Модель-ориентированный подход на основе нейросетевой обработки архивных данных стационарного лечения больных АГ является эффективным инструментом в работе врача при анализе наиболее значимых факторов, влияющих на состояние поступившего в стационар пациента, и подбора оптимального варианта антигипертензивной терапии наиболее щадящим способом со снижением риска осложнений и обострений, которые возникают на начальном этапе при традиционном лечении.
