Введение. Чрезвычайно актуальным вопросом является своевременная оценка состояния больного инфарктом миокарда (ИМ) и определения степени риска тяжелых осложнений и летального исхода [1-3]. Своевременное выявление степени риска может способствовать активному вмешательству в течение болезни [1, 4]. Разработаны различные прогностические шкалы, модели и отдельные критерии. Значительное большинство из них основано только на клинических и лабораторных данных и не учитывает влияния на прогноз электрической нестабильности миокарда (ЭНМ), параметры которой чрезвычайно важны для этой категории больных [5]. Данные различных авторов относительно прогностической информативности отдельных показателей ЭНМ неоднозначны, а иногда и противоречивы и чаще относятся к отдаленному прогнозу, чем к ближайшему. Рационального комплекса параметров ЭНМ для своевременного выделения групп повышенного риска не существует.
Включение отдельных параметров ЭНМ в комплексные методы прогнозирования ИМ, основанные на клинических, лабораторных и инструментальных данных [6-10], требуют большей частью использования медицинских компьютерных технологий, статистических вычислительных программ, много времени и оборудования и не могут осуществить своевременной стратификации риска.
Цель исследования: установить у больных острым инфарктом миокарда (ОИМ) прогностическую информативность различных показателей ЭНМ в первые два дня заболевания для оценки степени риска осложненного течения госпитального этапа и развития конкретных осложнений.
Материал и методы.
Статистическая обработка данных проводилась на персональном компьютере с использованием программы STATISTICA 10.0 в соответствии с принятыми методиками [18, 19].
В исследование включено 98 мужчин в возрасте до 70 лет (пределы колебаний 37-68 лет, средний возраст 54±7 лет) с первичным и повторным Q-ИМ с подъемом сегмента ST электрокардиограммы (ЭКГ). Почти у половины больных (48 из 98 - 49%) был задний инфаркт миокарда, несколько реже передний (42 больных - 43%) и статистически значимо в меньшей доле (p<0,001) - циркулярный (8 больных - 8%). Критериями исключения из исследования были сопутствующие тяжелые заболевания и состояния, которые могут существенно повлиять на течение и прогноз инфаркта миокарда. Тромболитическая терапия (ТЛТ) была проведена 55 больным (56%), у остальных тромболизис не применялся в связи с поздней госпитализацией или наличием противопоказаний. Всем больным проводилась стандартная однотипная терапия ИМ и стандартное клиническое и лабораторно-инструментальное исследование. При развитии осложнений осуществлялось их лечение.
Специальное исследование для оценки ЭНМ заключалось в трехкратном (в 1-2 сутки, на 7 сутки и перед выпиской из стационара) холтеровском мониторировании электрокардиографии высокого разрешения (ХМ ЭКГ ВР) в 12 общепринятых отведениях с частотой оцифровки сигнала 514 Гц с использованием прибора Комплекс Полифункциональный Холтер-монитор «Кардиотехника-04-АД-3(М)» фирмы «Инкарт» СПб. При мониторировании регистрировались следующие показатели ЭНМ: поздние потенциалы желудочков (ППЖ), циркадный индекс (ЦИ) частоты сердечных сокращений (ЧСС), вариабельность и турбулентность ритма сердца (ВРС и ТРС), длина и дисперсия корригированого интервала QT (QTc), которые оценивались в автоматическом режиме с обязательной врачебной коррекцией и интерпретацией. Клиническое проявление электрической нестабильности - аритмическая активность миокарда - определялась по максимально значимой градации нарушений ритма.
Мы включали в осложнения госпитального этапа нарушения ритма, зафиксированные с третьих суток до выписки из стационара по результатам ЭКГ покоя и второго (на седьмые сутки) и третьего (перед выпиской) ХМ ЭКГ ВР, и учитывали опасные желудочковые экстрасистолы (ЖЭ) и пароксизмы желудочковых и наджелудочковых тахикардий, а в трех случаях фибрилляции предсердий. При этом опасными ЖЭ мы считали все ЖЭ, начиная со II градации по классификации B. Lown и M. Wolf в модификации M. Ryan, и опасные ЖЭ I градации, возникающие более 10 в час [11] и длящиеся более трети суток [12]. По такому же принципу все опасные ЖЭ разделялись на частые (более 10 в час и длительнее 8 часов) и редкие.
Анализ ППЖ осуществлялся в общепринятых псевдоортогональных отведениях I, aVF, V2. Количественные критерии ППЖ вычислялись по трем принятым показателям: 1. продолжительность фильтрованного комплекса QRS (Tot QRS) в мс; 2. продолжительность низкоамплитудных сигналов на уровне 40 мкВ в конце комплекса QRS (LAS40) в мс; 3. среднеквадратичная амплитуда последних 40 мс фильтрованного сигнала QRS (RMS40) в мкВ. Параметры, разграничивающие признаки ППЖ от области нормальных значений ЭКГ ВР при использовании частотного фильтра 40 Гц: 1. Tot QRS>114 мс; 2. LAS40>38 мс; 3. RMS40<20 мкВ. Наличие двух или трех этих показателей свидетельствует о наличии ППЖ [13].
ЦИ ЧСС является проявлением вариабельности ритма сердца (ВРС) и отражает циркадную его изменчивость. Он рассчитывается как отношение среднедневной ЧСС к средненочной и имеет нормальное значение 1,24-1,44 [14].
Вегетативный контроль сердца заключается в суммации тормозного влияния парасимпатикуса и ускоряющего действия симпатической нервной системы. Основная оценка ВРС заключается в констатации её повышения при активации парасимпатикуса или снижения при повышении симпатического тонуса [14]. Вегетативные влияния на сердце были оценены путем изучения двух основных временных характеристик ВРС: 1. SDNN (мс) - стандартное отклонение от средней длительности всех синусовых интервалов RR, значение которого является интегральным показателем, характеризующим ВРС в целом, и зависит от воздействия как симпатического, так и парасимпатического отдела вегетативной нервной системы (ВНС); 2. pNN50 (%) - доля соседних синусовых интервалов RR, различающихся более чем на 50 мс - свидетельствует о тонусе парасимпатического отдела ВНС. Уменьшение SDNN ниже 100 мс считалось показателем повышения симпатических влияний на синусовый узел, а снижение pNN50 ниже 2% свидетельствовало о снижении защитного эффекта парасимпатической нервной системы [15]. Обязательно учитывалась также динамика этих параметров на протяжении госпитального периода.
ТРС оценивается двумя независимыми показателями: ТО (начало турбулентности), характеризующий изменения синусового ритма сразу после ЖЭ, т.е. период учащения ритма, и TS (наклон турбулентности), отражающий темп последующего урежения ритма в пределах 20 постэкстрасистолических интервалов [16]. Установлено, что ТО≥0% и TS≤2,5 мс/RR являются показателями патологии.
Продолжительность интервала QT зависит от ЧСС и пола пациента, поэтому для получения должного его значения используется QTc, который рассчитывается по модифицированной формуле H. Bazett. Кроме длины учитывается степень вариабельности интервала QTc, количественной характеристикой которой является дисперсия QTc (dQTc), т.е. разность максимального и минимального значения интервала QT в 12 отведениях не менее чем в трех последовательных циклах [17]. Данные литературы о прогностической значимости QTc и dQTc крайне противоречивы, а нормальные значения их показателей оцениваются неоднозначно. Согласно большинству литературных данных, мы считали интервал QTc у мужчин удлиненным при продолжительности более 450 мс. Насчет границы нормы для dQTc единого мнения нет, пределы ее колебания преимущественно 50-80 мс. Мы учитывали удлинение дисперсии при ее значении более 80 мс.
Для описания распределения качественных характеристик анализировались относительные величины и статистическая значимость различий оценивалась при помощи определения критерия соответствия χ2. При анализе количественных признаков во всех случаях распределение отличалось от нормального, ввиду чего количественные данные описывались при помощи медианы и квартилей в формате Me (Q25-Q75); оценка статистической значимости различий между группами по количественным признакам проводилась при помощи непараметрических методов: расчета и оценки критерия Мана-Уитни, рангового дисперсионного анализа Краскела-Уоллиса. Пороговый уровень статистической значимости установлен при р=0,05.
При помощи методов описательной статистики отбирались предикторы для моделирования течения госпитального периода ОИМ по результатам I ХМ. Были использованы методы моделирования: построение деревьев классификации, логистический регрессионный анализ. В качестве альтернативной модели использовался метод последовательной статистической диагностической процедуры.
Результаты. Осложнения госпитального этапа оценивались по клиническим и инструментальным (ЭКГ покоя и двукратное ХМ ЭКГ ВР) данным, зафиксированным на протяжении c третьих суток ОИМ до выписки из стационара. Инструментальные данные учитывались по результатам 2-го (на 7 сутки) и 3-го (перед выпиской) мониторирования. Были выявлены три группы осложнений: ассоциированные с ЭНМ - нарушения ритма и атриовентрикулярной проводимости (АВ-проводимости), ранняя постинфарктная стенокардия (РПИС), рецидивирующий ИМ (рИМ), внезапная сердечная смерть (ВСС); связанные с сократительной его недостаточностью - левожелудочковая недостаточность (ЛЖН) 2-3 класса по Killip и кардиогенный шок (КШ), правожелудочковая недостаточность (ПЖН) и с механической несостоятельностью - аневризма левого желудочка (ЛЖ). Нарушения ритма включали опасные ЖЭ и пароксизмы желудочковых и наджелудочковых тахикардий и фибрилляции предсердий.
Подавляющее количество осложнений относилось к группе, связанной с ЭНМ, и чаще всего проявлялось опасными ЖЭ (частыми в 41,8% и редкими в 39,8%). Остальные осложнения встречались относительно редко, несколько чаще других ЛЖН, в основном 2-3 класса по Killip (32,6%) и в 6 случаях КШ (4 класс по Killip), а также пароксизмальные нарушения ритма (32,6%), нарушения АВ-проводимости (27,5%) и РПИС (24,5%). Нарушения ритма и проводимости у части больных регистрировались только на одном мониторе, а у некоторых и на 2-ом, и на 3-ем. Изучение осложнений у каждого больного позволило разделить больных на три группы. Первую группу составили шесть больных с неосложненным течением госпитального периода (6,1%). Большинство вошло во вторую группу - осложненного течения с благоприятным исходом госпитального этапа (86 больных - 87,7%); 6 больных третьей группы (6,1%) имели осложненное течение с неблагоприятным исходом на госпитальном этапе, под которым понимается острое сердечно-сосудистое событие, являющееся конечной точкой данного исследования, - у 5 больных рИМ и у одного больного летальный исход (ВСС). Почти у всех больных 2 группы (85 из 86 - 98,6%) имели место нарушения ритма, из них у 80 - опасные ЖЭ, (частые у 41 и редкие у 39); у 5 пациентов выявлялись только пароксизмы наджелудочковых тахикардий и у одного - нарушение АВ-проводимости на фоне неопасных ЖЭ. Все остальные осложнения возникали на фоне нарушения ритма.
Статистически значимой связи течения госпитального периода с возрастом больных не установлено: средний возраст пациентов с неосложненным течением составил 56 (51 - 57) лет; при осложненном течении с благоприятным исходом - 54 (50 - 59) года; при осложненном течении с неблагоприятным исходом - 53 (47 - 53) года (p=0,3). Связи отдельных осложнений с возрастом у больных второй группы также не выявлено (табл. 1).
Таблица 1. Связь осложнений госпитального периода с возрастом
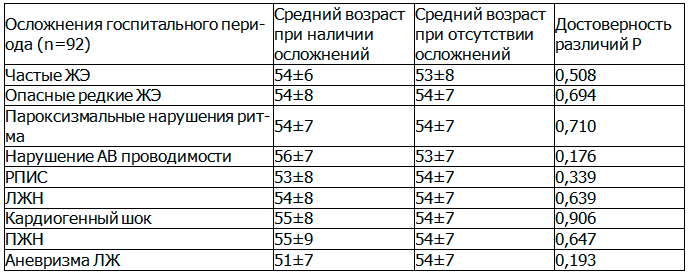
Статистически значимых различий течения госпитального периода от локализации ИМ и от проведения тромболитической терапии не установлено.
ЭНМ в остром периоде (на 1 мониторе) наиболее часто проявлялась удлинением dQTc (96%), уменьшением ЦИ ЧСС (95%), снижением SDNN (70%) и удлинением QTc (66%); около половины больных имели снижение pNN50 (47,5%); остальные показатели отмечались сравнительно редко: возникновение ППЖ у 31%, патологического значения TO - у 17%, TS - у 16%.
Аритмическая активность миокарда (выступающая в ипостаси как осложнения, так и показателя ЭНМ) проявилась на этом мониторе опасными ЖЭ, которые были выявлены у 81 пациента (у 44 частые и 37 опасные редкие), и пароксизмами желудочковых и наджелудочковых тахикардий - у 51 (частые у 18, редкие у 33); у 11 (5 пациентов 1-ой группы и 6 - второй) опасных нарушений ритма не отмечалось.
Для оценки возможности прогнозирования в первые два дня дальнейшего течения госпитального периода было проведено сравнение основных показателей первого монитора ЭКГ ВР у 3-х групп больных с разным течением и исходом госпитального периода.
В таблице 2 представлен свод переменных, полученных в результате проведения первого мониторирования, по которым имелись статистически значимые различия при различных вариантах течения госпитального периода. Данные переменные могут быть использованы в качестве предикторов течения госпитального этапа ИМ.
Таблица 2. Переменные первого мониторирования, имевшие статистически значимые различия при разных вариантах течения госпитального периода
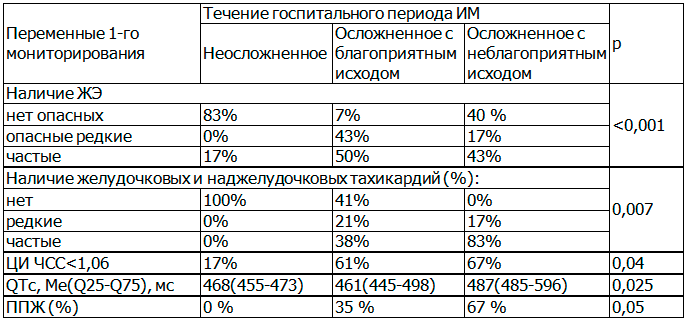
Большинство параметров ЭНМ являются также предикторами конкретных осложнений госпитального этапа.
Обсуждение. Полученные результаты свидетельствуют, что при неосложненном течении госпитального периода (первая группа) у подавляющего большинства больных (5 из 6 - 83%) не было опасных ЖЭ в остром периоде, но у одного (17%) зафиксированы даже частые ЖЭ. При осложненном течении с благоприятным исходом (вторая группа) опасные ЖЭ не выявлялись у 7% (6 пациентов из 86), а при неблагоприятном исходе (третья группа) опасные ЖЭ отмечались у всех 6-ти пациентов, причем у подавляющего большинства (5 пациентов - 83%) они были частыми, между тем как у пациентов второй группы частые ЖЭ регистрировались только у половины (43 из 86 - 50%).
Различия в частоте выявления опасных ЖЭ на первом мониторе у больных с разным течением и исходом госпитального периода статистически высоко достоверны (p<0,001).
Достоверные различия между группами имели место и по частоте пароксизмов желудочковых и наджелудочковых тахикардий на первом мониторе. У пациентов первой группы эти пароксизмы не выявлялись, у второй группы они имели место в 59% случаев и у третий группы у всех шести пациентов.
У обследованных пациентов были низкие значения ЦИ ЧСС. Межгрупповых статистически значимых различий не установлено, хотя имелась некоторая тенденция к снижению значений ЦИ от неосложненного течения к осложненному с благоприятным исходом и к осложненному с неблагоприятным исходом (1,09 (1,06-1,10), 1,05 (0,98-1,07) и 1,02 (0,90-1,06) соответственно). Значения ЦИ<1,06 статистически значимо чаще встречались в группах с осложненным течением (p=0,04). Так, в группе с неосложненным течением доля больных со значениями ЦИ ЧСС<1,06 составляла 17%, в группе с осложненным течением с благоприятным исходом - 61% и в группе с неблагоприятным исходом - 67%. Таким образом, можно предположить, что значение ЦИ ЧСС<1,06 увеличивает риск осложнений, а ЦИ<0,98 - риск неблагоприятного исхода.
По параметру интервала QTc на первом мониторе медианный тест установил статистически значимые различия (p=0,025) между группами, в том числе между обеими группами с осложненным течением с благоприятным и неблагоприятным исходом (p=0,019). Средние значения QTc составили 468 мс (455-473) при благоприятном течении, 461 мс (445-498) при осложненном течении с благоприятным исходом и 487 мс (485-596) с неблагоприятным. Таким образом, можно полагать, что при удлинении QTc>473мс увеличивается риск осложненного течения, а выше 498 мс - риск неблагоприятного исхода на госпитальном этапе.
По дисперсии интервала QTc значимых различий не выявлено. Средние значения составили при неосложненном течении 116 мс (115-119), при осложненном с благоприятным исходом 112 мс (95-140) и при осложненном течении с неблагоприятным исходом – 97 мс (83-222). Однако можно предположить, что удлинение dQTc>119 мс увеличивает риск осложнений госпитального периода, а свыше 140 мс - риск неблагоприятного исхода.
Приведенные результаты соответствуют некоторым литературным данным относительно информативности увеличения dQTc для ближайшего прогноза ИМ [9, 20].
Для разработки предикторов отдельных осложнений госпитального этапа было проведено сопоставление частоты развития каждого осложнения с показателями ЭНМ по первому мониторированию ЭКГ ВР.
Частые ЖЭ осложняли госпитальный период почти в два раза чаще при патологическом значении TS в остром периоде, чем при нормальном его значении (84,6% против 43,4%; p=0,005), что позволяет прогнозировать высокий риск этого осложнения по патологическому значению TS на первом мониторе.
Пароксизмальные нарушения ритма, являющиеся осложнением госпитального периода у 32 пациентов, значительно чаще возникали на госпитальном этапе у больных, имеющих подобные нарушения в остром периоде: частые выявлялись в 36% против 13%, а редкие - в 50% против 30% (p=0,00045). Пароксизмы на госпитальном этапе возникали также значительно чаще у больных с нарушениями АВ-проводимости на первом мониторе, чем у пациентов без этого нарушения (25% против 8%; p=0,026), и у больных с удлинением интервала QTc (41,3% против 17,8%; p=0,034). Таким образом, в первые два дня ИМ можно прогнозировать повышенный риск возникновения на госпитальном этапе пароксизмальных нарушений ритма по наличию на первом мониторе пароксизмальных желудочковых и наджелудочковых тахикардий, по нарушению АВ-проводимости и удлинению интервала QTc. При совпадении нескольких признаков прогностическая информативность их повышается.
Среди больных, имевших нарушение АВ-проводимости на госпитальном этапе, почти у половины (44% случаев) это нарушение имело место и на первом мониторе, но ни в одном случае оно не было выявлено только в остром периоде с дальнейшей нормализацией на госпитальном этапе. Кроме того, это осложнение госпитального периода ассоциировалось с патологическим значением TS на первом мониторе: АВ-проводимость была нарушена в госпитальном периоде у 69,2% больных, имевших патологическое значение TS в остром периоде, и у 28% с нормальным значением TS на первом мониторе (p=0,004). Следовательно, риск нарушения АВ-проводимости на госпитальном этапе повышается при наличии в остром периоде этого нарушения проводимости и патологического значения TS.
Возникновение РПИС ассоциируется с двумя показателями острого периода. Это осложнение возникло у 40% (24 из 60) пациентов с сниженным SDNN на первом мониторе, но ни разу не отмечено при нормальной активности симпатической нервной системы у 26 больных (p=0,05). Кроме того, РПИС имела место у 12 больных из 29 с наличием ППЖ на первом мониторе и у 12 больных из 57 при отсутствии ППЖ (41,4% против 21%; p=0,05). Различия по обоим показателям почти достигли достоверности, что позволяет прогнозировать в первые двое суток высокий риск РПИС по повышению активности симпатической нервной системы и наличию ППЖ.
ЛЖН 2-3 класса по Killip имела связь с рядом показателей первого монитора. Недостаточность левого желудочка чаще развивалась при наличии в остром периоде частых ЖЭ (66% против 38%; p=0,04) и частых желудочковых и наджелудочковых тахикардиий (34% против 12%; p=0,02). Установлена связь между наличием ЛЖН в госпитальном периоде и значениями ЦИ ЧСС на первом мониторе. Среднее значение ЦИ при наличии ЛЖН было более низким - 1,01 (0,96-1,06), чем при отсутствии данного осложнения 1,06 - (1,02-1,08), p=0,0033. Кроме того, ЛЖН чаще возникала на госпитальном этапе у больных, имеющих в остром периоде патологические значения TO (71,4% против 29,8%; p=0,004) и TS (84,6% против 28%; p<0,001) и сниженный показатель SDNN (48,4% против 11,5%; p=0,002).
Все указанные статистически значимые переменные включены в модель прогноза ЛЖН по результатом первого мониторирования: частые ЖЭ, частые пароксизмы желудочковых и наджелудочковых тахикардий, ЦИ ЧСС ниже 1,02, патологические значения TO и TS, сниженный показатель SDNN.
Остальные (редкие) осложнения госпитального этапа также ассоциировались с несколькими показателями первого мониторирования, но их связь желательно уточнить на большей когорте больных.
Таким образом, на основании анализа результатов мониторирования ЭКГ ВР в первые два дня ИМ у больных с разными осложнениями госпитального этапа определены предикторы повышенного риска осложненного течения и отдельных осложнений. Разработана таблица вероятных предикторов всех изученных осложнений госпитального этапа.
Вывод. Параметры ЭНМ позволяют в первые два дня ИМ выявить группу больных повышенного риска осложненного течения госпитального этапа и развития конкретных осложнений, что предопределяет возможность адекватного лечения каждого больного.
