Цель исследования. Анализ непосредственных результатов операций геометрической реконструкции левого желудочка (ЛЖ), реваскуляризации миокарда и коррекции митральной недостаточности.
Клинический материал и методы исследования. Были подвергнуты анализу данные исследования 85 пациентов с постинфарктной аневризмой левого желудочка, c сопутствующей митральной недостаточностью той или иной степени, от 2 до 4 ст., обследованных и прооперированных в Научном Центре cердечно-cосудистой хирургии (НЦССХ) им. А.Н. Бакулева РАМН в период с 1998 по 2010 г.
Было выделено 4 группы пациентов, в зависимости от вида выполненной коррекции митральной недостаточности при реконструктивных операциях на ЛЖ у больных с постинфарктной аневризмой левого желудочка (ПАЛЖ).
В группе обследованных больных было 75 (88,2%) мужчин в возрасте от 49 до 68 лет и 10 (11,8%) женщина в возрасте от 44 до 58 лет. Средний возраст больных составил в среднем 56±12 лет. Диагноз постинфарктная аневризма ЛЖ в сочетании с ишемической митральной регургитацией был установлен на основании клинической картины заболевания, анамнеза и данных клинико-инструментальных методов исследования.
- Группа пациентов, в количестве 12 человек, которым выполнена геометрической реконструкции ЛЖ в сочетании с реваскуляризацией миокарда и протезирование митрального клапана (МК).
- Группа пациентов, в количестве 15 человек, которым выполнена геометрической реконструкции ЛЖ в сочетании с реваскуляризацией миокарда и редукцией межпапиллярного пространства.
- Группа пациентов, в количестве 33 человек, которым выполнена операция геометрической реконструкции ЛЖ в сочетании с реваскуляризацией и пластикой МК край-в-край по Алфиери.
- Группа пациентов, в количестве 25 человек, которым выполнена геометрической реконструкции ЛЖ в сочетании с реваскуляризацией миокарда и пластикой МК на опорном кольце.
Всем больным проводилось общеклиническое обследование, электрокардиография с прекардиальным картированием, суточное Холтеровское мониторирование ЭКГ, эхокардиография, стресс-эхокардиография, коронарография и вентрикулография.
Всем пациентам была выполнена операция - реваскуляризация миокарда с реконструкцией ЛЖ по методике Бокерия - Дора и устранение митральной регургитации (протезирование и реконструкция МК) в условиях искусственного кровообращения и фармакохолодовой кардиоплегии раствором «кустодиол». Реконструкция МК проводилась трансвентрикулярным доступом. В зависимости от механизма возникновения регургитации на митральном клапане использовались несколько способов пластики. В нашем случае это редукция межпапиллярного пространства, аннулопластика по методу Алфиери, а так же имплантация опорного кольца Карпантье в митральную позицию, которую впервые в мире выполнена в НЦССХ им. А.Н.Бакулева академиком РАМН Л.А. Бокерия.
Результаты исследования. На операционном столе умерло 2 пациента, обеим была выполнена операция реваскуляризация миокарда, реконструкция ЛЖ и протезирование МК.
Повторные вмешательства на митральном клапане потребовалось 1 пациенту в 1 группе, 1 в 3 группе и 2 в 4 группе. Причиной вмешательства стало прорезывание швов с образованием сброса крови обратно в левое предсердие.
Время искусственного кровообращения в сравниваемых группах достоверно не различалось и составило соответственно 180±127 в 1 группе, 132±64 во 2 группе, 157±85 в 3 группе и 162±93 мин. в 4 группе.
Время аноксической остановки сердца в оперированных группах составило; в 1 группе 123±42, во 2 группе 89±30, в 3 группе 103±38 и в 4 группе 117±42 мин.
Эти данные указывают на однородность изучаемых групп по клинико-гемодинамическим параметрам и тяжести поражения коронарного русла.
Вспомогательная параллельная перфузия аппаратом искусственного кровообращения более 60 мин потребовалась 3 больным в 1 группе, 4 пациентам в 3 группе и 3 в 4 группе.
Метод вспомогательного кровообращения в виде внутриаортальной баллонной контрпульсации в послеоперационном периоде наблюдения потребовалась 3 больным в 1 группе, 4 во 2 группе, 6 в 3 группе и 5 в 4 группе.
Длительная кардиотоническая поддержка и искусственная вентиляция более 5 суток потребовалась в 1 группе 4 больным, во 2 группе 3, в 3 группе 3 и в 4 группе 3.
Среднее количество реваскуляризированных артерий в 1 группе составило 2,2±1,8, во 2 группе 2,4±1,6 (Р>0,05); в 3 группе 2,5±1,5 и в 4 группе 2,3±1,7.
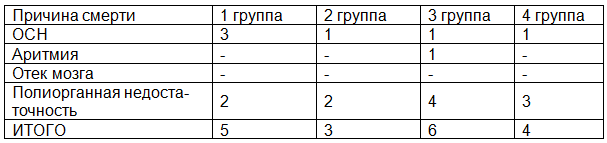
Госпитальная летальность оперированных больных составила: в I группе 5 (41%), во 2 группе 3 (20%), в 3 группе 6 (18,1%) и в 4 группе 4 (16%). Причины смерти были острая сердечная недостаточность, нарушения ритма, отек мозга и полиорганная недостаточность.
Причины послеоперационной летальности представлены в табл. 1.
Таблица 1. Характеристика причин послеоперационной летальности
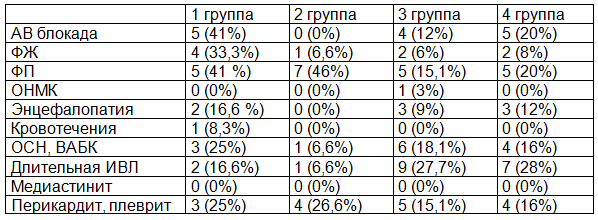
Осложнения в послеоперационном периоде так же не имели достоверные различия в группах по сердечной недостаточности и нарушениям ритма. Послеоперационные осложнения представлены табл. 2. Пациенты характеризовались тяжелым течением раннего послеоперационного периода, что проявлялось развитием сердечной недостаточности, требовавшей постановки внутриаортальной баллонной контрапульсации, развитием фибрилляции предсердий и желудочков, нарушение мозгового кровообращения у одного пациента. Часто послеоперационный период осложнялся развитием перикардита, плеврита и нарушениями со стороны ЦНС (энцефалопатия, гипоксия).
Таблица 2. Характеристика осложнений в раннем послеоперационном периоде
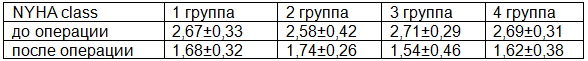
Положительный клинический эффект операции отмечен у большинства прооперированных больных. Сравнительные до и послеоперационные данные сердечной недостаточности по NYHA представлены в табл. 3. Класс сердечной недостаточности снизился с 2,67 до 1,68 в 1 группе, с 2,58 до 1,74 во 2 группе, с 2,71 до 1,54 в 3 группе и с 2,69 до 1,62 в 4 группе пациентов.
Таблица 3. Сердечная недостаточность по NYHA до и после операции по группам
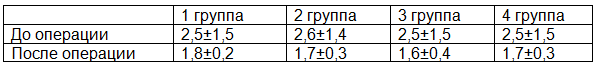
Распределение больных по функциональному классу стенокардии до и после операции представлено в табл. 4. Класс стенокардии снизился с 2,5 до 1,8 в 1 группе, с 2,6 до 1,7 во 2 группе, с 2,5 до 1,6 в 3 группе и с 2,5 до 1,7 в 4 группе пациентов.
Таблица 4. Распределение больных по классу стенокардии до и после операции
На момент выписки больным повторялось контрольное ЭХО-КГ исследование для оценки степени митральной недостаточности и сократимости миокарда после операции реваскуляризации.
Данные ЭХО-КГ до и после операции представлены в табл. 5.
Таблица 5. Результаты ЭХО-КГ после выполненных операций
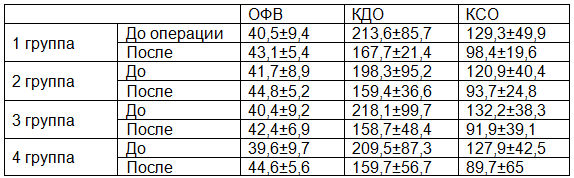
После хирургического лечения отмечено возрастание как общей, так и локальной сократимости. При сравнении до и после операционных данных отмечается прирост общая фракция выброса (ОФВ) с 40,57 до 43,12 в 1 группе, с 41,78 до 44,85 во 2 группе, с 40,46 до 42,47 в 3 группе и с 39,67 до 44,64 в 4 группе. Уменьшение объемов ЛЖ отмечено во всех исследуемых группах, конечно-диастолический объем (КДО) с 213,64 до 167,76 в 1 группе, с 198,32 до 159,45 во 2 группе, с 218,14 до 158,76 в 3 группе и с 209,56 до 159,77 в 4 группе.
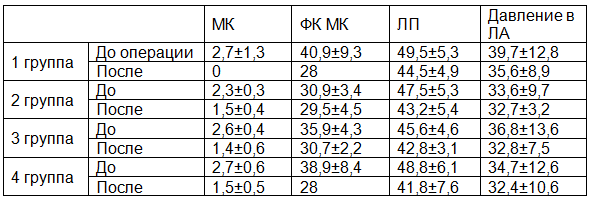
По сравнению с дооперационными значениями размеры левого и правого предсердий, а так же левого желудочка уменьшились. Митральная регургитация уменьшилась с 2,7 до 0 в 1 группе, с 2,3 до 1,5 во 2 группе, с 2,6 до 1,4 в 3 группе и с 2,7 до 1,5 в 4группе пациентов. Расчетное систолическое давление в легочной артерии снизилось. Диаметр фиброзного кольца митрального клапана по сравнению с исходными значениями уменьшился с 40,94 до 28 в 1 группе, с 30,94 до 29,53 во 2 группе, с 35,94 до 30,76 в 3 группе и с 38,94 до 28 в 4 группе.
Динамика основных объемных показателей ЛЖ после операции представлены в нижеприведенной табл. 6.
Таблица 6. Динамика степени митральной недостаточности после операции
После реваскуляризации миокарда была выявлена динамика в основных линейных показателях, характеризующих геометрию ЛЖ у пациентов. Размер длинной оси ЛЖ уменьшился и составил в среднем 8,7 ± 0,02 см. Значительно в меньшей степени отмечалось уменьшение размеров коротких осей ЛЖ. Так, короткая ось на уровне митрального клапана составила 4,6 ± 0,2 см (по сравнению с 5,2 ± 0,01, р > 0,05), на уровне папиллярных мышц 5,6 ± 1,0 см (исходно 6,2 ± 0,5), на верхушечном уровне 3,5 ± 0,6 (исходно 4,3 ± 0,6 см). Соответственно, индекс сферичности на базальном уровне уменьшился и составил 0,52 по сравнению с 0,54 исходно, на среднем уровне - 0,64 при исходном 0,65, на верхушечном уровне - 0,40 при исходном 0,44. Таким образом, достоверное изменение коэффициента сферичности было выявлено только на верхушечном уровне.
Обсуждение. Анализируя результаты проведенного исследования выявлено, что пациенты с ПАЛЖ и сопутствующим поражением митрального клапана относятся к тяжелой категории больных и характеризуются тяжелым проявлением коронарной и сердечной недостаточности. Основными механизмами, участвующими в развитии митральной недостаточности является изменение геометрии левого желудочка, вследствие ишемического ремоделирования и нарушения функции сосочковых мышц. Так же выявлено, что наличие сопутствующей митральной недостаточности неблагоприятно влияет на течение послеоперационного периода у больных с ПАЛЖ, что проявляется высокой летальностью и частым развитием осложнений в раннем послеоперационном периоде [1, 2, 5-7]. В исследовании выявлено, что протезирование МК, в сочетании с геометрической реконструкцией ЛЖ и реваскуляризацией миокарда имеет более высокую летальность в сравнении с пластикой клапана, выполненные при одинаковых исходных данных, что в свою очередь подтверждает исследования других авторов, такими как R.Dion, Akins C.W. и Bitran D. Существующие хирургические методы пластики МК, выполненные трансвентрикулярным доступом при митральной недостаточности позволяют выполнить эффективную коррекцию порока одномоментно с реконструкцией ЛЖ и реваскуляризацией миокарда [3-5]. В случаях отсутствия значительной митральной аннулодилятации оптимальным способом коррекции может быть вальвулопластика край в край. При расширенном же фиброзном кольце и митральной регургитации превышающую вторую степень может потребоваться более сложная реконструкция подклапанного аппарата и имплантация опорного кольца Карпантье [4, 7, 8]. Имплантация опорного кольца в митральную позицию, выполненная при операции геометрической реконструкции ЛЖ и реваскуляризации миокарда обеспечивает более надежную запирательную функцию клапана в сравнении с безимплантационными методами пластики и обеспечивает более жесткую фиксацию фиброзного кольца, что в свою очередь и в отдаленном периоде будет предотвращать рецидив анулодилатации и митральной регургитации. Операция геометрическая реконструкция ЛЖ и реваскуляризация миокарда в сочетании с коррекцией митральной регургитации приводит к восстановлению нормальной геометрии ЛЖ, уменьшает степень митральной недостаточности и дает хорошие непосредственные результаты.
