Цель исследования. В течение острейшего периода (1-3 сутки) ишемического атеротромботического каротидного инсульта исследовать концентрацию серотонина (С) в плазме обогащённой тромбоцитами (ПОТ) и тромбоцитах (ТС) периферической крови больных, по показателям которой возможно опосредованно судить о функциональной активности серотонинергической церебральной системы. Многие механизмы патогенеза инсульта остаются не исследованными. В частности, не до конца известна реакция на острую церебральную ишемию одной из основных нейромедиаторных систем мозга- серотонинергической. О реакции этой системы можно ориентироваться по характеру изменений серотонина в гуморально-транспортном её звене, поскольку процессы накопления, хранения и метаболизма этого медиатора очень сходны с таковыми в нейронах [2-5,9,10].
Задача исследования: исследовать количественное содержание в (нг/мл) С в ПОТ и тромбоцитах периферической крови в острейшем периоде атеротромботического каротидного ишемического инсульта у больных с тяжелым, угрожаемым для жизни течением заболевания, и в том числе заканчивающимся летально.
Материалы и методы исследования. Основную группу наблюдений составили 20 больных в острейшем (1-3 сутки) периоде каротидного атеротромботического ишемического инсульта с тяжёлым течением и неблагоприятным для жизни прогнозом. Ее образовали больные в возрасте 55-75 лет (средний - 69.4±1,7), из которых было 14 (70%) женщин и 6 (30%) мужчин. 7 человек (5 мужчин и 2 женщины) умерли в остром периоде инсульта. У 13 (65%) пациентов ишемический инсульт возник впервые в жизни, у остальных- 7 (35%) - повторно. В 14 (70%) случаях очаг ишемии располагался в бассейне среднемозговой артерии слева, в 6 (30%) - справа. У 18 (90%) больных инфаркт мозга, по данным МРТ, распространялся на две и более доли, у двух (10%) он ограничивался одной его долей. При поступлении 13 (65%) человек были в тяжёлом состоянии, 7 (35%) - в состоянии средней степени тяжести. Тяжесть состояния больных в острейшем периоде инсульта оценивалась в баллах по шкале Глазго и по Скандинавской шкале инсульта. На момент первого осмотра и забора крови 4 (20%) человека находились в коме на ИВЛ, 6 (30%) – в сопоре, 7 (35%) - в оглушении и 3 (15%) - в ясном сознании. Выраженный бульбарный синдром отмечался у 15 (75%) человек, парез взора у 15 (75%). У всех больных был грубый центральный парез до плегии в руке.
Показатели обследования 36 больных в острейшем (1-3 сутки) периоде со среднетяжёлым течением острого каротидного ишемического инсульта использовали для сопоставительного анализа. Средний возраст пациентов 65,9±1,3 лет. Из них было 12 (33,3%) женщин и 24 (66,7%) мужчин. У 22 (61,1%) пациентов ишемический инсульт возник впервые в жизни, у 14 (38,9%) - повторно. В 19 (52,8%) случаях очаг ишемии располагался в бассейне среднемозговой артерии слева, в 17 (47,2%)- справа. У 23 (63,9%) пациентов зона инфаркта, по данным МРТ, ограничивалась пределами одной доли мозга, у 13 (36,1%)- распространялась на две и более доли. При поступлении в стационар 14 (38.95%) человек были в удовлетворительном состоянии, 17 (47,2%) - в состоянии средней степени тяжести, 5 (13,9%) – в тяжелом состоянии. На момент первого осмотра и забора крови (1-3 сутки) : 31 (86%) человек находился в ясном сознании, 2 (5,6%) – в оглушении , 1 (2,8%)- в сопоре и у двух (5,6%) пациентов отмечалось психомоторное возбуждение. У всех больных имелся центральный спастический гемипарез: его средний балл в руке 2,9±0,3; в ноге 3,6±0,2.
Группу лабораторного контроля составили 20 больных с факторами высокого риска мозгового инсульта (артериальной гипертонией, ожирением, курением, гиперхолестеринемией, сахарным диабетом) в аналогичном с больными инсультом возрасте (средний - 63±1,3 лет).
Концентрация растворённого серотонина в ПОТ крови определялась в нг/мл методом иммуноферментного твёрдофазного анализа с помощью тест-системы ELISA (Serotonin ELISA, Hamburg). Содержание ТС также в нг/мл рассчитывалось по формуле в зависимости от количества тромбоцитов в обогащённой плазме крови. Забор крови производился при первом осмотре больного в острейшем (1-3 сутки) периоде ишемического инсульта.
Результаты исследования. Как видно из табл. 1, концентрация С в ПОТ и ТС у больных с тяжёлым течением инсульта (2-6 баллов по Скандинавской шкале инсульта) высоко достоверно ниже группы лабораторного контроля (p<0,0005). Несмотря на то, что большинство больных из группы с тяжёлым течением инсульта было осмотрено на 3 сутки заболевания, из таблицы видно, что депрессия серотонинергической системы начинается уже с первых суток.
В группе умерших больных концентрация С в ПОТ и ТС так же существенно ниже показателей группы лабораторного контроля (p<0,005), однако она незначительно выше показателей концентрации С в группе больных с тяжёлым течением инсульта в целом и в группе больных с инсультом средней степени тяжести.
В группе больных со среднетяжёлым течением ишемического инсульта (34-41 балл по Скандинавской шкале инсульта) концентрация С в ПОТ и ТС значимо (p<0,0005) выше концентрации С в группе лабораторного контроля. При этом, она незначительно выше концентрации С в ПОТ и ТС у больных с тяжёлым течением инсульта на 1 и 3 сутки заболевания и практически не отличается от показателей концентрации С у умерших больных.
По табл. 1 хорошо прослеживается депрессия концентрации С в ПОТ и ТС в течение всего острейшего периода инсульта. Минимальная концентрация С имеет место на третьи сутки заболевания. Подобная тенденция имеется и в группе больных с тяжёлым течением инсульта.
Таблица 1. Средние показатели тяжести инсульта, концентрации серотонина (нг/мл) в плазме обогащённой тромбоцитами (ПОТ) и тромбоцитах (ТС) в острейшем периоде ишемического инсульта
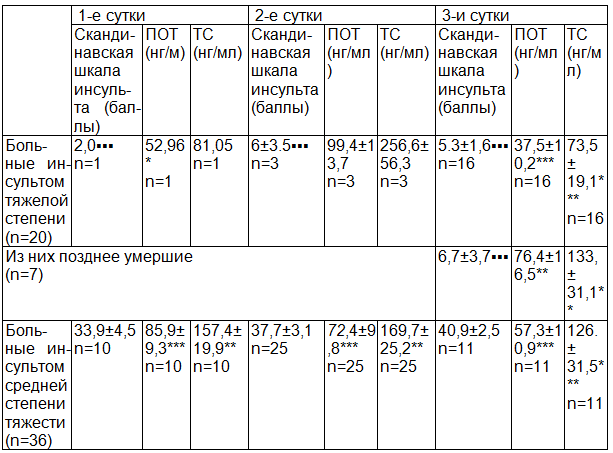
Примечания: p - достоверное отличие больных инсультом от группы с факторами высокого риска (ПОТ 139,5±8,6 нг/мл.; С в Tr 304,1±26,9 нг/мл), при p<0,05*; p<0,005**; p<0,0005***; p1 - достоверное отличие больных инсультом тяжёлой степени от больных инсультом средней степени тяжести, при p1<0,05▪; p1<0,005▪▪; p1<0,005▪▪▪.
Обсуждение. Полученные данные свидетельствуют о том, что гуморальная серотониновая система активно включается в механизмы стресса мозгового инсульта уже в дебюте заболевания. Происходит существенное снижение концентрации С в одном из главных его депо – в тромбоцитах. Поскольку, как уже было сказано, аналогичные процессы накопления, хранения и метаболизма этого медиатора происходят и в серотониновых нейронах головного мозга, и в их синаптической щели, то это свидетельствует о снижении функциональной активности серотонинергической нейромедиаторной системы. Острые нарушения мозгового кровообращения относятся к стрессовым для организма состояниям, поэтому развивающийся дефицит С в мозговых нейронах связан с повышенным его метаболизмом в ЦНС. Снижение содержания С может быть связано также с истощением его запасов ввиду участия в каскаде различных патологических ( метаболических и иных) реакций с острейшего периода инсульта, с повышенной физиологической инактивацией, уменьшением синтеза в условиях нарушения метаболических процессов, а также со снижением функции регуляторных структур головного мозга, участвующих в механизмах адаптации [2-4,9,10].
При этом депрессия серотонинергической системы возникает уже в первые сутки развития неврологической симптоматики, а максимальное снижение концентрации С в ПОТ и ТС происходит на третьи сутки.
У больных с изначально низким содержанием ТС отмечается более тяжёлое течение инсульта, чем у больных с относительно более высокими его значениями при средней степени тяжести инсульта. Это указывает на большее истощение серотонинергической системы и может быть маркером тяжести заболевания. Подобные результаты были получены в работе Скворцовой В.И. с соавт. [7].
Более высокую концентрацию ТС у больных в тяжёлом состоянии с большими очагами повреждения можно объяснить следующим образом: процессы перекисного окисления липидов, локального воспаления в очаге ишемии приводят к постепенному снижению неспецифического и приобретённого Т-клеточного иммунитета 1-го типа. При этом наблюдается значительное снижение генерации Т-лимфоцитами гама-Интерферона , гама - Интерферон является физиологическим супрессором активности белка-переносчика С в ЦНС и на тромбоцитах , и поэтому его снижение приводит к активации белка-переносчика С , что в свою очередь ведёт к повышению его содержания в тромбоцитах. Можно предположить, что изначально высокий уровень С у больных с большими очагами повреждения являются следствием активного воспалительного процесса, сопровождающегося постепенным снижением Т-клеточного иммунитета [7,8].
Кроме того, Г.Н.Бельской с соавт. показано, что при ишемическом инсульте возможно высвобождение С тромбоцитами, на поверхности которых находится серонектин , связывающий С. Этот гликопротеин обнаружен циркулирующим в крови в небольшом количестве - на поверхности лимфоцитов и гранулоцитов. Серотонектин содержится в парафолликулярных клетках щитовидной железы. При инсульте возможен выброс серотонина в кровь в результате активации гипоталамо-гипофизарно-надпочечниковой системы, для которой он является нейрогуморальным триггером [1].
Выводы Выраженный и стойкий дефицит гуморального серотонина при ишемическом каротидном атеротромботическом инсульте опосредованно свидетельствует о дефиците церебрального серотонина и о снижении функциональной активности серотонинергической системы, играющей важную роль в антидепрессантных и антиноцецептивных механизмах мозга. Низкий уровень С в ПОТ и ТС с первых суток ишемии и снижение его концентрации на протяжении всего острейшего периода заболевания может быть уже маркёром неблагоприятного для жизни течения заболевания.
