Злокачественные новообразования (ЗНО) занимают второе место среди причин смертности, как за рубежом, так и в Российской Федерации [1]. При этом непосредственной причиной смерти служит прогрессирование первичных распространенных форм опухолей, либо прогрессирование вторичных опухолей (рецидивов и метастазов). Появление рецидивов или метастазов ЗНО, как правило, предопределяют неблагоприятный исход заболевания.
Один из ведущих методов лечения больных с рецидивными и метастатическими солидными опухолями - это противоопухолевая химиотерапия. Тем не менее, при выборе этого метода лечения трудно предсказать реакцию конкретной опухоли на лечение химиопрепаратами [5]. Основная проблема для клиницистов при принятии решении о назначении химиотерапии - неопределенность ответа опухоли на введение цитостатиков.
Существование опухоли, как морфологического субстрата - это взаимодействие двух структурных компонентов: паренхимы и экстрацеллюлярного матрикса (ЭЦМ) [4]. Формирование ЭЦМ новообразования регулируется сигналами клеток паренхимы опухоли. В свою очередь рост паренхимы обусловлен увеличением числа опухолевых клеток в процессе их многократного удвоения в результате митотического деления, то есть, в результате их пролиферации [2].
Одновременно с увеличением количества клеток в паренхиме в опухоли идет процесс их убыли вследствие таких процессов, как апоптоз [7,8] и некроз [4]. Совокупность этих процессов получила название фактор клеточных потерь (ФКП) [3]. Темп роста паренхимы опухоли определяется сочетанием митотической активности опухоли (МАО) и ФКП [6].
Основной механизм действия противоопухолевых препаратов - необратимое повреждение клетки, находящейся в интерфазе или процессе митотического деления. Клетки в состоянии «пролиферативного покоя», как правило, к химиопрепаратам не чувствительны. Таким образом, МАО определяет количество точек приложения химиопрепаратов в опухоли. Следовательно, введение химиопрепаратов смещает баланс кинетических факторов МАО:ФКП в сторону замедления роста опухоли. Таким образом, ФКП и МАО в совокупности определяют кинетику роста опухолевого узла.
В настоящей работе мы поставили цель определения влияния кинетических параметров опухоли на эффективность химиотерапии.
Для достижения указанной цели были поставлены следующие задачи:
- Разработать абстрактную модель опухолевого роста, в которой скорость роста опухоли определялась бы сочетанием таких структурных параметров, как МАО, доля стромы в опухоли, доля паренхимы, доля некрозов, доля клеток паренхимы в интерфазе и доля клеток в состоянии пролиферативного покоя, а также уровнем клеточных потерь.
- Определить влияние МАО и ФКП на скорость роста рецидивных и метастатических опухолей.
- Изучить влияние химиотерапевтического лечения на кинетику роста опухоли.
- Определить при каких кинетических параметрах роста опухоли можно добиться максимального эффекта от химиотерапевтического лечения.
Совместно с сотрудниками кафедры математики Нижегородского государственного университета имени Н.И. Лобачевского нами разработана математическая модель роста рецидивных и метастатических опухолей, в которой рост опухоли запрограммирован процессами пролиферации и клеточных потерь. Исходными данными для модели послужили морфометрические параметры рецидивных и метастатических опухолей. В результате расчетов были получены такие кинетические параметры, как ФКП и скорость роста опухоли. Учитывая, что в основе опухолевого роста лежит удвоение клеток ее паренхимы, для удобства оценки скорости роста опухоли мы применяли показатель времени удвоения опухоли (ВУО). Для удобства расчетов кинетических параметров исследуемых опухолей на основе указанной модели была создана компьютерная «Программа расчета фактора клеточных потерь в рецидивных и метастатических злокачественных опухолях» (свидетельство о государственной регистрации программы для ЭВМ №2014661872).
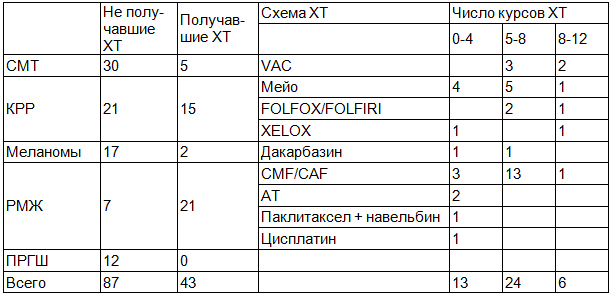
Всего в Нижегородском областном онкологическом диспансере в период с 2009 по 2012 г. было обследовано 130 больных с рецидивными и метастатическими опухолями пяти различных видов: саркомы мягких тканей (СМТ), колоректальный рак (КРР), меланомы, рак молочной железы (РМЖ) и плоскоклеточный рак головы и шеи (ПРГШ). Информация о количественном соотношении больных в разных группах, перенесших разные виды лечения приведена в табл. 1. У 43 больных рост опухоли проходил на фоне химиотерапевтического лечения. Скорость роста опухолей этой группы сопоставлялась со скоростью роста вторичных опухолей оставшихся 87 пациентов, не получавших химиотерапевтическое лечение (ХТ).
Таблица 1. Распределение клинических наблюдений по локализациям первичных очагов и характеру проведенного лечения
В целях исследования структуры опухолевых очагов для каждого из обследуемых пациентов проводилась морфометрия гистологических препаратов удаленных опухолей.
На основании компьютерной обработки данных о структуре опухолевых очагов при помощи указанной выше математической программы были получены кинетические параметры исследуемых рецидивных и метастатических опухолей (табл. 2).
Таблица 2. Кинетические параметры опухолей разного типа
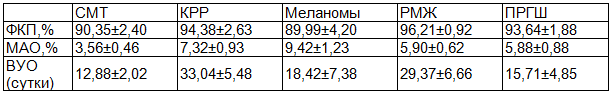
При анализе данных, изложенных в табл. 2, можно выделить две основные категории рецидивных и метастатических опухолей.
- Относительно медленнорастущие опухоли: вторичные очаги КРР (среднее ВУО 33,04±5,48) и РМЖ (среднее ВУО 29,37±6,66).
- Быстрорастущие опухоли: рецидивные и метастатические СМТ (среднее ВУО 12,88±2,02), меланомы (среднее ВУО 18,42±7,38) и ПРГШ (среднее ВУО 15,71±4,85).
Среди опухолей всех типов могут встречаться как быстрорастущие, так и медленнорастущие опухоли.
На основании сравнительного анализа двух групп пациентов, получавших и не получавших лечение цитостатиками, были даны рекомендации: при каких кинетических параметрах опухоли можно достигнуть максимального эффекта химиотерапии, а при каких химиотерапевтическое лечение малоэффективно.
Эффективность проведенного лечения в онкологии, как правило, определяется в виде увеличения сроков дожития пациентов, получавших химиотерапию по сравнению с пациентами, не получавших лечение цитостатиками. Проведенные исследования показали, что у обследованных нами пациентов, получавших химиотерапию, продолжительность жизни составила 16,89 месяцев, а медиана выживаемости 16 месяцев. Средняя же выживаемость пациентов, не получавших химиотерапию несколько меньше (13,30 месяцев). Медиана выживаемости этой группы больных 9 месяцев.
В нашем исследовании мы определили коэффициент эффективности химиотерапии (КЭХТ), как степень замедления роста опухоли под влиянием цитостатиков. Общий КЭХТ был равен отношению среднего ВУО у пациентов, которым проводилась химиотерапия, к среднему ВУО пациентов, не получавших химиотерапию. Общий КЭХТ для всех исследованных нами групп пациентов составил 1,57.
Нами проведен анализ эффективности химиотерапии в различных диапазонах таких кинетических параметров рецидивных и метастатических опухолей как МАО (табл. 3),ФКП (табл. 4) и ВУО (табл. 5).
Таблица 3. Прогноз и эффективность лечения цитостатиками рецидивных и метастатических опухолей с разной митотической активностью
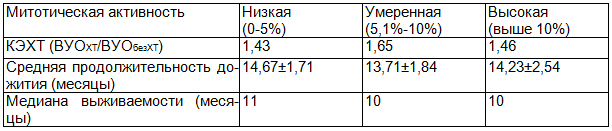
Как видно из табл. 3, такой показатель, как МАО, в нашем исследовании практически не влияет на выживаемость пациентов. Для пациентов с различной МАО различия в эффективности химиотерапии, рассчитанные для каждой группы, не велики. Для опухолей c умеренной митотической активностью выявлены максимальные показатели КЭХТ (1,65). КЭХТ по нашим данным ниже для группы рецидивных и метастатических ЗНО с низкой митотической активностью опухоли (1,43) и для группы опухолей с высокой митотической активностью опухоли (1,46).
Таблица 4. Прогноз и эффективность лечения цитостатиками рецидивных и метастатических опухолей с разным уровнем клеточных потерь
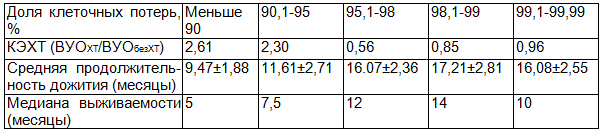
Отмечено снижение КЭХТ (с 2,61 до 0,96) по мере увеличения показателя ФКП. Наибольший отклик на лечение цитостатиками дают опухоли с низкими показателями ФКП. Проведение химиотерапевтического лечения пациентов с рецидивными и метастатическими опухолями с уровнем клеточных потерь выше 95%, по нашим данным, не приводит к замедлению опухолевого роста.
В то же время, уровень ФКП, по нашим данным, имеет большое прогностическое значение. По мере увеличения клеточных потерь отмечается тенденция увеличения таких показателей выживаемости, как средняя продолжительность жизни пациента (с 9,47±1,88 до 16,08±2,55 месяцев) и медиана выживаемости (с 5 до 10 месяцев).
Таблица 5. Прогноз и эффективность лечения цитостатиками рецидивных и метастатических опухолей с различной скоростью роста

Выявлена зависимость эффективности химиотерапии от скорости роста рецидивной или метастатической опухоли. Зависимость эта носит нелинейный характер. Наибольший показатель КЭХТ (1,33) отмечен у опухолей с очень высокой скоростью роста. У опухолей с ВУО в диапазоне от 20,1 до 40 суток замедления скорости роста под влиянием цитостатиков не выявлено.
Доказано, что чем меньше ВУО, тем хуже прогноз для жизни пациента с рецидивной и метастатической опухолью. По мере увеличения ВУО медиана выживаемости увеличивается с 5,5 до 16,5 месяцев.
С использованием методики Многофакторного регрессионного анализа разработан дробный факторный план. В качестве независимых переменных служили кинетические параметры МАО и ВУО пациентов основной группы. В качестве зависимой переменной (предиктора) - КЭХТ.
С помощью специализированной компьютерной программы обработки и планирования эксперимента на основе полных и дробных факторных планов, разработанной сотрудниками Нижегородского государственного университета имени Н.И. Лобачевского, построена математическая модель второго порядка в виде функции отклика КЭХТ=f(МАО, ВУО):
КЭХТ=0,20424+0,16848* МАО+0,061713* ВУО-0,008465* МАО* ВУО+0,00092596* МАО2-0,0005346* ВУО2-0,00054675 *МАО2 *ВУО-0,000015584* МАО* ВУО2+0,000020779* МАО2* ВУО2
С целью более наглядного восприятия этой математической зависимости выполнена аппроксимация данной функции двух переменных в виде нелинейной поверхности, отображенной на номограмме, представленной на рис. 1.
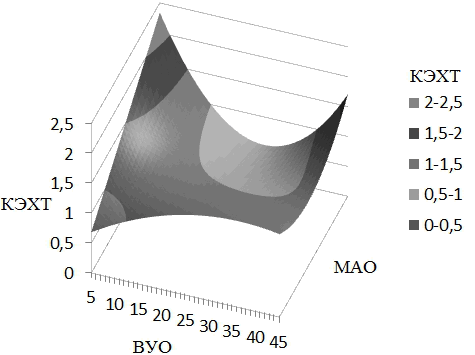
Рис. 1. Номограмма зависимости коэффициента эффективности химиотерапии от скорости роста и митотической активности опухоли.
По шкале X отложены значения МАО, по шкале Y - ВУО. Значения КЭХТ отложены по шкале Z. При аппроксимации значений КЭХТ на диаграмме получена искривленная поверхность, по своей форме напоминающая седло. На представленной поверхности выполнена цветовая градация различных диапазонов КЭХТ. На практике это используется следующим образом: при пересечении перпендикулярных линий, проведенных через значения кинетических параметров ВУО и МАО, определяем значение КЭХТ. При величинах КЭХТ ниже 1 делаем вывод, что проведение химиотерапевтического лечения в нашем случае будет малоэффективным. При значениях выше 1,5 проведение ХТ рекомендуется. В остальных случаях, решение о проведении лечения цитостатиками принимается на усмотрении лечащего врача.
Подводя итоги всему изложенному выше можно сделать следующие выводы:
- В ходе проведенной нами работы предложен новый критерий оценки эффективности проведения химиотерапевтического лечения (КЭХТ), который характеризует степень замедления роста опухоли под влиянием цитостатиков.
- Доказано, что кинетические параметры роста опухолей являются важными прогностическими факторами течения рецидивных и метастатических ЗНО.
- Для удобства применения в клинической практике построен трехмерный график, позволяющий на основании сочетания кинетических параметров вторичной опухоли определить КЭХТ.
- Опираясь на полученные данные, установлено, что наибольшей чувствительностью к химиотерапии обладают опухоли с умеренной митотической активностью, высокой скоростью роста и низкими клеточными потерями.
