Рак молочной железы занимает лидирующие позиции в структуре злокачественных новообразований. В 2012 г. в России зарегистрированы 59538 новых больных. По сравнению с 2007 г. прирост составил 13,8%. Данное заболевание занимает 1-е место в структуре онкологической заболеваемости женского населения стран СНГ [3]. К 2020 г. прогнозируют увеличение ежегодной заболеваемости раком молочной железы (РМЖ) до 2000000 Лечение больных раком молочной железы включает хирургическое лечение (радикальная резекция молочной железы или мастэктомия) в сочетании с химиолучевым лечением. Самым распространенным осложнением радикального оперативного лечения рака молочной железы является лимфорея или серома. Серома или лимфоцеле – это скопление серозной жидкости в «мёртвом пространстве» под мобилизованными кожными лоскутами в подмышечной области после радикальной мастэктомии и в ткани молочной железы после органосохраняющего лечения. Увеличение риска образования серомы может быть связано со следующими факторами: пожилой возраст, высокий индекс массы тела (более 25), использование электорокоагуляции при выполнении хирургического пособия, вид хирургического лечения Различные группы авторов на протяжении длительного времени докладывают о высокой частоте развития сером в послеоперационном периоде. Частота этого осложнения достигает 81% [5]. Длительная лимфорея мешает проведению специального лечения (химиотерапии или лучевой терапии) больным в послеоперационном периоде в установленные сроки, а также увеличивает экономическую нагрузку на лечебно-профилактическое учреждение в связи с длительным пребыванием больных. Выполнение подмышечной лимфаденэктомии, как обязательного элемента операции радикальной мастэктомии, с пересечением большого количества лимфатических протоков дают возможность лимфе свободно истекать в подмышечную ямку и накапливаться в подмышечной области. Мобилизованные кожные лоскуты во время операции создают еще большее пространство для накапливания жидкости, а мышечная помпа за счет движения верхней конечности после операции увеличивает ток лимфы [1]. Длительно существующая лимфорея опасна присоединением вторичной инфекции, а также усугубляет развитие лимфедемы верхней конечности. Различными авторами предлагаются хирургические приемы, позволяющие предупредить развитие лимфореи и тем самым улучшить непосредственные результаты операции. Использование дренажей после хирургии молочной железы является самым изученным вопросом и в то же время самым спорным. Варианты дренажей после радикальных мастэктомий зависят от предпочтений хирургов. Дренажи после радикальных мастэктомий используются рутинно, так как считается, что они снижают объем лимфорейной жидкости и частоту развития сером. Однако, дренажи, помещенные в подмышечную область, могут причинять значительный дискомфорт. Они могут вызывать боль, ограничение нормальной подвижности плечевого сустава, быть источником вторичных инфекций раны, так как могут являться проводниками инфекции в рану и самостоятельно могут вызывать воспаление окружающих тканей, как инородные тела. Вакуумные дренажи были впервые представлены в 1947 г. Murphey, который полагал, что данные дренажи, создавая отрицательное давление, закроют полость оставленную после выполнения подмышечной лимфаденэктомии. Отрицательное давление способствует «прилипанию» мобилизованных кожных лоскутов, тем самым, ускоряя заживление раны, снижая частоту инфекционных осложнений, некрозов краев раны, расхождения краев раны и образования серомы. Общепринятая практика включает оставление дренажей в ране, пока объем суточного отделяемого не будет ниже 30-50 мл/сутки [5]. По литературным данным еще одним методом профилактики лимфореи является применение тканевых сиалентов. Тканевые сеаленты представлены в виде фибринового клея, тромбина, тромбоцитарного клея. Данные препараты активируют последнюю ступень коагуляционного каскада, в частности, превращение фибриногена в фибрин в присутствии ионов кальция и тромбина. Тканевые сеаленты, полученные из плазмы, представляют собой два отдельных компонента: концентрат фибриногена/фибронектина/фактора XII и антифибринолитического раствора с тромбином и ионами кальция. Добавление тромбоцитов к тканевым сеалентам усиливает гемостатический процесс, так как тромбоциты создают каркас для образования сгустка. Более того, фибриновый клей стимулирует миграцию клеток в очаг введения, а тромбин вызывает пролиферацию фибробластов. Положительной особенностью фибринового клея, обогащенного тромбоцитами - это способность стимулировать освобождение ростовых факторов эндотелиальными клетками. Многие хирурги пытаются использовать адгезивные компоненты с целью снижения лимфореи после радикальных мастэктомий. Данные препараты «запечатывают» лимфатические и кровеносные сосуды, а также удерживают кожные лоскуты в контакте с грудной стенкой [2]. Некоторые авторы описывают хороший клинический результат, который был получен при применении высокоэнергетического лазера для обработки раневой поверхности после выполнения радикальной мастэктомии (РМЭ). Аналогичные результаты зафиксированы при обработке подключично-подкрыльцово-подлопаточной зоны воздушноплазменными потоками. Некоторые авторы предлагают закрывать полость, образованную в результате осуществления подмышечной лимфодиссекции, миопластикой малой грудной мышцей и фрагментом широчайшей мышцы спины. В Ростовском научно-исследовательском онкологическом институте был разработан и внедрен в ежедневную практику способ ушивания раны при РМЭ без активного ее дренирования в послеоперационном периоде [7,8]. Этот метод с применением рассасывающегося шовного материала и был применен нами в клинической практике.
Цель исследования: улучшение результатов оперативного лечения больных раком молочной железы. Оценка эффективности применения методики бездренажной мастэктомии по Маддену в клинической практике.
Материалы и методы. В работе были изучены результаты лечения 120 больных раком молочной железы II и III стадии, разделенных на 2 группы. В основную группу вошли 60 пациентов, прооперированных в Государственном бюджетном учреждении Ростовской области «Онкологический диспансер» в г. Шахты в период с декабря 2014 г. по сентябрь 2015 г. с применением бездренажной мастэктомии по Маддену. В контрольную группу вошли 60 человек, прооперированных с применением стандартной мастэктомии по Маддену. Средний возраст больных в основной группе составил 61,3±0,5 года, в контрольной 59,8±0,6 года. По стадиям заболевания пациентки распределились следующим образом: основная группа – 32 человека (T2N0Mo), 21 человек (T2N1Mo), 7 человек (T2N3аMo); контрольная группа - 29 человек (T2N0Mo), 20 человек (T2N1Mo), 11 человек (T2N3аMo) (табл.1).
Таблица 1. Распределение пациенток основной и контрольной групп по стадиям заболевания

У всех больных учитывалось количество и длительность лимфореи, длительность операции, частота развития послеоперационных осложнений.
Для статистического анализа динамики лимфореи в послеоперационом периоде использовали критерий Стьюдента.
Описание методики. Больным в основной группе выполнялась радикальная модифицированная мастэктомия по Маддену с удалением подмышечно-подлопаточной и подключичной клетчатки с подшиванием образовавшегося кожно-жирового лоскута к ложу подмышечно-подлопаточной клетчатки шовным материалом Викрол 2-0. Подкожная клетчатка ушивалась тем же шовным материалом. Кожа сшивалась косметическим швом с применением рассасывающегося шовного материала. Подкожная жировая клетчатка и ложе подмышечно-подлопаточной клетчатки дренировались полосками перчаточной резины (рис. 1, 2).
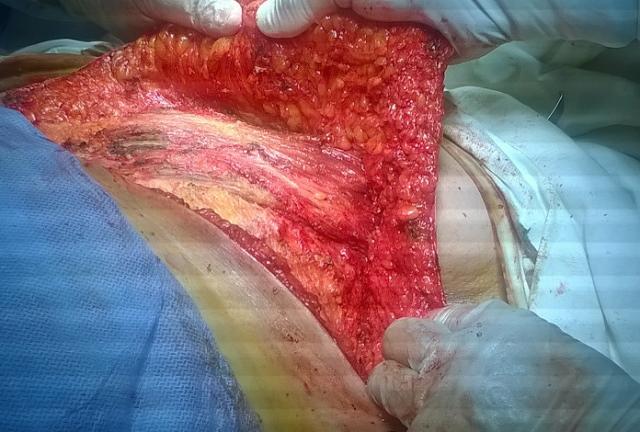
Рис. 1. Подшивание кожно-жирового лоскута к ложу подмышечно-подлопаточной клетчатки.
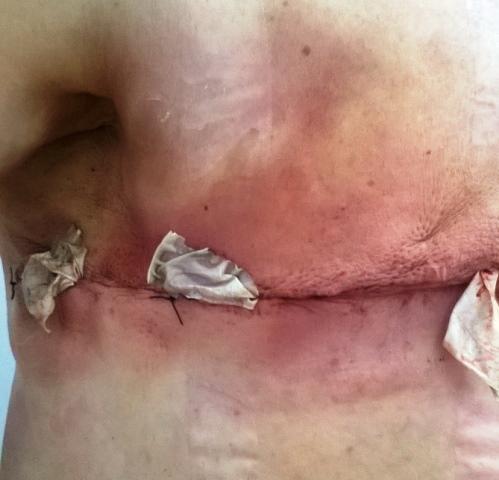
Рис. 2. Вид послеоперационной раны после применения методики бездренажной мастэктомии.
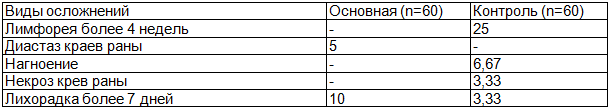
Результаты и обсуждение. Проанализировав имеющиеся данные, получены следующие результаты: осложнения послеоперационного периода наблюдались у 20% пациентов. Лимфорея более 12 дней наблюдалась в основной группе в 60% случаев, в контрольной в 20% случаев. Лимфорея более 1 месяца в основной группе не наблюдалась, тогда как в контрольной составила 25%. При этом у пациентов контрольной группы на фоне длительной лимфореи развились следующие послеоперационные осложнения: нагноение раны (6,67%), некроз краев раны (3,33%), что потребовало продления длительности антибиотикотерапии, смену режима терапии, некрэктомию с наложением вторичных швов (табл. 2).
Таблица 2. Осложнения после радикальной мастэктомии в раннем послеоперационном периоде, %
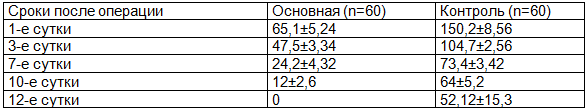
Динамика лимфореи также была лучше в основной группе, чем в контрольной. Так на 1-е сутки после операции среднее количество отделяемого в основной группе составило 65,1±5,24 мл, тогда как в контрольной группе этот показатель составил 150,2±8,56. На 12 сутки в основной группе лимфореи не наблюдалось, тогда, как в контроле количество жидкости составило 52,12±7,3 мл (табл. 3).
Таблица 3. Сравнение динамики лимфореи в послеоперационном периоде у пациенток перенесших мастэктомию (M±m)
Также к преимуществам бездренажной методики можно отнести лучшие косметические результаты (рис. 3).
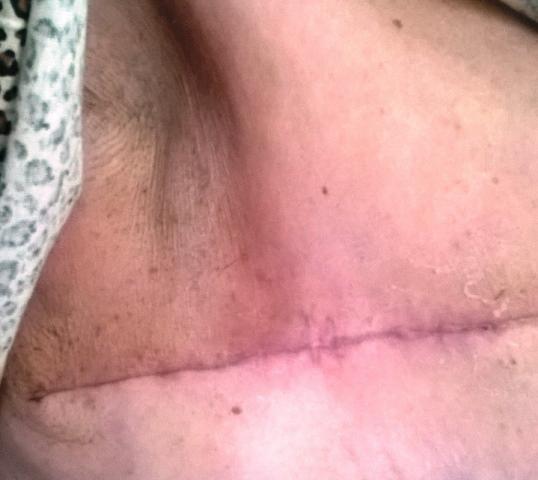
Рис. 3. Вид послеоперационной раны после применения методики бездренажной мастэктомии на 15 сутки.
Однако длительность операции в основной группе была в среднем на 50±15 минут больше, чем в контроле что обусловлено усложнением методики оперативного вмешательства, а повышение температуры тела в послеоперационном периоде выше 38˚С наблюдалось на 30% чаще чем в контроле.
Выводы. Частота, тяжесть и длительность лимфореи зависит от объема «мертвого пространства» на месте ложа подмышечно-подлопаточной клетчатки. Применение методики бездренажной мастэктомии по Маддену с подшиванием образовавшегося кожно-жирового лоскута к ложу подмышечно-подлопаточной клетчатки рассасывающимся шовным материалом позволяет снизить интенсивность и длительность лимфореи, снизить число послеоперационных осложнений, улучшить косметические результаты операции, но приводит к значительному удлинению времени оперативного вмешательства.
