Плоскоклеточный рак головы и шеи занимает 6-е место среди всех злокачественных опухолей в мире. Соотношение заболеваемости между мужчинами и женщинами - 2:1 [1].
Современная стратегия лечения больных плоскоклеточным раком органов головы и шеи включает применение хирургического метода, лучевой терапии, химиотерапии и таргентной терапии, а также различные варианты комбинированного лечения.
В последние годы отмечается бурный рост новых технологических решений в области лучевой терапии. Появились такие методики, как трехмерная конформная лучевая терапия (3DCRT), лучевая терапия с модуляцией интенсивности пучка излучения (IMRT), лучевая терапия с управлением по изображениям (IGRT), адаптивная лучевая терапия (ART), стереотаксическая лучевая терапия и радиохирургия [2].
Основные неудачи терапии данной патологии связаны, в первую очередь, с лечением поздних (III-IV) стадий заболевания, частота которых крайне высока. Быстрый инфильтративный рост опухоли, раннее лимфо- и гематогенное метастазирование, поздняя диагностика и, как правило, выраженные клинические проявления заболевания значительно ограничивают радикальность лечения и являются причиной высокой летальности, которая уже на первом году после установления диагноза достигает более 40% [3]. Комбинированное и комплексное лечение злокачественных новообразований слизистой оболочки полости рта нередко приводит к развитию острых или обострению хронических воспалительных процессов не только в мягких тканях, но и в костных структурах полости рта, вплоть до развития остеорадионекроза [4].
Профилактику нежелательных клинических эффектов комплексного лечения следует рассматривать, прежде всего, в плане нивелирования (исключения) тяжелых, потенциально опасных осложнений. При этом основная роль в профилактике осложнений принадлежит специалистам-онкологам, так как именно они проводят подготовку к облучению, выбирают режимы лучевой терапии и возможность применения химиопрепаратов, определяют границы резекции новообразования. Однако решить этот вопрос без участия стоматологов также не представляется возможным, ввиду различного состояния полости рта у пациентов с новообразованиями данной локализации [5]. Настоящее исследование анализирует стоматологические последствия у больных с раком полости рта, с целью избежать осложнений которые появляются после начала онкологического лечения.
Материалы и методы исследования. Материалом настоящего исследования послужили данные ретроспективного изучения данных больных со злокачественными новообразованиями орофарингеальной зоны в соответствии с клиническими и гистологическими критериями. Исследование проводилось на базе Челябинского окружного клинического онкологического диспансера в период с 2008 по 2014 г.
В общей сложности были зарегистрированы 53 пациента, из которых 10 были исключены из анализа (соответственно 7 умерли и 3 не найдены). Остальные 43 пациента были осмотрены. Данные, соответствующие каждому пациенту были введены в базу данных: возраст, пол, локализации поражения, гистология и предоперационная стадия опухоли, проведенное лечение и лечение осложнений, вредные привычки до и после диагноза рака орофарингеальной зоны, частота посещения стоматолога до диагностики рака и после, с оценкой здоровья полости рта и зубов. При первичном обращении определяли интенсивность поражения кариесом зубов на основании подсчета индекса КПУ у каждого из обследованных и его среднего значения в исследуемой группе. Индекс КПУ определяли путем подсчета суммы кариозных (К), пломбированных (П) и удаленных (У) постоянных зубов в каждом клиническом наблюдении. Интенсивность поражения кариесом в исследуемой группе определяли по формуле:
М = Σ КПУ / N,
где М - величина, характеризующая интенсивность поражения кариесом в исследуемой группе; Σ КПУ - суммы всех индексов КПУ в исследуемой группе; N - общее число обследуемых лиц в группе, имеющих кариес зубов.
Во всех случаях, рак орофарингеальной зоны был диагностирован на основании гистологического исследования очагов поражения с последующим направлением пациента в соответствующий медицинский центр, где проведено соответствующее онкологическое лечение.
Результаты и их обсуждение. В исследовании были проанализированы 43 пациента (27 мужчин (63%) и 16 женщин (37%). Средний возраст составил 65,3 года (диапазон от 29-93 лет). 55% пациентов были курильщиками, и 78% из них бросили курить после постановки диагноза рака полости рта. В 16 случаях (37,2%), повреждения были расположены на латеральном крае языка, в то время как 9 опухолей было расположено на дне полости рта (20,9%), 5 на небе (11,6%), 4 на нижней губе (9,3%), 3 в области альвеолярного отростка нижней челюсти (6,9%), и по 2 на корне языка (4,7%), альвеолярном отростке верхней челюсти (4,7%) и ретромолярной области (4,7%).
Стадии опухоли на момент постановки диагноза были T1N0M0 в 13 случаях (30,2%), T2N0M0 в 8 случаях (18,6%), T4N0M0 в 6 случаях (14%), T3N0M0 (11,6%) и T3N2M0 (11,6%) по 5 случаев, T2N1M0 в 4 случаях (9,3%) и T3N1M0 в 2 случаях (4,7%). Хирургическое лечение было проведено в 9 случаях (21%). 16 пациентов получили только лучевую терапию (37,2%), в то время как 21 пациенту проведена комбинированная терапия, лучевая терапия плюс химиотерапия (48,8%).
В общей сложности 34 пациента получили лучевую терапию либо отдельно, либо в сочетании с химиотерапией, и только 2 из них (5,8%) получили стоматологическое лечение до начала лучевой терапии. В этих случаях была проведена гигиена полости рта, консервативное лечение кариеса и удаление разрушенных зубов.
Ни один из пациентов не посещал регулярно стоматолога для планового осмотра полости рта и зубов во время онкологического лечения. Посещения стоматолога были зафиксированы только в случае острых состояний.
Что касается контроля пациентов после онкологического лечения, 5 пациентов (11,6%) обращались за стоматологической помощью в государственные либо частные стоматологические клиники в плановом порядке, еще 13 пациентов (30,2%) обращались к хирургу стоматологу с целью удаления зубов, остальные 25 пациентов(58,2%) не обращались за стоматологической помощью (у 5 из них было полное отсутствие зубов). 2 раза в день чистят зубы 56% опрошенных, 1 раз в день 32%, вообще не чистят зубы - 12%.
Были зафиксированы следующие осложнения: сухость во рту в 37 случаях (86%), лучевой кариес в 32 случаях (74,4%), затруднение речи в 20 случаях (46,5%), снижение вкусовой чувствительности в 37 случаях (86%).
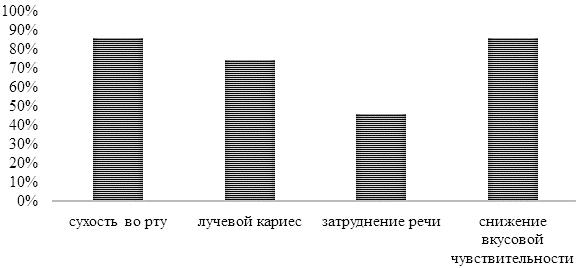
Рис. 1. Структура осложнений лучевой терапии со стороны полости рта.
Оценивалась интенсивность поражения кариесом зубов, и составила 15+ 0,4, что соответствует высокой интенсивности поражения.
В среднем от диагностики рака полости рта до изучения собранных данных прошло 3 года (от 1 до 6 лет).
Несмотря на последние достижения онкологии, в настоящее время, после комбинированного и лучевого лечения злокачественных новообразований челюстно-лицевой области невозможно избежать осложнений, связанных с ионизирующим излучением. В частности, побочным результатом лучевой терапии является интенсивное разрушение зубов. Поражение твердых тканей зубов связывают как с непосредственным действием на них лучистой энергии, так и с последующим иммунодепрессивным состоянием, нарушением минерального и белкового обменов, количества и состава слюны, функционального состояния важнейших физиологических систем организма [6].
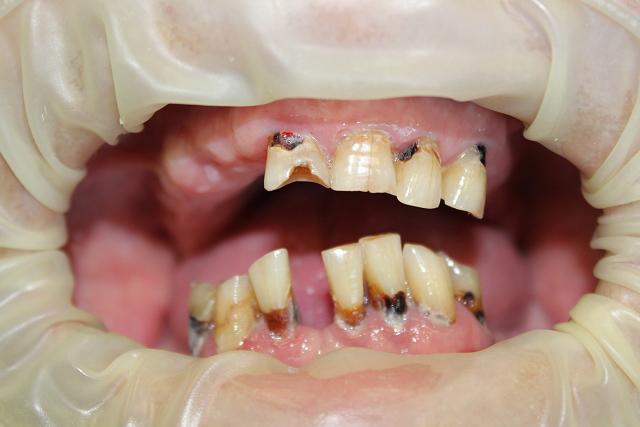
Рис. 2. Пациент В. 63 года. Осложнение после лучевой терапии. Лучевой кариес.
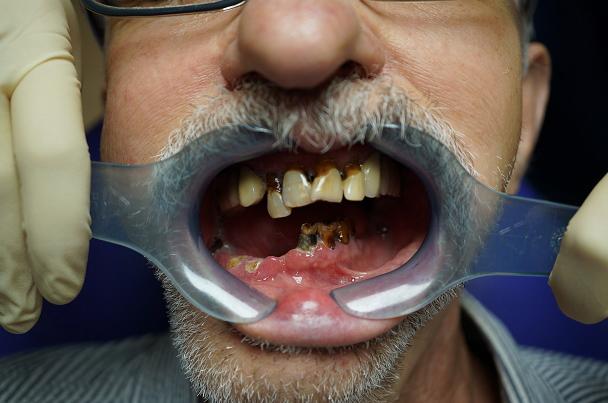
Рис. 3. Пациент А. 51 год. Осложнение после лучевой терапии. Лучевой кариес.
Основной целью стоматолога при подготовке этих больных к специальным методам лечения является профилактика обострения заболеваний зубочелюстной системы, конечным итогом которой должно быть улучшение их качества жизни на всех этапах специального лечения [7].
Стоматологическую помощь у больных с орофарингеальным раком следует начинать с момента обнаружения поражения и постановки диагноза. Стоматологическое сопровождение включает в себя предварительное обследование, подготовку пациента, меры, применяемые после онкологического лечения и долгосрочное наблюдение. В нашем исследовании только 2 пациента были направлены к стоматологу общего профиля для профилактики осложнений после лучевой терапии. Что говорит о том, что пациентам с раком головы и шеи стоматологическая помощь оказывается в ограниченном спектре. Тем не менее, после онкологического лечения, было отмечено увеличение количества пациентов, обратившимся к стоматологу в плановом порядке.
Анализ полученных результатов позволяет связать значительную выраженность патологических изменений тканей зубов не только с воздействием лучевого лечения, негативными изменениями в организме, но и с некачественным проведением гигиенических процедур.
Также частым осложнением лучевой терапии является ксеростомия. Значительная ксеростомия встречается практически в 100% случаев после проведенного лечения, прием интенсивность ее прогрессивно нарастает в первые 6 месяцев после лечения, в дальнейшем происходит частичное восстановление саливации [7].
В этой ситуации, ксеростомия приводит к сухости в полости рта, ощущению жжения, трещинам губ, трудности в приеме пищи и проблемам в использовании зубных протезов. В нашем исследовании 100% облученных пациентов испытывали сухость во рту, хотя и в меньшей степени, чем в конце лучевой терапии. Симптоматическое лечение постлучевой ксеростомии у пациентов без остаточной функции слюнных желез основано на использовании заменителей слюны.
Благоприятное действие заместительной терапии в конечном итоге сказывается и на качестве жизни пациентов с радиационно-индуцированной ксеростомией. Происходит это за счет устранения или уменьшения выраженности чувства дискомфорта в полости рта, нормализации сна и речи. Больные отмечают улучшение настроения [8].
Дисгевзия индуцированная лучевой терапией обусловлена рядом факторов: прямым нейротоксическим действием на клетки вкусовых рецепторов, сухостью во рту и возможным присоединением инфекции. Большинство пациентов выздоравливают в течение 2-3 месяцев, хотя в некоторых случаях гипогевзия может быть постоянной [9].
В нашем исследовании 37 пациентов(100%) сообщили о субъективном постоянном уменьшении вкусовых ощущений.
Заключение. Протоколы профилактики осложнений со стороны полости рта и зубов после лучевой терапии направлены на улучшение качества жизни пациентов. Однако, на основании проведенного исследования можно сделать выводы что в большинстве случаев не уделяется должного внимания осмотру полости рта при планировании онкологического лечения рака орофарингеальной зоны. В результате не принимается никаких мер по профилактике осложнений, что затрудняет достижение цели. Таким образом, диагностика и лечение рака орофарингеальной зоны требует мультидисциплинарного подхода, что способствует сокращению числа тяжелых осложнений.
