Тугоухость остается одной из актуальных проблем оториноларингологии [1-3,5,14]. Снижением слуха различной степени, страдают более 20% населения трудоспособного возраста, что определяет социальную значимость проблемы [1,3,5,14]. 360 миллионов человек в мире страдают нарушениями слуха, согласно данным опубликованным Всемирной Организацией Здравоохранения (ВОЗ).
Каждый третий человек в возрасте старше 65 лет – страдает нарушением слуха различной степени выраженности. Тогда как, умеренное снижение слуха связанное с возрастными изменениями чаще корригируется слуховыми аппаратами [1,5,10], тугоухость высокой степени требует, как правило, проведение кохлеарной имплантации.
Кохлеарная имплантация (КИ) является наиболее эффективным и общепризнанным методом хирургического лечения больных с тугоухостью высокой степени [1,11]. В связи с широким применением кохлеарной имплантации актуальность приобретает анализ и оценка риска и возможных побочных эффектов после хирургического лечения. Одним из возможных осложнений, сопряженных со значительным изменением качества жизни пациента является головокружение [1,2,6,10,16]. Вестибулярные поражения после кохлеарной имплантации встречаются по данным различных авторов в 23-100% [1, 15,16]. У некоторых пациентов головокружение возникает в ранние сроки после операции, в то время как у других пациентов оно развивается через несколько недель и даже месяцев [15,16]. Так же размещение электродной решетки в улитки вызывает морфологические и функциональные изменения во внутреннем ухе. Гистологические исследования демонстрируют, что после кохлеарной имплантации изменения происходят не только в улитке внутреннего уха, но и в sacculus, utriculus и полукружных каналах [16]. Несмотря на микроскопические и функциональные данные, свидетельствующие о повреждении периферического вестибулярного отдела, не все пациенты после кохлеарноий имплантации страдают от послеоперационного головокружения [15,16].
Целью настоящего исследования явилось изучение изменений вестибулярной функции у больных тугоухостью высокой степени после кохлеарной имплантации с использованием объективных методик обследования.
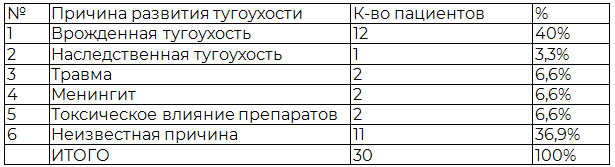
Материалы и методы. Под нашим наблюдением находилось две группы: первая - 30 пациентов, страдающих хронической двусторонней сенсоневральной тугоухостью IV степени тяжести, в возрасте от 17 до 50 лет (медиана возраста – 24,8 года). Причины развития тугоухости у пациентов первой группы представлены в табл. 1. Вторая контрольная группа (20 человек) в возрасте от 18 до 47 лет (медиана возраста – 25,1 года), не имеющих отклонений в вестибулярном и слуховом паспорте.
Таблица 1. Этиологические факторы тугоухости у пациентов первой группы
Всем пациентам первой группы в соответствии с показаниями выполнена кохлеарная имплантация по традиционной методике через кохлеостому слуховыми системами Cochlear Nucleus (6), MedEl (2), Advanced Bionics (5) и Neurelec (17) в Томском филиале ФГБУ «Научно-клинический центр оториноларингологии Федерального медико-биологического агентства».
Критерии исключения: врожденные пороки развития и острые воспалительные заболевания верхних дыхательных путей, наличие в анамнезе или в настоящее время признаков клинически значимого неконтролируемого заболевания любого органа или системы органов (например, активный туберкулез, онкологические заболевания), наличие состояний, которые могут ограничивать законность информированного согласия или искажать интерпретацию результатов исследования (психические нарушения, алкоголизм, значимое снижение интеллекта), выраженные изменения зрительного анализатора, отсутствие информированного согласия, двусторонняя кохлеарная имплантация.
Все пациенты первой группы сначала были опрошены в декретированные сроки на предмет возникновения приступов головокружения, в том случае если пациенты отмечали головокружение были заданы дополнительные вопросы: время появления головокружения, качество, частота возникновения, продолжительность, провоцирующие факторы.
Всем пациентам выполнялись: полный оториноларингологический осмотр (многофункциональная ЛОР-установка Atmos), составление вестибулярного паспорта, исследование вестибулярного анализатора путем регистрации видеонистагмографии (Heinemann 3.SA, модуль Interacoustics VN 415B), калорическая проба (воздушный калоризатор Heinemann), стабилометрия (стабилометрическая платформа ST 150 «БиоМера»). Все исследования проводились в три этапа до хирургического вмешательства, в первые сутки после операции и через месяц после кохлеарной имплантации.
Анализ данных проводился с помощью программы Statistica 6.0 (StatSoft, США) с использованием непараметрических методов (критерий Вилкоксона парных сравнений, дисперсионный анализ Фридмана). Полученные данные представляли в виде медианы (Ме) и 25-го и 75-го процентиля, U-критерия Манна-Уитни для независимых выборок, анализа корреляций Спирмена. Проверка нормальности распределения в тесте Шапиро-Уилка.
Результаты и обсуждение. Анализ опроса пациентов показал, что до хирургического лечения у пациенты первой группы приступов головокружения не отмечали. Из 30 пациентов первой группы у 5 (16,6%) отмечались субъективные симптомы вестибулярной дисфункции на первые сутки после проведения КИ, которые исчезали в течение 3-х дней после хирургического вмешательства. В отдаленные сроки пациенты пользующиеся системой кохлеарной имплантации не предъявляли жалобы, указывающие на патологию вестибулярного анализатора.
У всех пациентов обоих групп в декретированные сроки спонтанный нистагм не регистрировался. Исследование проводилось в темноте с применением модуль Interacoustics VN 415B в течение 80 с в очках с комплектом инфракрасных камер (рис. 1).
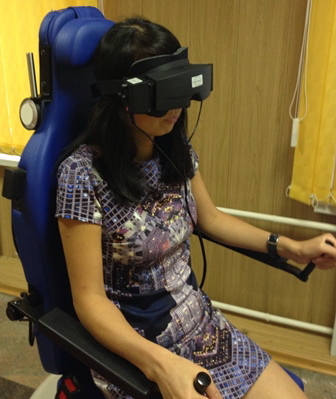
Рис. 1. Исследование пациента Б. 25 лет. Диагноз: хроническая двусторонняя сенсоневральная тугоухость IV степени.
У 9 из 30 пациентов исследуемой группы (30,0%), в калорическом и вращательном тесте была зарегистрирована двусторонняя арефлексия или гипорефлексия. При проведении калорического теста использовался холодовой (19ºС) и тепловой (45ºС) стимулы. При проведении исследования жалоб пациенты не предъявляли, исследование перенесли удовлетворительно.
Двое из 30 пациентов (6,6 %) первой группы не имели динамики в калорическом и вращательном тесте после проведения КИ в первые сутки и через месяц. У 5 пациентов (16,6%) в раннем послеоперационном периоде отмечались симптомы головокружения, тошнота. Результаты реакции спонтанного нистагма до имплантации и после были неизменными у всех 30 пациентов, статистически значимых изменений не выявлено.
Сила и фаза вызванного нистагма в маятниковом тесте у пациентов первой группы до и после проведения КИ имели статистически значимые отличия (15,1% (12-18%) и (76,6º (74-82º); в сравнении с результатами, полученными у пациентов группы контроля (40,1% (39-45%) и (2,80 (-5 - 4) соответственно; (p<0,01).
Изменений в значениях симметричности нистагма у пациентов первой группы до и после КИ не отмечено в сравнении с группой контроля (2,6% (-1-5%); (p>0,01). Однако выявлены статистически значимые отклонения (p<0,01) в значениях симметричности нистагма у пациентов первой группы с хронической двусторонней сенсоневральной тугоухостью до и после проведения КИ.
У первой группы пациентов, по сравнению с контрольной, выявлены достоверные различия средних значений разброса площади статокинезиограммы и коэффициента Ромберга (p<0,05).
При проведении анализа показателей постурографии выявлены статистически значимые различия стабильности в позе Ромберга до проведения КИ как в положении «глаза открыты» (37,2 (16,2-69,9), так и в положении «глаза закрыты» (23,2 (5,9-47,3) в сравнении с данными, регистрируемыми в течение первой недели после КИ в положении «глаза открыты» (34,4 (14,0-57,6) и «глаза закрыты» (19,5 (7,6-46,1); (р<0,05). В раннем послеоперационном периоде у пациентов с вестибулярным синдромом отмечается улучшение значений стабильности в положении «глаза открыты», что свидетельствует о визуальном компенсационном механизме. Степень выраженности изменений находится в обратной зависимости от срока наблюдения.
Таблица 2. Средние значения площади, коэффициента Ромберга и стабильности статокинезиограммы больных первой группы
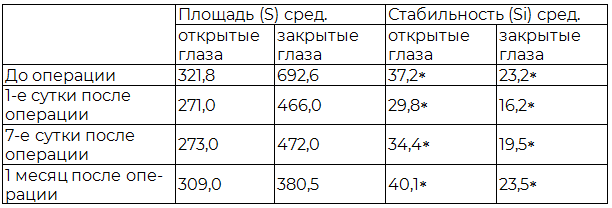
Примечание: * различия статистически значимые при p<0,05.
Выводы:
1. Вестибулярный синдром является общим осложнением КИ в раннем послеоперационном периоде, встречается в 16,6% и характеризуется снижением чувствительности периферического вестибулярного анализатора на стороне имплантации. Пациенты с высоким риском развития раннего послеоперационного вестибулярного синдрома могут быть выявлены до хирургического вмешательства.
2. Послеоперационное головокружение реже наблюдается у пациентов имеющих до хирургического вмешательства симптомы гипорефлексии либо арефлексии лабиринта, чем у пациентов с сохранными функциями вестибулярного анализатора. Таким образом, предоперационное тестирование вестибулярного анализатора помогает прогнозировать течение послеоперационного периода в отношении частоты развития головокружений.
3. В случае возникновения периферического вестибулярного синдрома в раннем послеоперационном периоде, важную роль в реабилитации играет визуальный компенсационный механизм.
