Введение. Анализ современной литературы показывает, что разработка средств и методов повышения эффективности лечения пациентов с хроническим гнойным средним отитом остается одной из главных задач современной отиатрии [4, 9, 15, 16, 18, 20]. Многолетний опыт хирургического лечения ХГСО доказывает высокую эффективность и необходимость его выполнения для достижении стойкого клинического эффекта у всех пациентов с данной патологией, вне зависимости от характера и распространённости патологического процесса в среднем ухе [10, 13, 14, 22]. К тому же, успехи в разработке реконструктивных методов хирургического вмешательства также позволяют производить коррекцию тугоухости обусловленной последствиями патологического процесса в среднем ухе. Однако, несмотря на достигнутые успехи, ряд вопросов совершенствования и оптимизации методов данных операций остаются открытыми. В частности, среди реконструктивных операций для достижения стойкого клинического эффекта и улучшения слуха пациента особое значение имеют тимпанопластика и ее заключительный этап - мирингопластика. Несмотря на накопленный опыт и современные возможности их выполнения неудовлетворительные результаты в случае обширных, тотальных и субтотальных, перфораций барабанной перепонки составляют от 10,8 до 28,6% [1, 7]. Большая часть неудовлетворительных результатов представлена реперфорациями, западением или провисанием трансплантата в барабанную полость, латерализацией неотимпанальной мембраны или притуплением переднего меатотимпанального угла, развитием в послеоперационном периоде спаечного процесса в барабанной полости [6, 8, 21, 27, 33].
Высокая частота наблюдаемости и необходимость выполнения повторных операций для устранения перечисленных осложнений обуславливают важность разработки методов профилактики их развития. Одной из главных причин развития перечисленных осложнений является нестабильность позиции трансплантата в первично заданном положении на ранних послеоперационных сроках [8, 15, 1, 24]. В свою очередь нестабильность положения определяется как недостаточной надежностью фиксации трансплантата, так и отсутствием для него надежной опоры, преимущественно в передних отделах барабанного кольца. Для решения вопроса стабилизации положения трансплантата предложено множество различных методов и средств дополнительно фиксирующих трансплантат как с внешней, так и внутренней сторон [12, 3, 2, 5, 26]. Однако, отдаленные результаты их применения выявили ряд недостатков, среди основных из которых развитие подобных осложнений: реперфорации, развитие спаечного процесса в барабанной полости, недостаточная функциональность вновь созданной барабанной перепонки [8, 34]. В связи с чем в последние годы актуальным представляется разработка различных видов и конфигураций самих трансплантатов, за счет собственных свойств которых обеспечивается их необходимая стабильность положения [19, 25, 28, 32]. Тем не менее, данные способы также не всегда являются успешными. Одним из их недостатков, по нашему мнению, является трудоемкость формирования и техническая сложность укладки. Наиболее сложным, в техническом аспекте, остается фиксации трансплантата в передних отделах барабанного кольца [11, 29, 30, 31].
Цель: повышение эффективности хирургического лечения пациентов с ХГСО при субтотальных дефектах барабанной перепонки.
Материалы и методы исследования.
Нами было проведено обследование и хирургическое лечение 74 пациентов с ХГСО в возрасте от 15 до 68 лет. В исследование включены 31 (41,9%) мужчина и 43 (58,1%) женщины. Критериями включения в группы исследования явились: наличие субтотального дефекта барабанной перепонки (в том числе и у части больных с неудовлетворительным клинико-анатомическим результатом ранее выполненной тимпанопластики при обширном центральном дефекте барабанной перепонки), целостность цепи слуховых косточек. Из исследования исключены больные с эпитимпаноантральной формой ХГСО и наличием деструктивных изменений цепи слуховых косточек.
Пациенты были разделены на 2 однотипные клинические группы. Первую (основную) группу составили 37 пациентов восстановление целостности барабанной перепонки которым произведено по разработанной методике с использованием хондро-перихондриального трансплантата с хрящевым компонентом подковообразной формы. Во контрольной (второй) группе (37 пациентов) восстановление целостности барабанной перепонки выполнено цельным хондро-перихондриальным трансплантатом.
Из 74 пациентов 11 ранее была произведена мирингопластика обширного центрального дефекта барабанной перепонки, данные пациенты включены в исследование по причине несостоятельности неотимпанальной мембраны от ранее выполненной операции. В основной группе таких больных было 9 (24,3%), в контрольной - 2 (5,4%).
При исследовании вентиляционной функции слуховой трубы получены следующие результаты: I степень вентиляционной функции была выявлена у 49 (66,2%) больных, II степень - у 23 (31,1%) больных, III степень - у 2 (2,7%) больных, IV степень не выявлена.
Интраоперационно у 9 (12,2%) пациентов исследуемых групп была обнаружена тугоподвижность цепи слуховых косточек. В основной группе больных с тугоподвижностью цепи слуховых косточек было 4 (10,8%), в контрольной - 5 (13,5%).
У большинства исследуемых больных состояние слизистой оболочки барабанной полости составляло норму - 46 (62,2%) пациента, мукозит I степени был выявлен у 20 (27,0%), II степень у 8 (10,8%) больных, III степень не выявлена.
На дооперационном этапе в I группе больных несколько преобладало количество пациентов с I степенью тугоухости, которых было 17 (46,0 %), II степень была диагностирована у 14 (37,8%) больных. Число пациентов с III и IV степенью тугоухости было минимальным, 2 (5,4%) и 2 (5,4%) соответственно. Больных с нормальным слухом было 2 (5,4%), у данных пациентов была ранее выполнена тимпанопластика оперируемого уха.Во II группе больных в зависимости от степени тугоухости, до хирургического вмешательства, пациенты распределились следующим образом. С I степенью тугоухости было 19 (51,4%) больных, со II - 14 (37,8%), с III- 4 (10,8%), пациентов с нормальным слухом и с IV степенью тугоухости не было.
По показателю КВИ на дооперационном этапе большую часть в обеих клинических группах - 40 человек (54,0%) составили пациенты с КВИ в пределах от 21 до 30 дБ. Меньший процент распределялся на пациентов со средним значением КВИ от 11 до 20 дБ - 15 (20,3%) больных и от 31 до 40 дБ - 13 (17,6%) больных.
Статистически достоверной разницы между клиническими группами больных по форме (p=0,485, метод χ2), степеням тугоухости (p=0,311, критерий Манна-Уитни), а также значениям костно-воздушного интервала (p=0,940, критерий Манна-Уитни) на дооперационном этапе не выявлено.
Статистический анализ данных выполнялся с использованием пакета программ Statistica 6.1 (StatSoft, Inc., США) в соответствии с рекомендациями О.Ю. Ребровой [17]. Для сравнения связанных групп по количественным признакам применялся критерий Вилкоксона, а для сравнения несвязанных групп выполнялся непараметрический анализ по Манну-Уитни. Сравнение групп по качественным признакам проводилось с использованием теста χ2. При проверке гипотез статистически значимыми различия результатов считались при достигнутом уровне значимости р<0,05.
Состояние неотимпанальной мембраны в послеоперационном периоде оценивалось путем стандартной отоскопии и с помощью микроскопа (отомикроскопия). Тональную пороговую аудиометрию проводили с использованием аудиометра клинического Interacoustic AD 229е (Дания) с определением порогов слуха по воздушному и костному проведению на частотах 128 - 8000 Гц.
Методики хирургического вмешательства. Хирургическое вмешательство производили под контролем операционных микроскопов Carl Zeiss Senseria (Германия) или Carl Zeiss OPMI Sensera (Германия), микрохирургическим инструментарием фирмы Karl Storz (Германия). В большинстве случаев (49 пациентов) операцию проводили под местной инфильтрационной анестезией. У всех пациентов использовался заушный хирургический доступ. После деэпителизации краев перфорации, формирования меатотимпанального лоскута, оценки состояния слизистой оболочки барабанной полости, целостности и функциональности цепи слуховых косточек приступали непосредственно к забору пластического материала и формированию неотимпанальной мембраны. В качестве источника пластического материала у всех пациентов использовался аутохрящ ушной раковины, забор необходимого объёма которого производился стандартным способом.
Пациентам II (контрольной) группы закрытие дефекта барабанной перепонки производилось стандартным способом - укладкой предварительно истонченной цельной хондро-перихондриальной пластины непосредственно под остатки барабанной перепонки, на рукоятку молоточка. Использование данного способа сохраняет определенные риски смещения трансплантата в передних отделах ввиду отсутствия необходимой для него опоры. Учитывая это нами был разработан новый способ формирования неотимпанальной мембраны. В качестве источника пластического материала нами так же, как и при первом способе использовалась цельная хондро-перихондриальная пластина. С оголенной стороны которой, по средней линии, проводили разрез скальпелем через всю толщину хряща, не травмируя надхрящницу покрывающую его с другой стороны. Одну половину хряща удаляли, другой придавали подковообразную форму (рис. 1).
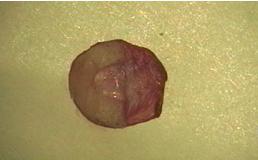
Рис. 1. Хондро-перихондриальный трансплантат с хрящевым компонентом подковообразной формы.
Для повышения степени контакта хрящевого компонента в передних отделах барабанного кольца производили отсепаровку слизистой оболочки барабанной полости от фиброзного кольца. Данное место в дальнейшем служило ложем для хрящевого компонента трансплантата. Выпуклой стороной хрящевого компонента подводили сформированный трансплантат в область ранее сформированного ложа, при этом надхрящничный компонент трансплантата располагался снаружи, а ветви хрящевого компонента располагались кпереди от молоточка не касаясь его. За счет формы и эластичности хрящевого компонента трансплантата его ветви играли роль распорки, фиксируя его между верхней и нижней стенки костного кольца. Надхрящница укладывалась на рукоятку молоточка и частично заднюю стенку наружного слухового прохода. Меатотимпанальный лоскут укладывался в исходное положение.
При проведении реопераций по причине несостоятельности неотимпанальной мембраны (западение неотимпанального трансплантата) производили отсепаровку ранее установленного трансплантата от остатков барабанной перепонки с рассечением рубцов. Производили оценку состояния слизистой оболочки барабанной полости и тимпанального устья слуховой трубы, целостности и подвижности цепи слуховых косточек, передачу механических колебаний на вторичную мембрану окна улитки. При необходимости удаляли верхне-латеральный отдел задней стенки наружного слухового прохода (навес над стременем) до полной визуализации всех структур ниши окна преддверия.
В обоих случаях хирургическое вмешательство завершали контролем уровня положения неотимпанального трансплантата на предмет полноценности закрытия дефекта барабанной перепонки, укладкой полосок латексной резины на меатотимпанальный лоскут, тампонадой наружного слухового прохода тампонам пропитанными раствором антибиотика широкого спектра действия (Цефтриаксон), ушиванием послеоперационной раны и накладыванием наружной асептической повязки. В послеоперационном периоде для предупреждения осложнений все пациенты обеих клинических групп получали антибактериальную и десенсибилизирующую терапии. Швы после операции удаляли на 7 - 8 сутки, тампоны из наружного слухового прохода на 21 сутки.
Результаты хирургического лечения и их обсуждение.
Оценку результатов хирургического лечения осуществляли по анатомическим и функциональным показателям.
Анатомические результаты выполненных операций оценивали через 1, 3, 6, 9 и 12 месяцев после выполненной операции. Условно, анатомические результаты нами расценивались как отличные и неудовлетворительные. Отличными считались результаты при отсутствии реперфораций, отклонений вновь созданной барабанной перепонки от первично заданного положения, таким образом состоятельной, подвижной и находящейся в «естественном» положении неотимпанальной мембраны. Неудовлетворительными, соответственно, считались результаты при наличии реперфорации и/или отклонении трансплантата от первично заданного положения в различных отделах.
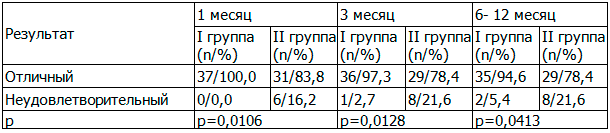
На момент удаления тампонов из наружного слухового прохода у 37 (100%) имелся отличный результат, результатов не было. В контрольной группе у 6 (16,2%) пациентов имелся неудовлетворительный результат - в передних отделах неотимпанальной мембраны обнаружены различной обширности щелевидные дефекты. На 3 месяц контрольного наблюдения в основной группе пациентов неудовлетворительный результат имелся у 1 (2,7%) пациента, в контрольной группе у 8 (21,6%). К 6 месяцу наблюдения в основной группе неудовлетворительные результаты имелись у 2 (5,4%) пациентов - в нижних отделах неотимпанальной мембраны имелись щелевидные дефекты, во II (контрольной) группе число пациентов с неудовлетворительным результатом оставалось прежним - 8 (21,6%) с учетом 6 (16,2%) у которых таковые были выявлены ранее. Число пациентов с неудовлетворительными результатами в I и II группах на 9 и 12 месяцы контрольного наблюдения было неизменным, 2 (5,4%) и 8 (21,6%) больных соответственно (таб. 1).
Таблица 1. Анатомические результаты пациентов I и II клинических групп в сроки 1, 3, 6, 9 и 12 месяцы после операции
Через год после операции в I группе больных, с использованием хондро-перихондриального трансплантата с хрящевым компонентом подковообразной формы, внешний вид неотимпанальной мембраны приобрел характерные черты: цвет ее был близким к таковому естественной барабанной перепонки, у некоторых пациентов неотимпанальная мембрана была несколько мутноватой. У всех больных в передних отделах неотимпанальной мембраны четко контурировался хрящевой, подковообразный, компонент трансплантата. В II группе больных, у пациентов с состоятельной неотимпанальной мембраной, внешний вид вновь сформированной барабанной перепонки был типичным - белого цвета пластина аутохряща.
Таким образом, к 12 месяцу наблюдения неудовлетворительные анатомические результаты лечения в I (основной) группе составили 5,4% (2 больных), отличные результаты достигнуты у 94,6% (35 пациентов). Во II группе соответственно - 21,6% (8 больных) и 78,4% (29 пациентов).
При проведении сравнительного анализа анатомических результатов исследуемых групп больных на 1, 3 и 12 месяцы наблюдения по методу χ2 получены статистически достоверные различия (p1=0,0106, p3=0,0128, p12=0,0413).
Анализируя неудовлетворительные клинико-анатомические результаты у пациентов I (основной) группы главной причиной недостаточной эффективности выполненного хирургического вмешательства, по нашему мнению, было недостаточное подведение надхрящничного компонента трансплантата под меатотимпанальный лоскут в нижних отделах, что в свою очередь не обеспечило его должной фиксации и необходимого кровоснабжения. Также, среди причинных факторов следует учитывать послеоперационную рубцовую ретракцию надхрящницы. Во II группе неудовлетворительные результаты мы связываем с отсутствием опоры для трансплантата в передних отделах барабанного кольца.
В качестве основного метода оценки функциональной эффективности выполненных операций нами использовалась тональная пороговая аудиометрия, с помощью которой определялись: степень тугоухости по международной классификации ВОЗ (1997) и величина резидуального костно-воздушного интервала на частотах 500 - 4000 Гц.
Оценивая полученные данные показателей тональной пороговой аудиометрии через 1 год после операции можно сделать вывод о том, что в обеих исследуемых группах в послеоперационном периоде произошло улучшение показателей звукопроведения по воздуху.
К 12 месяцу послеоперационного наблюдения процент пациентов с нормальным слухом несколько преобладал в I (основной) группе (67,6%), во II (контрольной) группе он составил 59,5%. Число пациентов с I степенью тугоухости преобладало во II клинической группе и составило 11 (29,7%) больных, в то время как в I группе их было 7 (18,9%). Статистически достоверная разница между клиническими группами по динамике изменения степени тугоухости получена только на 3 месяце наблюдения (p=0,048, критерий Манна-Уитни).
Безусловно, уровень тонального звукопроведения, по которому определяется степень тугоухости, играет немаловажную роль в восприятии больным звука. Однако, в первую очередь о функциональной эффективности оперативного вмешательства свидетельствует уменьшение костно-воздушного интервала. Проводя анализ функциональных результатов, мы учитывали сокращение костно-воздушного интервала через 3, 6, 9 и 12 месяцев после операции. В качестве градации эффективности функционального результата по костно-воздушному интервалу нами, условно, была выбрана следующая шкала результатов:
- «Отличный» - костно-воздушный интервал в пределах 10 дБ;
- «Хороший» - костно-воздушный интервал в пределах 11 - 20 дБ;
- «Удовлетворительный» - интервал в пределах от 21 до 30 дБ;
- «Неудовлетворительный» - костно-воздушный интервал более 30 дБ
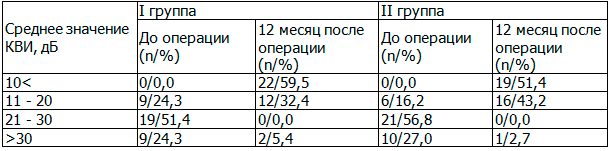
При оценке остаточного КВИ (табл. 2), как основного показателя функциональной эффективности операции, у большинства больных, 59,5% (22 больных) в основной и 51,4% (19 больных) в контрольной, к 12 месяцу достигнут отличный результат - сокращение КВИ до 10 дБ. Хороший результат (остаточный КВИ от 11 до 20 дБ) достигнут у 12 (32,43%) больных в I и у 16 (43,24%) во II группах. Однако, по сравнению с контрольной, в основной группе сокращение КВИ до 10 дБ наблюдалось в более ранние сроки - 3 месяца. Хотя в дальнейшем (6 - 12 месяц наблюдение) соотношение больных между группами с данным показателем было практически одинаковым. Вероятнее всего это может быть объяснено несколько большей жесткостью на первоначальном этапе и толщиной цельного хондро-перихондриального трансплантата по сравнению с надхрящницей, использованной в качестве основного материала формирующего неотимпанальную мембрану у пациентов I группы. В дальнейшем хрящевой компонент цельного хондро-перихондриального трансплантат, вероятнее всего, несколько теряет свою жесткость и становится более пластичным, о чем, хотя и косвенно, могут свидетельствовать полученные нами функциональные результаты во II группе больных. Отсутствие значимого изменения КВИ у части больных, 2 (5,4%) в I и 1 (2,7%) во II группах, было обусловлено выраженной тугоподвижностью цепи слуховых косточек из-за имевшегося тимпаносклероза, что в свою очередь не позволило нам выполнить необходимое хирургического вмешательства на первом этапе операции.
Таблица 2. Распределение больных в клинических группах в зависимости от среднего значения КВИ на дооперационном этапе и 12 месяце после операции
Несмотря на преобладание неудовлетворительных анатомических результатов операции во второй клинической группе приведенные результаты свидетельствуют о достигнутом высоком функциональном результате у пациентов обеих клинических групп. Данное обстоятельство может быть объяснено тем, что реперфорации у пациентов во второй группе локализовались в передних отделах барабанного кольца и были в основном щелевидными и, как следствие, в меньшей степени влияли на слух пациента.
Вывод. Разработанный метод формирования неотимпанальной мембраны при субтотальных дефектах барабанной перепонки хондро-перихондриальным аутотрансплантатом с хрящевым компонентом подковообразной формы позволяет надежно фиксировать его к передним отделам костного анулюса и внутренней поверхности фиброзного кольца, полноценно восполнить обширные дефекты барабанной перепонки и значительно повысить эффективность хирургического лечения пациентов с ХГСО, что подтверждено полученными достаточно высокими анатомическими (94,6%) и функциональными (59,5%) результатами в ближайшем и отдаленном периодах у больных основной группы.
