Торакоскопия широко используется при лечении эмпием плевры [2, 3, 9-12]. Однако исследований, посвященных применению торакоскопии при ограниченных эмпиемах плевры мало, тогда как использование торакоскопии у таких больных сопряжено с рядом трудностей. Это обусловлено тем, что хирург осуществляет свои действия в узком, неправильной щелевидной формы пространстве, часто не имея возможности использовать дополнительный манипулятор.
Нередко при ограниченных эмпиемах плевры нагноение захватывает реберно-диафрагмальный синус, распространяясь вверх по реберной плевре. Большинство авторов относит такие нагноения к базальным эмпиемам плевры, хотя в классическом понимании термином «базальная» эмпиема называют эмпиему, прилежащую только к диафрагмальной плевре. Некоторые авторы для обозначения таких эмпием плевры используют термин косто-диафрагмальные, выделяя их в отдельную группу [5]. Для простоты понимания в нашей работе эти эмпиемы мы будем называть «базальные».
Несмотря на относительно малые размеры нагноения при таких эмпиемах плевры возможно, как и при любых других, формирование тяжелых септических осложнений, хронических эмпием плевры. Отличает такую локализацию эмпием то, что их следствием может становиться формирование адгезивного плеврита в проекции реберно-диафрагмального синуса. Адгезия в проекции синуса приводит к сращению диафрагмальной и реберной плевр, что ограничивает подвижность диафрагмы, приводит к уменьшению резервного объема плевральной полости, что отрицательно влияет на функцию дыхания.
Целью нашего исследования стала разработка оптимизированной методики выполнения торакоскопического доступа и санации эмпиемной полости у больных базальной эмпиемой плевры.
Материалы и методы. За период 2000-2012 г. в отделении торакальной хирургии городской клинической больницы №4 г. Перми проходили лечение 102 пациента с базальными эмпиемами плевры. Пациентам обеих групп в день поступления выполнялась торакоскопия. В зависимости от техники выполнения торакоскопической санации всех пациентов разделили на 2 группы.
В I группу вошли 47 больных с острыми эмпиемами плевры, которым в процессе лечения использовали разработанную нами оптимизированную методику выполнения торакоскопического доступа и санации эмпиемной полости.
Во II группу вошли 55 человек, проходивших лечение в период, когда методика находилась на стадии разработки.
В до- и послеоперационном периоде лечение больных обеих групп было идентичным. Пациентам применяли инфузионную терапию, антибактериальную терапию с подбором препарата по чувствительности к антибиотикам, современные методы детоксикации. Проводились промывания эмпиемной полости растворами антисептиков, пассивная и активная аспирация по показаниям. У 2-х больных при наличии более чем стойкого трехдневного коллапса легкого и значительном сбросе воздуха по дренажу использовали временную окклюзию несущего свищ бронха.
Проведя анализ медицинской документации и результатов лечения больных II группы, мы выявили факторы, которые приводят к ухудшению результатов лечения базальных эмпием плевры [9]:
- плохая санация эмпиемной полости, оставление в синусе гнойно-некротических секвестров и фибринозных фрагментов;
- неадекватное дренирование, при котором не обеспечивается своевременная эвакуация вновь образующегося экссудата из гнойной полости, происходит его застой и, как следствие, формирование сращений.
Общепризнанно, что повысить качество выполнения оперативного приема позволяет использование рационального оперативного доступа [6, 7]. Правильно выполненный оперативный доступ должен обеспечить возможность хирургу свободно достигать все отделы полости нагноения и адекватно санировать полость гнойника. Доступом при оперативной торакоскопии является торакоцентез, поэтому мы решили найти такое место для выполнения торакоцентеза, которое позволит хирургу свободно манипулировать во всех отделах полости базальной эмпиемы плевры.
Для определения оптимальных мест выполнения торакоскопического доступа и дренирования мы провели анатомический эксперимент. Исследование выполнили на 75 трупах взрослых людей зрелого возраста. Экспериментальный материал был разделен по типам телосложения и форме грудной клетки по В.Н. Шевкуненко и А.М. Геселевичу (1938): 25 объектов исследования с долихоморфным типом телосложения, 25 – с мезоморфным и 25 – с брахиморфным [8].
Оценку хирургического доступа проводили по методике А.Ю. Созон-Ярошевича (1954) с учетом особенностей эндоскопических технологий [7].
Первым этапом нашего исследования мы выявили место, из которого обеспечивается наилучшая хирургическая доступность при проведении эндоскопической санации реберно-диафрагмального плеврального синуса. В эндоскопии наилучшим для проведения лечебных манипуляций считается такое место выполнения эндоскопического доступа, расстояние от которого до места воздействия (глубина раны) равна половине длины дистанционного манипулятора (то есть 17,5 см при стандартной длине манипулятора в 35 см). При таком расстоянии уравновешивается воздействие рук хирурга с воздействием на ткани рабочей части инструмента [6]. При выполнении санационных мероприятий у больных базальной эмпиемой плевры местом проведения хирургичеих манипуляций является вся площадь реберно-диафрагмального плеврального синуса. Хирург должен иметь возможность свободно манипулировать в наиболее удаленных участках реберно-диафрагмального синуса – в его переднем и заднем отделах. В этой связи, наилучшим для выполнения торакоскопического оперативного доступа – торакоцентеза определяли точку, расстояние от которой до переднего и заднего окончаний реберно-диафрагмального синуса максимально приближалось к оптимальному операционному расстоянию в 17,5 см.
Мы провели сравнительную топографо-анатомическую оценку торакоцентезов, выполненных в IV, V, VI, VII, VIII и IX межреберьях по подмышечным линиям. Исследовали глубину операционной раны по отношению к переднему и заднему окончаниям реберно-диафрагмального синуса.
Проведенные исследования показали, что оптимальными параметрами оперативной доступности для обеспечения наилучших условий санации реберно-диафрагмального плеврального синуса обладают следующие участки грудной стенки:
- у пациентов с долихоморфным типом телосложения справа 5 межреберье по средней подмышечной линии (глубина раны относительно переднего окончания реберно-диафрагмального синуса (ГРОПОРДС) 17,0±0,15 см, глубина раны относительно заднего окончания реберно-диафрагмального синуса (ГРОЗОРДС) – 18,3±0,23 см) и 6 межреберье по задней подмышечной линии (ГРОПОРДС – 17,2±0,2, ГРОЗОРДС – 15,8±0,27); слева – 5 межреберье по задней подмышечной линии (ГРОПОРДС – 15,77±0,18 см, ГРОЗОРДС – 17,2±0,2 см).
- у пациентов с мезоморфным типом телосложения справа – 6 межреберье по средней подмышечной линии (ГРОПОРДС – 16,9±0,16 см, ГРОЗОРДС – 16,2±0,16 см) и 6 межреберье по задней подмышечной линии (ГРОПОРДС – 19,44±0,18 см, ГРОЗОРДС – 16,5±0,26 см); слева – 5 межреберье по задней подмышечной линии (ГРОПОРДС – 17,01±0,14 см, ГРОЗОРДС – 19,3±0,15 см) и 6 межреберье по задней подмышечной линии (ГРОПОРДС 14,43±0,15 см, ГРОЗОРДС – 16,3±0,23 см).
- у пациентов с брахиморфным типом телосложения справа – 6 межреберье по средней подмышечной линии (ГРОПОРДС 17,5±0,2 см, ГРОЗОРДС – 18,2±0,16 см); слева – 5 межреберье по задней подмышечной линии (ГРОПОРДС – 17,6±0,17 см, ГРОЗОРДС – 20,6±0,18 см) и 6 межреберье по задней подмышечной линии (ГРОПОРДС 14,9±0,13 см, ГРОЗОРДС – 17,5±0,21 см).
Следующим направлением нашего исследования стал поиск мест для наиболее эффективного дренирования эмпиемной полости. Опыт многих исследователей показывает, что дренаж должен быть не менее 10 мм в диаметре, что обеспечивает его постоянную проходимость [4]. Мы изучили ширину межреберий. Выявили, что дорсальнее лопаточной линии введение дренажа в плевральную полость становится малоэффективным, так как ширина межреберий в этом месте сужается до критической величины – меньше 10 мм у представителей всех типов телосложения.
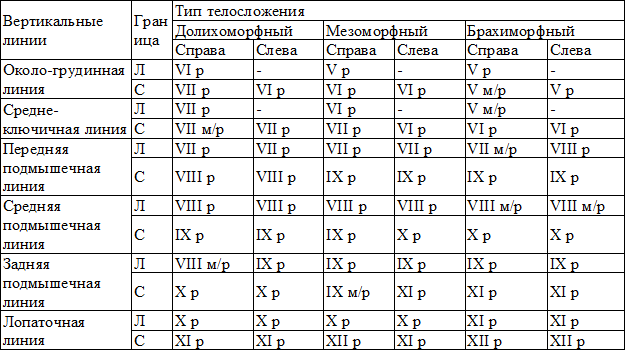
Исходили из того, что для наиболее эффективного дренирования дренаж должен быть расположен в наиболее низких отделах эмпиемной полости. Применительно к базальным эмпиемам – дренаж должен быть в наиболее низко расположенных отделах реберно-диафрагмального плеврального синуса. Мы изучили параметры реберно-диафрагмального синуса у людей различных типов телосложения (таблица 1). Выявлено, что средние отделы синуса имеют схожую топографию при всех типах телосложения. Поэтому при затруднениях в определении типа телосложения больного дренирование можно осуществлять в 8 межреберье по средней подмышечной линии и в 9 межреберье по задней подмышечной линии.
Полученные результаты мы представили в виде схем с указанием мест предпочтительной постановки дренажа. Указанные схемы размещены в эндоскопической операционной для использования хирургами в качестве ориентиров при выполнении торакоскопии.
Таблица 1. Проекция нижних краев легкого (Л) и реберно-диафрагмального синуса (С) на ребра (р) и межреберья (м/р) у пациентов различных типов телосложения
На основании данных анатомического исследования и опыте лечения больных II группы мы разработали стандартизированную трехэтапную методику выполнения оперативной торакоскопии у больных базальной эмпиемой плевры:
1 этап: После рентгенологической, а при необходимости и сонографической визуализации границ эмпиемы выполняется торакоцентез максимально приближенный к одной из определенных нами точек, обладающих оптимальными параметрами оперативной доступности для обеспечения наилучших условий санации реберно-диафрагмального плеврального синуса.
2 этап: Из первого торакоцентеза выполняется санация в монопортальном режиме в направлении задних отделов реберно-диафрагмального синуса, где проводится второй торакоцентез. Второй торакоцентез служит для введения эндоскопического манипулятора и для дренирования плевральной полости. Согласно результатам нашего исследования для эффективного дренирования плевральной полости торакоцетез должен быть расположен кпереди от лопаточной линии и в реберно-диафрагмальном синусе, согласно разработанным нами схемам, на 2-3 см выше диафрагмы. Через торакоцентез вводится эндоскопический манипулятор и санация продолжается в бипортальном режиме. Санация включает в себя удаление гнойно-некротических секвестров и фибринозных фрагментов, вскрытие осумкований гноя, разрушение разграничивающих осумкования сращений. Выполнение санации, вскрытие осумкований гноя инструментом введенным через второй торакоцентез обеспечивает беспрепятственное движение гноя в направлении второго торакоцентеза, а следовательно и дренажа в послеоперационном периоде.
3 этап – дренирование плевральной полости. При завершении санационных мероприятий через второй торакоцентез вводится дренаж в направлении от основания к верхушке эмпиемной полости. При наличии признаков массивного бронхо-плеврального свища и ригидного легкого устанавливается второй дренаж через первый тораоцентез (если позволяют размеры эмпиемной полости).
Указанную методику выполнения оперативной торакоскопии использовали в лечении пациентов I группы. Тип телосложения определяли по индексу телосложения (В.Н. Шевкуненко, А.М. Геселевич, 1938): длину туловища (расстояние от яремной вырезки грудины до лонного сочленения) поделить на длину тела (рост) и умножить на 100 [8]. Если полученный в результате вычисления индекс меньше 29 – тип телосложения долихоморфный, 29-31 – мезоморфный, более 31 – брахиморфный. Указанные размеры вычисляли с помощью линейки, прикрепленной к краю операционного стола. Для оценки эффективности предложенной нами методики сравнили результаты лечения больных обеих групп.
Средняя длительность госпитализации больных в I группе составила 27,76±1,2 койко-дней, во II группе – 31,56±2,1 койко-день.
В I группе выздоровели 46 (97,9%) из 47 (100%) пациентов. Исходов в хроническую эмпиему плевры в I группе не было. Умер 1 (2,1%) пациент. Во II группе выздоровели 46 (83,6%) из 55 (100%) больных. Хроническая эмпиема плевры сформировалась у 5 (9,1%) больных. Умерло 4 (7,3%) пациента.
Сравнили количество исходов в адгезивный плеврит. В I группе выраженный адгезивный плеврит наблюдали в 1 (2,1%) случае, умеренно выраженный в 4 (8,5%) случаях. Во II группе выраженный адгезивный плеврит наблюдали в 5 (9,1%) случаях, умеренно выраженный – в 12 (21,8%) случаях. Как видно из приведенных данных, достигнута отчетливая положительная динамика.
Таким образом, стандартизация методики торакоскопии позволила улучшить результаты лечения больных базальными эмпиемами плевры.
