Актуальность. В последнее десятилетие интерес к проблеме гипермобильности суставов (ГМС) заметно возрос. Внимание исследователей направлено на изучение проблемы модифицирующего влияния данной патологии на риск возникновения и характер суставных заболеваний, среди которых лидирующее место занимает остеоартроз (ОА). ГМС чаще встречается среди женщин и детей, что свидетельствует о возможной роли гормональных факторов в ее этиологии [1]. Распространенность ГМС по литературным данным варьирует от 2% до 57% в зависимости от возраста, пола, расовой принадлежности обследуемых [2]. ГМС определяется как состояние, при котором амплитуда активных и/или пассивных движений в суставах превышает условную среднестатистическую норму [3]. Она имеет склонность к семейной агрегации с различным типом наследования (аутосомно-доминантным, аутосомно-рецессивным или Х-сцепленным доминантным), большей частью по женской линии [5].
Анализ родословных свидетельствует о наличии в одной родословной (при обследовании и по анамнестическим данным) родственников с ГМС, а также негипермобильных «носителей» [6]. J. Simmonds и R. Keer сообщили, что от 27% до 65% их пациентов сообщили о родственниках с ГМС. Даже если они не знали о ГМС у своих родственников, то другие дополнительные сведения, такие как, вывихи, растяжения связок, ОА указывали на наличие у них этого состояния [5].
К настоящему времени накоплены факты, показывающие связь ГМС и «суставных» заболеваний. ГМС считается фактором риска для ОА, хотя исследования имеют противоречивые результаты. Большинство авторов придерживаются мнения, что ГМС является фактором риска для развития ОА, который развивается у представителей этой категории чаще и раньше, чем в общей популяции [6, 7].
Несколько семейных исследований посвящены взаимосвязи ОА и ГМС [6-8]. J. Martin и E. Ives сообщили о двух родных братьях и сестре с семейной ГМС и ОА ладьевидно-трапецио-трапециевидного и ладьевидно-трапециевидного сустава [8].
F. Schilling наблюдал семью с членами I и II степени родства (n=28), в которой в каждом поколении отмечалась ГМС, приводящая к раннему ОА, и у одного члена семьи это потребовало эндопротезирование суставов [6].
Семейное исследование пациентов с ОА кистей (n=1839), проведенное H. Jonsson установило связь ГМС с маркером D19S591 на хромосоме 19р13.3. Интересно, что два гена, предположительно влияющих на возникновение ГМС (FBN3 и COL5A3), располагаются в пределах 5 и 7 Mb от этого маркера [9].
Развитие ОА при ГМС может быть обусловлено особенностями биомеханики движений в суставе с избыточным объемом движений и характером генетических мутаций [10, 11].
Генетическая теория, согласно которой ГМС может привести к ранним дегенеративным изменениям хряща следующая: ген, предрасполагающий к ГМС, по-видимому, определяет и предрасположенность к ОА [10]. Из этого следует, что ГМС является фенотипическим маркером определенного генотипа, который предрасполагает к преждевременному возникновению ОА.
Следует отметить, что как при ГМС, так и при ОА обнаруживается накопление таких дефектов опорно-двигательного аппарата, как сколиоз, плоскостопие, кифоз, спондилолистез/спондилез и др. [10]. Это свидетельствует о возможной этиологической общности ГМС и ОА, что подтверждает генетическую теорию.
Генетическая природа заболевания отнюдь не исключает значения внешних факторов. Наряду с конституционными факторами на развитие ОА при ГМС оказывает влияние уровень физической активности [11].
Таким образом, многие ученые склоняются к тому, что одна только ГМС не может вызывать возникновение ОА, а другие ко-факторы, такие как пол, возраст, тип конституции, малоподвижный образ жизни или наоборот чрезмерная нагрузка на суставы (занятия спортом, тяжелый труд), травмы, операции на суставах предрасполагают к развитию преждевременного ОА, могут быть важными «провокаторами» симптомов и результатом исхода ГМС в ОА [10].
Следовательно, можно предположить два патогенных фактора, трансформирующих ГМС в ОА. С одной стороны, патологическая структура хряща может приводить к первичному ОА, и, с другой стороны, биомеханика нестабильности суставов и нарушение суставной проприоцепции приводят к постоянной микротравматизации, являющейся пусковым фактором развития ОА.
Цель исследования – определить тип наследования ГМС и проанализировать данные о частоте, тяжести течения ОА у пациентов с семейной ГМС.
Материалы и методы. За период с 2009 по 2014 г. проведено генеалогическое исследование пробандов (n=61) с ОА на фоне сопутствующей ГМС и 455 их родственников I, II, III степени родства. Группу контроля составили семьи 60 пробандов с ОА и 180 их родственников I, II, III cтепени родства без сопутствующей ГМС.
Критерии включения: 1) пациент с ГМС и документированным диагнозом ОА (I – IV рентгенологических стадий); 2) письменное информированное согласие пациента на участие в исследовании; 3) отягощённый семейный анамнез (наличие у родственников с ГМС и ОА).
Критерии исключения: 1) другие ревматические заболевания; 2) наличие в анамнезе травм или операций на суставах.
У всех пациентов существенное внимание уделяли сбору анамнеза, с акцентом на выявление в их семьях родственников с ОА и ГМС. Оценка состояния здоровья родственников пробанда базировалась на опросе и клиническом осмотре. Анализировались: степень родства с пробандом, пол и возраст. Проводилась регистрация сопутствующих заболеваний.
При анализе родословных выявляли общее число родственников, степень их родства с пробандом и среднее число поколений в родословной. К I степени кровного родства относились родители, дети, сибсы, ко II-й – дяди/тети, племянники/племянницы, бабушки/дедушки, внуки, полусибсы, к III-й – двоюродные сибсы (кузен, кузена). При составлении родословной придерживались общепринятых правил. Каждый член родословной имел свой символ и шифр, состоящий из двух цифр – римская обозначала номер поколения (поколения нумеровались сверху вниз, цифра ставилась слева от родословной), арабская – номер индивида при нумерации членов одного поколения последовательно слева направо. Братья и сестры располагались в родословной в порядке рождения. В тех случаях, когда супруг не был обследован на наличие рассматриваемых признаков, его родословная не анализировалась. Все индивиды располагались строго по поколениям в один ряд. Под родословной, которая охватывала не менее двух – трех поколений, помещалась легенда, содержащая пояснения к условно принятым обозначениям. Схематическое изображение родословной начиналось с пробанда, который помечался стрелкой, затем, с учетом последовательности беременностей и их исходов, собирались и обозначались сведения о детях пробанда и его сибсах. Далее собирались данные о кровных родственниках по линии матери: сначала все о матери пробанда, ее сибсах и их детях, затем все о бабушке по линии матери, ее сибсах и их детях и внуках и т.д. После этого в такой же последовательности собирались сведения о кровных родственниках по линии отца [14].
Поскольку в настоящее время приходится сталкиваться с родословными, включающими небольшое число членов, то для анализа такого материала все данные суммируют и проводят сегрегационный анализ.
Проверка гипотезы о моногенной рецессивной природе признака более сложная задача, чем проверка гипотезы о моногенном доминантном наследовании, т.к. возникает необходимость избежать погрешностей, вызванных особенностями сбора генеалогического материала. Источник этой погрешности заключается в вероятности непроявления признака в семье с небольшим числом детей, потому что в этом случае такая семья не попадет в поле зрения генетика. Такой отбор формирует смещенную выборку, и генетические показатели оказываются искаженными. Для того чтобы учесть погрешности, вызванные особенностями сбора материала, сегрегационные частоты (SF) рассчитывают по формуле «сибсового» метода М. Вайнберга (формула 1) [15]:
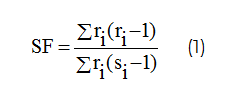
где SF – оценка сегрегационной частоты;
ri – количество пораженных детей у семей данного типа;
si – общее количество детей у семей данного типа с учетом пробанда.
Вычисленную сегрегационную частоту сравнивали с теоретически ожидаемой, используя t-критерий Стьюдента (формула 2):
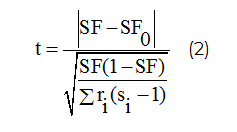
где SF – оценка сегрегационной частоты;
SFo– ожидаемое значение сегрегационной частоты: для аутосомно-рецессивного типа наследования – 0,25; для аутосомно-доминантного – 0,5.
Если значение t превышает величину 2,58, то для анализируемого заболевания гипотеза о соответствии определенному типу наследования отвергается.
Наследуемость предрасположенности к заболеванию (н²) определялась по модели Фальконер (нормальное распределение подверженности заболеванию в популяции и среди родственников I степени родства), которая постулирует следующее: если проявление генетической конституции индивида модифицируется средовыми условиями, «улучшая» или «ухудшая» его фенотип, то этот вклад можно включить в генотипическое значение как его часть. Коэффициент наследуемости принимает значения от 0 до 1 (или от 0 до 100%) и выражает вклад аддитивных генетических факторов в изучаемый фенотип. Другими словами, можно сказать, что наследуемость – это популяционный статистический параметр, который выражает генетический вклад в изучаемый признак в процентах. Низкое значение наследуемости подразумевает малый вклад аддитивно действующих генов в признак, тогда как высокое значение – большой вклад.
Существует соотношение между наследуемостью и теоретическим коэффициентом корреляции между родственниками. Согласно модели Фальконер, коэффициент регрессии подверженности рассчитывается по формуле 3 [16]:
b=Xq–Xr/a (3)
где Xq – пороговая точка распределения подверженности в популяции; Хr – пороговая точка распределения подверженности среди родственников; a – средняя величина подверженности больных в популяционной выборке.
Коэффициент наследуемости определяет вклад генетических факторов в развитие болезни при совместном действии генотипических и средовых факторов. Наследование признака оценивается как моногенное, если коэффициент наследуемости составляет 100% или как мультифакториальное (наследственно-средовое) при показателе менее 50%.
Коэффициент наследуемости (н²) вычислялся по формуле 4:
н² =b/r (4)
где r – мера родства, которая для родственников 1-й степени родства составляет 2.
Все семьи пробандов анализировались методом количественной оценки отягощенности генеалогического анамнеза с помощью показателя, называемого индексом отягощённости наследственного анамнеза (Jo), который рассчитывался по формуле 5:
Jo = общее число больных родственников, о заболеваниях которых есть сведения, включая пробанда / общее число родственников, о состоянии здоровья которых есть сведения, включая пробанда (5)
При значении индекса от 0–0,3 отягощенность генеалогического анамнеза расценивалась как благополучная, 0,3–0,6 – условно благополучная, > 0,6 – как неблагополучная [15].
Частота встречаемости ОА в семьях с ГМС, по нашим данным, составила 44,8% (204 больных родственника из 455 обследованных), что значительно превышает данные других исследователей, приводящих цифры от 6% до 26% [5-9]. Частота встречаемости ОА в семьях контрольной группы составила 25,2% (14 больных родственника из 180 обследованных), что согласуется с результатами исследования семей с ОА, проведенного Th. Schäller, составившими 27% [17]. Распространенность ОА по суммарным данным в общей популяции составляет 20% [18]. Определенная по данным нашего исследования частота ОА в семьях с ГМС превышает частоту заболевания в семьях без ГМС, распространенность ОА в общей популяции и в популяции гипермобильных пациентов, свидетельствуя о явной ассоциации ГМС и ОА, что подтверждает данные других исследователей [6-8].
Нами отмечена зависимость частоты встречаемости ОА и ГМС от степени родства с пробандом: чем выше степень родства, тем чаще данная патология наблюдалась среди его родственников. Так, в семьях пробандов с ОА и ГМС среди родственников I степени родства данная патология встречалась в 61,3% случаев, а среди родственников II и III степени родства – в 36,1% и 35,4% соответственно. Среди родственников I степени родства наиболее часто ОА наблюдался у матерей (84,6%) и дочерей (56,5%) пробанда. Заболеваемость сибсов в семьях составила для сестер 58,6% и 40,0% для братьев (рис. 1).

Рис. 1. Частота случаев ОА в семьях с ГМС.
Нами выявлена высокая ассоциация между ГМС и ОА, что может свидетельствовать о значимом вкладе сопутствующей ГМС в развитие генетической предрасположенности к ОА. Можно предположить, что гены, отвечающие за ГМС, входят в число главных генов «генных сетей», отвечающих за предрасположенность к ОА. Высокий процент встречаемости ГМС и ОА у лиц женского пола свидетельствует, что важный вклад в развитие данной патологии вносят и эстрогены.
Оценка влияния частота ОА и ГМС среди родственников в зависимости от пола пробанда не выявило значимых различий. Так, частота случаев заболевания среди родственников пробандов мужского пола по мужской и женской линиям составляет 30,7% и 28,4% случаев соответственно. Аналогичные данные получены и в отношении родственников пробандов женского пола их родственницы мужской и женской линиям болеют соответственно в 53,8% и 59,3% случаев, χ2 с поправкой Йетсена = 0,000, p=0,996.
Обследование семей показало, что ОА и ГМС только по линии матери встречался в 10 семьях (16,4%), только по линии отца – в 3 семьях (4,9%). Наиболее часто встречались сочетания: бабушка-мать-пробанд 11,5%, мать-сибс-пробанд 6,5%, а линии мать-сибс-пробанд-дочь, мать-сибс-пробанд-племянник, мать-пробанд-племянник-племянница, бабушка-мать-тетя-пробанд-кузена в 3,8% семей. В 4 семьях при наличии ОА и гипермобильности суставов у пробанда наблюдалось его отсутствие у членов семьи.
При анализе структуры заболеваний опорно-двигательного аппарата родственников пациентов с семейной ГМС выявлена высокая частота остеохондроза позвоночника – 51,3%, сколиоза – 21,1%, плоскостопия – 24,5%.
Обращает на себя внимание высокий процент пациентов с ОА в семьях с ГМС, имеющих показания к эндопротезированию одного или нескольких суставов – 22,0% (45 из 204 человек) по сравнению с семьями пациентов без ГМС, в которых у 14 человек, страдающих ОА, отсутствовали показания к операции (χ²=3,89; p=0,040). Этот факт, несомненно, свидетельствует о тяжелом течении ОА в семьях с ГМС. Операции по замене сустава проведены 28 пациентам (13,7%) из семей с ГМС. Средний возраст эндопротезирования суставов у пациентов составил 47 лет (41,5;51,5). В силу различных причин операция не проведена у 5 (2,5%) пациентов (наличие противопоказаний к операции, отказ от оперативного вмешательства и т.д.).
При оценке индекса отягощенности по ОА в семьях контрольной группы у 48 (80,0%) семей он определен как благополучный, а у 12 (20,0%) семей условно благополучный. Так как в семьях контрольной группы не выявлено неблагополучной отягощенности генеалогического анамнеза, то определение типа наследования патологии в них не проводилось. При оценке индекса отягощенности по ОА в семьях с ГМС лишь у 4 (6,5%) семей он был определен как благополучный, в 43 (70,4%) семьях – как условно благополучный и в 14 (23,1%) – неблагополучный.
Установленный факт высокой частоты ОА среди родственников пробандов и характер его распределения в семьях с ГМС свидетельствуют о возможной его наследственной предрасположенности.
Наследуемость предрасположенности к ОА определялась по модели Фальконер. Согласно этой модели коэффициент регрессии предрасположенности к ОА рассчитывался по формуле 6:
b=Xq–Xr/a=0,842-0,151/1,4=0,49 (6)
Величины Xq, Xr, a были взяты из таблицы-приложения значений Х и а для уровней от 0,01% до 50,0% [16].
Коэффициент наследуемости определялся по следующей формуле 7:
н²=b/r =0,49/2=0,245 (7)
Таким образом, наследуемость предрасположенности к ОА, согласно модели Фальконер, составила 25%, остальные 75% приходятся, вероятнее всего, на средовые факторы.
Поскольку выявлен небольшой (25%) вклад генетического компонента в детерминации заболевания, то это позволяет сделать вывод о том, что ОА является мультифакториальной патологией, ассоциированной с ГМС.
По литературным данным в семьях с ГМС определен различный тип ее наследования [5-8]. Однако в этих исследованиях тип наследования определялся визуально при помощи построения генеалогического дерева: по вертикали, когда признак регулярно передавался из поколения в поколение без пропусков, свидетельствуя об аутосомно-доминантном типе наследования, и по горизонтали (аутосомно-рецессивный тип), когда аналогичный признак обнаруживался у родных, двоюродных и троюродных сибсов пробанда. Проверка гипотезы о моногенной рецессивной природе признака более сложная задача, чем проверка гипотезы о моногенном доминантном наследовании из-за погрешностей, заключающихся в вероятности непроявления признака в семье с небольшим числом родственников. Для анализа такого материала все данные суммируют и проводят сегрегационный анализ. Чтобы учесть погрешности, вызванные особенностями сбора материала, сегрегационные частоты (SF) рассчитывают по формуле «сибсового» метода М. Вайнберга. При выполнении вычислений сегрегационных частот, использовались семьи с числом сибсов не менее двух, как наиболее информативные. В таблице анализа сегрегационной частоты остеоартроза представлены сибства, в которых один из родителей болен, а другой здоров (табл. 1).
Таблица 1. Сегрегационный анализ в семьях с ГМС
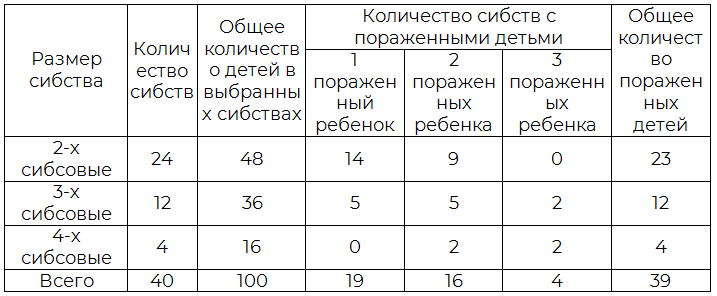
Оценку сегрегационной частоты получали по формуле 8 (данные взяты из табл. 1):
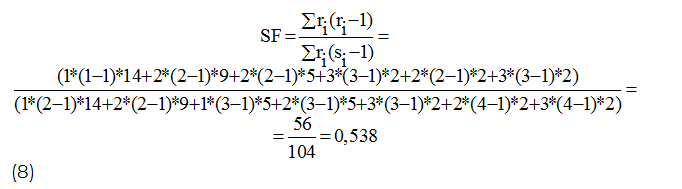
Вычисленную сегрегационную частоту сравнивали с теоретически ожидаемой, используя t-критерий Стьюдента (формулы 9 и 10):
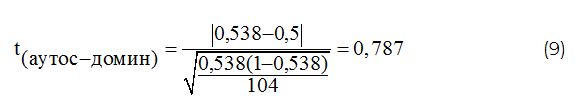
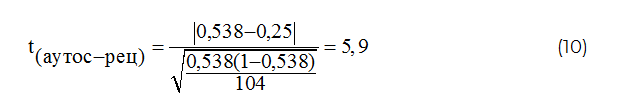
Таким образом, учитывая результаты «сибсового» метода сегрегационного анализа в семьях, пробанды которых имеют гипермобильность суставов, установлен аутосомно-доминантный тип наследования данной патологии, так как значение t=0,787 (<2,58).
Выводы
1. Определяемая по модели Фальконер наследуемость предрасположенности к ОА в семьях с ГМС выявила малый вклад генетического компонента в детерминации заболевания, что позволяет сделать вывод о том, что ОА является мультифакториальной патологией, ассоциированной с ГМС.
2. В семьях пациентов с ГМС определена высокая частота ОА, превышающая его частоту в семьях без ГМС. Отмечена зависимость частоты ОА и ГМС от степени родства с пробандом: чем выше степень родства, тем чаще встречается ОА и ГМС среди родственников пробанда.
3. В семьях пациентов с ГМС и ОА определена высокая частота раннего эндопротезирования суставов по сравнению с семьями без ГМС.
4. С помощью «сибсового» метода М. Вайнберга определен аутосомно-доминантный тип наследования ГМС в семьях.
