Введение. Грыжи - одно из самых распространенных заболеваний человека, которое наблюдается у 2-4% людей или до 40 на 10000 населения [1]. Ежегодно в мире выполняется более 20 миллионов операций по поводу грыж, что составляет от 10 до 15% всех вмешательств вообще [2, 3]. При использовании собственных тканей у каждого восьмого-десятого больного возникают рецидивы заболевания [4, 5]. В 1984 году I. Lichtenstein и P. Amid предложили использовать синтетические сетчатые эндопротезы из монофиламентного полипропилена и выдвинули новый подход в лечении паховых грыж – «ненатяжная герниопластика» [6]. Сегодня протезирующая герниопластика с применением полимерных материалов занимает ведущее место в хирургическом лечении грыж живота, что позволило снизить частоту рецидивов до 1,8-10% [7, 8]. В течение 20 века было создано большое количество синтетических материалов для протезирующей реконструктивной хирургии мягких тканей, однако ни один из них не лишен недостатков [9]. Для создания имплантатов будущего необходимо ответить на целый ряд вопросов о необходимой прочности, жесткости, поверхностной плотности, размерах ячейки, типа материала и др. Все вышесказанное и предопределило цель нашего исследования.
Цель работы. Изучить биомеханические свойства синтетических протезов различной структуры, химического состава и технологий производства после их имплантации.
Материалы и методы. Нами были изучены шесть образцов синтетических сетчатых протезов, выполненные из монофиламентного полипропилена (ПП) трех различных диаметров – Эсфил стандартный (d-0,12 мм, 62 г/м2), Эсфил легкий (d-0,09 мм, 40 г/м2), Эсфил сверхлегкий (d-0,07 мм, 19 г/м2); монофиламентного поливинилиденфторида (ПВДФ) – Унифлекс (d-0,12 мм, 150 г/м2); смеси монофиламентных ПП и ПВДФ – Флексилен (d-0,12 мм, 60 г/м2); смеси монофиламентных ПП и полиглекапрона (ПГК) – Ультрапро.
Основные структурно-физические параметры оценивались с помощью высокоточных электронных весов, разрывной машины РТ-250, осциллографического аппарата для измерения жесткости ИЖ-3.
Работа была выполнена на базе клиники экспериментальных животных №2 Военно-медицинской академии им. С.М. Кирова и кафедры оперативной хирургии Северо-Западного государственного медицинского университета им. И.И. Мечникова.
Для исследования было взято 54 кролика породы «Шиншилла» обоих полов в возрасте 1 – 1,5 года, весом 3000 – 3500 г. Все животные были разделены на шесть групп (в зависимости от имплантируемого эндопротеза) по 9 кроликов в каждой.
В соответствии со сроком имплантации (7, 30 и 90 суток) в каждой когорте животных были выделены подгруппы по 3 кролика. Основные этапы исследования включали: «введение» животных в эксперимент; экспозиция и наблюдение на протяжении срока имплантации эндопротеза; «выведение» животных из эксперимента и забор материала; оценка подпороговой (8 и 16 Н) и разрывной нагрузки, подпорогового (8 и 16 Н) и разрывного удлинения, жесткости на изгиб.
Оперативные вмешательства были проведены в асептических условиях под общей анестезией с использованием комбинации препаратов Золетил 50 и Ксила. После введения животного в наркоз после обработки операционного поля по средней линии живота в продольном направлении рассекалась кожа и подкожная клетчатка длинной 4 – 5 см, отступя книзу от мечевидного отростка на 2 см. Далее передняя стенка влагалища (апоневроза) прямых мышц освобождались от клетчатки путем ее отсепаровки в стороны от срединного разреза на расстояние 2,5 - 3 см. В созданное таким образом пространство («ложе») помещался эндопротез и фиксировался к апоневрозу прямых мышц живота узловыми швами по периферии нитью на атравматической игле. Эндопротезы фиксировали полипропиленовой мононитью 3/0.
Для выполнения биомеханических измерений выполнялось отделение сетки с капсулой острым и (или) тупым способом от мышц, после чего эндопротез помещался в емкость с физиологическим раствором NaCl 0,9% и немедленно доставлялся в лабораторию. Для проведения исследования на разрывной машине из представленного образца 5х10 см, готовились полоски шириной строго 1 см и длиной не менее 5 см. Регистрировалось удлинение полоски при нагрузке в 8 Н, 16 Н и в момент разрыва образца, кроме того, регистрировалась разрывная нагрузка. Методика измерения жесткости проводилась по методике проф. В.М. Лазаренко в двух направлениях: вдоль петельного ряда, вдоль петельного столбика.
Результаты и обсуждение. На сроке 7 суток ни один из образцов не изменил своих геометрических размеров. Однако уже через 1 месяц полипропиленовые протезы Эсфил стандартный и Эсфил легкий продемонстрировали усадку, которая составила 17,2% и 9% по площади, вдоль петельного ряда – 8% и 3%, вдоль петельного столбика – 10% и 7% соответственно. Спустя 90 дней после имплантации общая усадка достигла 19,5% и 8,6%, вдоль петельного ряда – 9% и 3%, вдоль петельного столбика – 12,5% и 4% для первого и второго образцов. Остальные же сетчатые имплантаты продемонстрировали на поздних сроках стабильность своих физических размеров.
При оценки жесткости уже через 7 суток после имплантации первые два образца (Эсфил стандартный и легкий) достигли пика по данному показателю, как вдоль петельного ряда, так и вдоль петельного столбика. Эндопротез Эсфил сверхлегкий и Унифлекс обладали максимальной жесткостью через месяц после имплантации. Самый тяжелый из представленных имплантатов Ультрапро и Флексилен приобретали наибольшую жесткость к 3 месяцам имплантации (табл. 1).
Таблица 1. Характеристика жесткости протезов на различных сроках после имплантации, (сН∙мм2)
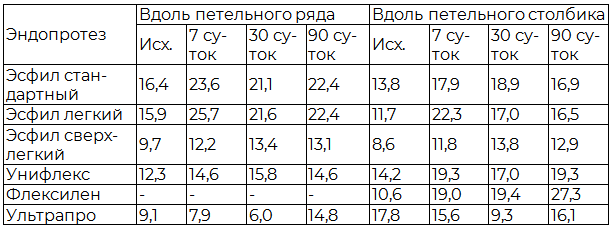
Примечание: здесь и далее Исх. - исходные данные физико-механических свойств эндопротезов до имплантации.
Исследование прочностных свойств сетчатых имплантатов показало, что максимальная прочность эндопротезов соответствовала их пиковой жесткости. Такая закономерность объясняется тем, что именно в эти периоды тканевой реакции вокруг сетчатого материала имеется наиболее грубая капсула. Исключением из этого правила стал имплантат Ультрапро это связано с тем, что у него имеется рассасывающаяся часть, за счет которой и понижается прочность (табл. 2).
Таблица 2. Прочностные свойства протезов при одноосном растяжении на различных сроках после имплантации
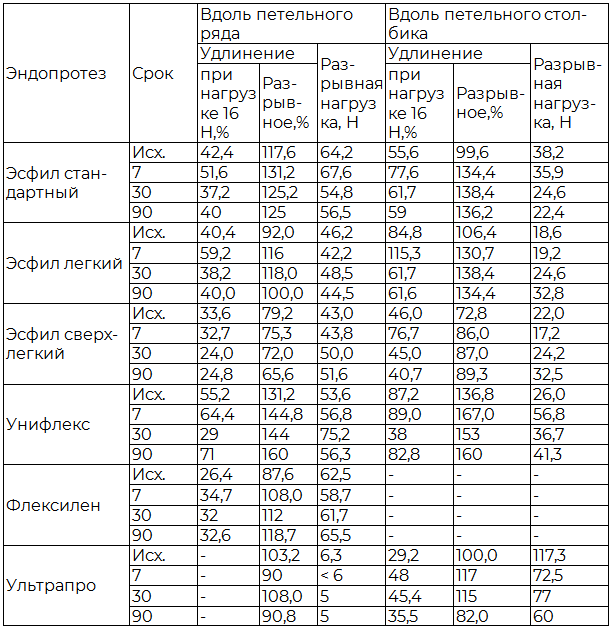
Выводы. Проведенное экспериментальное исследование биомеханических свойств образцов позволило получить ценную информацию о динамике инкорпорации имплантатов в окружающие ткани, выявило особенности реакции тканей на различные виды эндопротезов и позволило сформулировать основные требования к структурно-физическим параметрам инновационных сетчатых материалов. Среди основных обнаруженных закономерностей можно выделить нижеследующие, имеющие особое практическое значение.
Начиная с 30 суток после имплантации подпороговая (при нагрузке 8 Н и 16 Н) растяжимость эндопротезов всецело определяется свойствами соединительнотканной капсулы. Это указывает на бессмысленность придания эндопротезам растяжимости более 20-30% при подпороговой нагрузке.
Жесткость эндопротезов на изгиб определяется преимущественно диаметром мононитей, из которых изготовлена сетка. При этом структура сетки (большие или малые ячейки) имеет второстепенное значение.
Анизотропия сетчатого эндопротеза (в следствие несовершенной технологии плетения или в результате рассасывания компонентов) может приводить к высокой угрозе его разрушения в тканях на любом сроке после имплантации. При этом даже через 90 суток прочность сформированной рубцовой капсулы не превышает 5-7 Н.
Уменьшение поверхностной плотности эндопротеза – один из основных факторов, благоприятно влияющих на биомеханические свойства сеток. Однако при неоправданном снижении данного показателя прочность сетки многократно снижается, повышая риск ее разрушения при минимальных нагрузках.
