Проблема тромбоэмболий при хирургических операциях, сопровождающихся наложением пневмоперитонеума, требует дальнейшего изучения [2,3,5]. Несмотря на относительную редкость указанных осложнений в клинической практике, имеются указания на субклинические проявления нарушений кровообращения [2,4].
Одной из недостаточно изученных, остается проблема состояния эндотелия при различных режимах интраоперационного пневмоперитонеума.
Как известно, под эндотелиальной дисфункцией определяется, прежде всего, дисбаланс продукции вазоконстрикторов и вазодилататоров [5,8-10].
Основными факторами, активирующими эндотелиальные клетки, являются: изменение скорости кровотока, тромбоцитарные факторы, циркулирующие нейрогормоны (катехоламины, ацетилхолин, эндотелин, брадикинин, ангиотензин II), гипоксия [7,8,10].
Поддержание повышенного внутрибрюшного давления во время проведения лапароскопических операций сопровождается микроциркуляторными сдвигами, что может повлечь за собой повреждение клеток эндотелия, изменение сосудистого тонуса и развитие тромбоэмболических осложнений.
Остаются недостаточно изученными изменения функции эндотелия под влиянием различных режимов интраоперационного пневмоперитонеума и их значение в патогенезе тромбоэмболических осложнений, недостаточно обоснованы безопасные границы внутрибрюшного давления.
Цель работы: оценить уровень маркеров функции эндотелия при различных режимах интраоперационного пневмоперитонеума.
Материалы и методы. Изучена группа из 100 больных женского пола, в возрасте от 40 до 60 лет, которым проводилась лапароскопическая холецистэктомия по поводу желчнокаменной болезни.
Все пациенты находились на лечении в ГУЗ Городская клиническая больница №1 города Читы. Из исследования исключались лица, имеющие тяжелую сопутствующую патологию, операционно-анестезиологический риск выше II класса по ASA (Американская ассоциация анестезиологов), а также с варикозной болезнью вен нижних конечностей.
Пациенты не получали антикоагулянты и дезагреганты. Кровь у больных забиралась из локтевой вены до наложения пневмоперитонеума и сразу после выведения газа из брюшной полости.
Исследование содержания циркулирующих эндотелиоцитов проводилось при помощи проточной цитометрии. Определение лимфоцитарно-тромбоцитарной адгезии (ЛТА) выполнялось по методу, предложенному Ю.А. Витковским и соавт. [1].
Подсчитывали число лимфоцитарно-тромбоцитарных коагрегатов на 100 клеток (показатель ЛТА) и среднее число кровяных пластинок, адгезированных на поверхности одного лимфоцита (степень адгезии).
Для количественного определения антигена фактора Виллебранда, урокиназного активатора плазминогена (u-PA), тканевого активатора плазминогена (t-PA) в образцах человеческой цитратной плазмы методом иммуноферментного анализа использовались наборы TECHNOZYM® (Technoclone).
При определении уровня гомоцистеина с помощью анализатора «Expert 96» применялся метод твердофазного иммуноферментного анализа.
Обследуемые пациенты разделялись на 4 группы:
1-я группа - 25 человек, которым выполнялась лапароскопическая холецистэктомия с использованием давления в брюшной полости от 8 до 12 мм рт.ст., временем выполнения операции до 30 минут;
2-я группа больных (n=25) - во время операции давление пневмоперитонеума составляло от 12 до 16 мм рт. ст., время операции до 30 минут;
3-я группа больных (n=25) - использовалось давление пневмоперитонеума от 8 до 12 мм рт.ст., и временем выполнения операции от 30 до 60 минут;
4-я группа больных (n=25) - во время операции давление пневмоперитонеума составляло от 12 до 16 мм рт. ст., время операции от 30 до 60 минут.
Статистический анализ проводился с помощью пакета программ Microsoft Excel с применением параметрических (критерий Стьюдента) и непараметрических (критерий Манна-Уитни, χ2) методов.
Критический уровень значимости при проверке гипотез p=0,05.
Результаты и обсуждение. Под действием пневмоперитонеума происходит повышение содержания циркулирующих эндотелиальных клеток (ЦЭК) во 2-й группе пациентов в 1,7 раза (p<0,05) (табл. 1).
Кроме того, в этой же группы регистрируется увеличение содержания молодых (ростковых) эндотелиоцитов на 83% (p<0,05), а также повышение количества активированных эндотелиоцитов на 17% (p<0,05).
В свою очередь, использование пневмоперитонеума от 12 до 16 мм рт. ст. и длительности операции от 30 до 60 минут у пациентов 4-й группы приводит к увеличению количества циркулирующих эндотелиоцитов в 1,8 раза (p<0,05), числа молодых эндотелиоцитов на 64% (p<0,05) и активированных - на 11% (p<0,05) (табл. 2).
Таблица 1. Изменение содержания циркулирующих эндотелиоцитов при разных режимах пневмоперитонеума (M±SD)
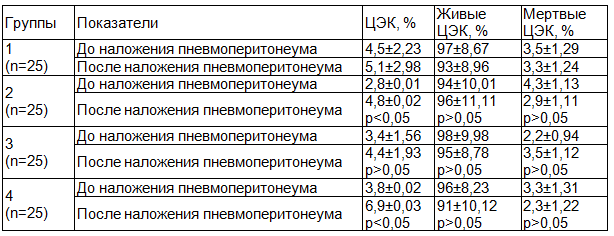
Примечание: p - значимость относительно исходных значений.
Таблица 2. Изменение содержания ростковых и активированных циркулирующих эндотелиоцитов, при разных режимах пневмоперитонеума (M±SD)
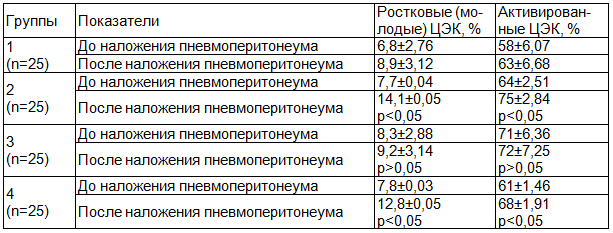
Повышение количества циркулирующих и активированных эндотелиальных клеток во 2-й и 4-й группах свидетельствует о повреждающем действии повышенного внутрибрюшного давления на сосудистую стенку при данных режимах пневмоперитонеума.
Кроме того, увеличение числа молодых (ростковых) эндотелиальных клеток свидетельствует об усилении механизмов регенерации.
У пациентов 1-й и 3-й групп не выявлено значимых изменений количества ЦЭК.
При исследовании тканевого фактора активации плазминогена (t-PA) у пациентов 1-й, 2-й, 3-й групп не выявлено значимых изменений.
Отмечено повышение t-PA у пациентов 4-й группы на 78% (p<0,05) с наибольшим внутрибрюшным давлением и большей длительностью операции.
При исследовании u-PA не выявлено значимых изменений концентрации ни в одной из групп (табл. 3).
Таблица 3. Изменение содержания тканевого активатора плазминогена (t-PA), урокиназного активатора плазминогена (u-PA) при разных режимах пневмоперитонеума (M±SD)
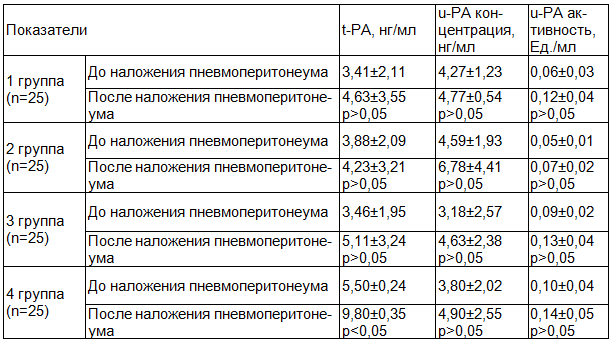
Тканевой активатор плазминогена секретируется эндотелиальными клетками и является основным активатором системы фибринолиза [3].
У пациентов 4-й группы происходит повышение содержание t-PA выше физиологической нормы, что может свидетельствовать о значительной активации эндотелиоцитов, снижении кровотока в венозной системе, и включении компенсаторных механизмов в ответ на повышение риска венозного тромбоза.
При определении антигена фактора Виллебранда у пациентов 1-й, 2-й, 3-й групп не выявлено значимых изменений. Однако зарегистрировано повышение его концентрации у пациентов 4-й группы на 19% (p<0,05) (табл. 4).
Таблица 4. Изменение ЛТА и антигена фактора фон Виллебранда во время лапароскопического вмешательства при разных режимах пневмоперитонеума (M±SD)
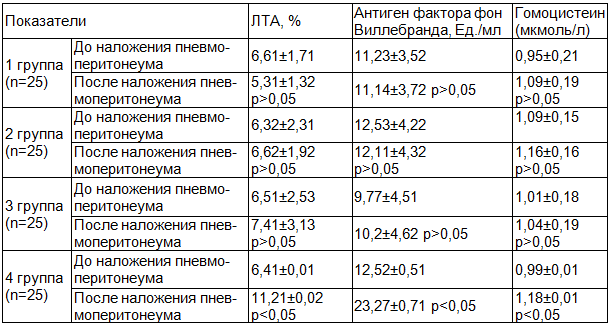
Повышение количества антигена фактора фон Виллебранда также свидетельствует о повреждении сосудистой стенки и изменении биохимических свойств крови.
Содержание гомоцистеина не меняется при наложении пневмоперитонеума у пациентов 1-й, 2-й и 3-й групп.
При этом в 4-й группе с наиболее высоким давлением и большей продолжительностью операции определяется повышение гомоцистеина в 1,9 раза (p<0,05), до уровня 23,27 мкмоль/л, что соответствует умеренной гипергомоцистеинемии (табл. 4).
Данное состояние оказывает неблагоприятное влияние повышенного брюшного давления на механизмы ауторегуляции сосудистого тонуса, обмена липидов и коагуляционного каскада [11].
При исследовании лимфоцитарно-тромбоцитарной адгезии (ЛТА) значимое влияние пневмоперитонеума выявлено у пациентов с давлением 12 - 16мм рт.ст. и длительностью операции от 30 до 60 минут (4-я группа).
Отмечается повышение ЛТА под влиянием пневмоперитонеума в 1,75 раза (p<0,05), но при этом значение параметра не выходит за рамки физиологической нормы.
Однако можно предположить, что значительное увеличение продолжительности операции с длительной интраабдоменальной гипертензией может привести к существенным сдвигам уровня ЛТА, и других маркеров дисфункции эндотелия, что будет свидетельствовать об активизации межклеточных взаимодействий, значительном повреждении клеток сосудистой стенки, которое в свою очередь сопровождается дисбалансом вазоактивных веществ, нарушениями механизмов ауторегуляции периферического кровотока и опасно увеличением риска тромбоэмболических осложнений.
Выводы
- У пациентов при давлении пневмоперитонеума свыше 12 мм. рт. ст. и продолжительности операции менее 30 минут в системном кровотоке происходит повышение концентрации циркулирующих эндотелиальных клеток в 1,7 раза, повышение количества ростковых эндотелиоцитов на 83%, количества активированных эндотелиальных клеток на 17%.
- Интраабдоменальная гипертензия свыше 12 мм рт. ст. при длительности операции от 30 до 60 минут сопровождается увеличением количества циркулирующих эндотелиальных клеток в 1,8 раза, ростковых эндотелиоцитов на 64%, активированных эндотелиальных клеток на 11%.
- Применение пневмоперитонеума свыше 12 мм рт. ст. при длительности операции от 30 до 60 мин сопровождается повышением в крови больных уровня тканевого фактора активации плазминогена на 78%, антигена фактора Виллебранда на 19%, уровня гомоцистеина в 1,9 раза, активности лимфоцитарно-пластиночных взаимодействий в 1,75 раза.
