Актуальность. Острый холецистит (ОКХ) в настоящее время остается одним из наиболее часто встречаемых заболеваний в абдоминальной ургентной хирургии и занимает второе место после аппендицита [1, 2].
Частота его обусловлена большой распространенностью желчнокаменной болезни, которая осложняется развитием острого или хронического холецистита, холедохолитиаза, механической желтухой и др. [3, 4].
Заболевание чаще наблюдается у лиц пожилого и старческого возраста, а в последние годы многие исследователи отмечают рост заболеваемости у пациентов молодого и среднего возраста [5, 6]. При этом большинство больных поступает с флегмонозной или гангренозной формой.
Увеличение больных с деструктивными формами обусловлено поздним обращением больных, частотой сопутствующих заболеваний, способствующих атипичному течению и проявлению заболевания, снижением иммунобиологической реактивности населения, приемом многих лекарственных препаратов: гормонов, иммуно-депресантов, антибиотиков, различных обезболивающих и спазмолитических средств [7, 8].
Несмотря на совершенствование хирургической техники, применение различных мер профилактики, частота послеоперационных раневых осложнений остается на высоком уровне, особенно при деструктивных формах холецистита.
Наибольший удельный вес среди осложнений занимают раневые, при возникновении которых увеличиваются сроки стационарного и амбулаторного лечения, а следовательно и увеличиваются материальные затраты больного и государства. Идут поиски мер, которые бы надежно предотвращали возникновение раневых осложнений.
Цель исследования – улучшить результаты лечения у больных с деструктивными формами холецистита за счет использования инфракрасного излучения на область операционной раны.
Материал и методы исследования. Под наблюдением находилось 170 больных с острым деструктивным холециститом, которые были оперированы в хирургических отделениях Городской клинической больницы №1, г. Бишкек в период 2017 и по март 2018 г.
Мужчин было 51, женщин 129. Возраст колебался от 17 до 82 лет. Наибольшее число больных было в возрасте от 40 до 60 лет (102 чел. – 60,0% ).
В процессе работы с целью оценки эффективности мер профилактики мы выделили две группы больных.
В первую включили пациентов у которых в послеоперационном периоде использовали антибиотики (гентамицин по 80 мг два раза в сутки внутримышечно или ампициллин по 500 тыс. ед. 4 раза в сут. внутримышечно) на протяжении 4-5 сут. – эта группа служила для нас контролем – 102 чел.
Во вторую группу мы включили больных, которые до операции получали цефазолин или цефтриаксон по 1,0 внутривенно и в этой же дозировке к концу операции тоже вводили внутривенно, а после операции, начиная с 2 сут. назначали инфракрасное лазерное излучение аппаратом «Мустанг», экспозиция 10 мин., на курс 4-5 облучений – это была основная группа, она включало 68 больных.
В обеих группах больные, помимо мер профилактики получали лечение сопутствующих заболеваний, инфузионную терапию, включающую солевые растворы, реополиглюкин, комплекс витаминов, обезболивающие средства по показаниям.
В обследовании больных помимо общеклинического (анализ крови и мочи, свертываемость, ЭКГ), использовали УЗИ органов брюшной полости до операции для определения характера заболевания и сопутствующей патологии, а после операции для выявления осложнений брюшной полости и оценки течения раневого процесса (эхоморфометрия ран) – измеряли зону инфильтрации операционной раны через 1, 3 и 5 сут. после операции, а при необходимости и в более поздние сроки, а также оценивали клинические показатели (нормализация температуры, исчезновение боли, частота осложнений и сроки стационарного лечения).
В разработку включали больных с деструктивными формами холецистита (флегмонозная, гангренозная, эмпиема желчного пузыря), с подтверждением макроскопическим и гистологическим исследованием. Было уделено внимание срокам поступления в стационар (табл. 1) с момента заболевания.
Полученные результаты обработаны методом вариационной статистики с вычислением средней арифметической (М), средней квадратичной величин (σ) и ошибки ряда (m).
Степень достоверности вычисляли по таблице Стьюдента. Различия между сравниваемыми параметрами считали достоверными при р≤ 0,05.
Таблица 1. Сроки поступления в стационар больных с острым деструктивным холециститом
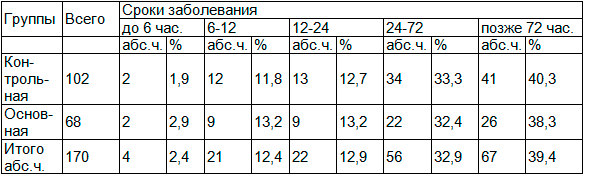
Анализ сроков заболевания показал, что в обеих группах больных в первые 6-12 ч. от начала заболевания больные поступали редко, а основная часть больных была госпитализирована позже суток от начала заболевания и почти 1/3 позже 3 сут.
При этом установлено, что многие больные, зная о существовании у них ЖКБ принимали обезболивающие, спазмолитические средства и лишь при прогрессировании – обращались к врачу или вызывали бригаду скорой помощи. Нередко (28 чел.) пациенты наблюдались у семейного врача.
В этом случае основное внимание уделялось сопутствующим заболеваниям, и при появлении симптомов раздражения брюшины больных направляли в хирургическую клинику.
В результате обследования в контрольной и основной группах были выявлены следующие сопутствующие заболевания (табл. 2).
Таблица 2. Характер сопутствующих заболеваний у больных холециститом
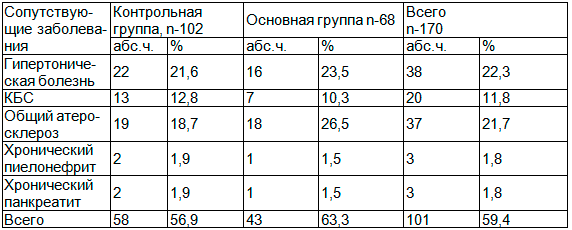
Наибольшую группу составили больные, страдавшие гипертонической болезнью и общим атеросклерозом, другие сопутствующие заболевания выявлялись реже.
Анализ результатов УЗИ показал, что у всех обследованных выявлены конкременты (одиночные у 84, а у остальных множественные), изменения стенки пузыря, увеличение объема, а у 18 наличие перивезикулярного абсцесса, у 11 перивезикулярного инфильтрата.
Больные контрольной и основной группы оперированы под эндотрахеальным наркозом. У большинства холецистэктомия выполнялась из минилапаротомного доступа (5-6 см) и лишь у 17 больных контрольной и 12 основной группы выполнен традиционный доступ (20-25 см) – этот доступ выполнялся при выявлении при УЗИ перивезикулярного абсцесса или инфильтрата.
Результаты исследования и их обсуждение. После проведенного обследования и установления характера заболевания все больные оперированы. В процессе ведения послеоперационного периода проследили за клиническими показателями больных контрольной и основной групп (табл. 3).
Таблица 3. Клинические показатели больных с острым деструктивным холециститом контрольной и основной групп в послеоперационном периоде (в сут.)
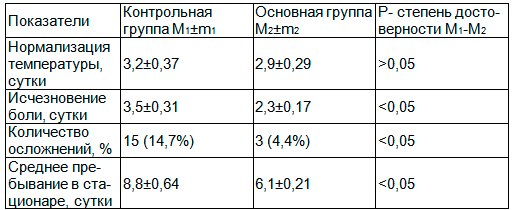
При оценке клинического течения заболевания отмечено, что у больных основной и контрольной групп одновременно наступала нормализация температуры, но болевой синдром исчезал достоверно быстрее у больных основной группы, а также достоверно реже возникали осложнения.
В контрольной группе из 102 оперированных осложнения возникли у 15 больных, что составило 14,7%. Из 98 больных, которым выполнена была холецистэктомия у 3 возникли осложнения (кровотечение 1, желчеистечение 2, нагноение раны у 4 и инфильтрат в области операционной раны у 3), у одной из них была выполнена повторная операция по поводу возникшего кровотечения, а остальные осложнения вылечены медикаментозной терапией.
У 3 пациентов выполнена холецистэктомия с дренированием по Вишневскому – у двух из них выявлены осложнения – желчеистечение и инфильтрат.
Еще у одного произведена холецистэктомия с внутренним дренированием у него послеоперационный период осложнился нагноением раны.
В основной группе оперировано было 68 больных с острым холециститом, осложнения возникли у 3 (4,4%), из них нагноение раны у одного и у 2 инфильтрат, которые были излечены к моменту выписки из стационара.
При анализе сроков стационарного лечения было установлено достоверное увеличение срока у больных контрольной группы (соответственно 8,8±0,64 и 6,1±0,21 койко-дней).
Известно, что в медицинской практике широко используются различные физические методы воздействия (тепловые, электрические, световые, лучевые и др.), улучшающие заживление ран.
К новейшим разработкам в этом отношении, несомненно, можно отнести разработки и последующего внедрения, с середины прошлого столетия, в практику различных разделов клинической медицины метода транскутанного воздействия низкоинтенсивным лазерным излучением.
Метод демонстрировал выраженный позитивный физиотерапевтический эффект при лечении многих заболеваний в терапии, неврологии, гинекологии и др. [2].
По мнению большинства исследователей, лечебное воздействие низкоинтенсивного лазерного излучения в клинической практике поливалентно. Определенное значение имеют данные о свойствах низкоинтенсивного лазерного излучения, улучшающих микроциркуляторные процессы, что представляет исключительный интерес для практики интенсивной терапии и реанимации.
Выраженный эффект низкоинтенсивного лазерного излучения в отношении транспорта кислорода наблюдали многие клиницисты [3, 5].
Учитывая данные литературы, в процессе лечения было использовано инфракрасное лазерное облучение послеоперационных ран для профилактики гнойно-септических осложнений.
В процессе наблюдения за течением раневого процесса мы выполнили эхоморфометрию ран в контрольной и основной группах (табл. 4).
Таблица 4. Эхоморфометрия ран больных с острым деструктивным холециститом контрольной и основной групп (в см) в послеоперационном периоде
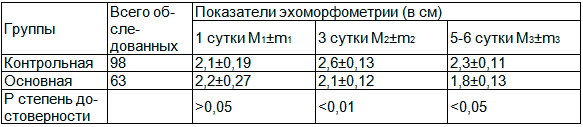
Результаты эхоморфометрии показали, что через сутки после операции зона инфильтрации операционной раны была равнозначной в обеих группах, а на 3 сут. у больных контрольной группы зона инфильтрации увеличилось в сравнении с первыми сутками, в то время как у больных основной группы она оставалась на уровне показателя через сутки после операции.
На 5-6 сут. показатель эхоморфометрии ран снизился до 2,3±0,11 см, но более выраженное снижение имело место у больных основной группы.
Следовательно, применение инфракрасного излучения способствует более благоприятному течению раневого процесса. Однако, далеко не у всех больных наблюдалась такая закономерность.
Полученные результаты в целом коррелируют с данными других авторов [4, 6].
У 4-х больных контрольной и у 3-х больных основной группы на 5-е сутки после операции мы не отметили уменьшения зоны инфильтрации в сравнении с 3 сутками, что явилось для нас основанием для ревизии раны и усиления противовоспалительной терапии, что и было нами выполнено и предотвратило возникновение осложнений.
Результаты исследования показали, что введение антибиотиков до операции и к концу ее с включением в комплекс профилактики после операции инфракрасного излучения на область операционной раны способствует более благоприятному течению послеоперационного периода и снижению частоты осложнений.
Выводы:
- Использование антибиотиков с целью профилактики гнойно-воспалительных осложнений малоэффективно (процент осложнений при применении только антибиотиков составил 14,7%).
- Применение внутривенного введения антибиотика в сочетании с инфракрасным лазерным излучением после операций, выполненных по поводу деструктивного холецистита способствует более раннему исчезновению болевого синдрома, снижает частоту раневых осложнений (4,1%) ведет к сокращению сроков стационарного лечения, что является основанием для внедрения этих мер профилактики в хирургических стационарах.
