Лечение повреждений локтевого сустава (ЛС) до настоящего времени остается одной из трудных и до конца не решенных проблем современной травматологии и ортопедии. Они занимают первое место по числу посттравматических осложнений, до 30% случаев приводит к стойкой инвалидизации пациентов [1], это связано со сложность анатомии и биомеханики ЛС, а так же со склонностью к параартикулярной оссификации и быстрому развитию посттравматических контрактур.
Патогенез развития посттравматических контрактур ЛС по данным литературы разнообразен и включает в себя: особенности его анатомии, часто сложный характер переломов, повреждение капсулы и связок, кровоизлияние в мягкие ткани, которое увеличивается при попытках закрытой репозиции; фиксацию гипсовой повязкой на длительный срок, позднее выполнение операции, ее травматичность, неполную репозицию и нежесткую фиксацию переломов, длительную внешнюю иммобилизацию после операции, а также нерациональную реабилитацию - позднее начало активных движений, попытки редрессации пассивными движениями, назначение физиопроцедур, тепла и массажа.
Причиной снижения функциональных показателей после проведенного остеосинтеза костей образующих локтевой сустав является отсутствие эффективного реабилитационного лечения. Восстановительный период после операции на локтевом суставе, по нашему убеждению и мнению многих авторов, является не менее важным, чем сама операция.
При переломах костей образующих локтевой сустав со смещением отломков полная репозиция и конгруэнтность сустава должны быть восстановлены открытой репозицией в первые сутки после травмы или через 4-6 дней после полного спадения отека. Индивидуальный остеосинтез по технологиям АО в зависимости от степени тяжести перелома обеспечивает надежную фиксацию для безгипсового ведения больного и раннего восстановительного лечения после операции. У всех оперированных больных использовали разработанные нами протокол и реабилитационную программу.
Занимаясь решением проблем улучшения результатов лечения около-и внутрисуставных переломов ЛС, мы с 2008 г. в большом ортопедо-травматологическом центре (430 коек КБ СМП им. Н.В. Соловьева г. Ярославль) выделили одно место для лечения этих больных – отделение хирургии кисти и локтевого сустава, и на основе достижений зарубежных травматологов [2-4], придерживающихся воззрений швейцарской ассоциации по изучению внутреннего остеосинтеза (AO/ASIF), выработали протокол оказания высокоспециализированной помощи таким пострадавшим и протокол их реабилитации. В этом протоколе мы четко выделили показания к консервативному и оперативному лечению. Консервативно лечили лишь тех, у кого не было смещений отломков. У всех получили отличные и хорошие результаты. При наличии смещений не делали попыток закрытой репозиции, так как, если бы они и были удачными, то все равно было бы необходима 4-6 недель внешняя иммобилизация, а это неминуемая контрактура ЛС.
Оперировали около-и внутрисуставные переломы ЛС по технологиям АО/ASIF. При репозиции переломов дистального отдела плечевой кости преимущества отдаем доступу без отсечения локтевого отростка и сухожилия трехглавой мышцы плеча. При оперативном лечении отличные и хорошие результаты были получены у 90,4% больных с внесуставными переломами, у 94,1% - при неполных внутрисуставных переломах и у 80,7% - при полных внутрисуставных переломах.
Мы не получили полного удовлетворения от результатов лечения. Контрактуры ЛС порой были непредсказуемы. Это заставило нас искать причину таких осложнений.
Мы обратили внимание, среди больных с удовлетворительными и неудовлетворительными исходами чаще были женщины с особым психологическим статусом (нервные, плаксивые, неуверенные). Анализ связи боли и психологического состояния показал, что боль всегда ассоциируется с тревогой и депрессией. Такие психофизиологические расстройства, как нарушение сна, беспокойство, тревога, астения очень часто наблюдаются у людей, у которых впоследствии развивается хронический болевой синдром. Ранее была высказана гипотеза о том, что депрессия усиливает сенсорную трансмиссию боли, в результате чего происходит её соматическое фокусирование. Возникающий порочный круг приводит к так называемой катастрофизации самоощущения (нет веры в то, что можно излечиться, решить проблемы), что в свою очередь приводит к акцентуации болевых ощущений. Серотонин помогает передать информацию из одной области мозга в другую. Кроме того, он влияет на множество психологических и других процессах в организме. Из 80-90 миллиардов клеток головного мозга серотонин оказывает прямое или косвенное влияние на большинство из них. Он затрагивает работу клеток, которые отвечают за настроение, аппетит, сон, память и способность к обучению, температуру и некоторые аспекты социального поведения. Доказано, что при снижении серотонина повышается чувствительность болевой системы организма, то есть даже самое слабое раздражение отзывается сильной болью.
XXI век — время стрессов и перегрузок, преимущественно психических, вследствие этого распространенность психических расстройств в человеческой популяции (по данным Эпидемиологической программы Национального института психического здоровья, США) составляет 32,7%. Из них наиболее характерными являются тревожно-аффективные расстройства (22,9%) и депрессия (5,9%). Эти расстройства настолько тесно связаны между собой, что их принято объединять в единое понятие — «тревожно-депрессивный синдром». В неврологии и психиатрии так называют пациентов с субклинически выраженной тревогой [5, 6]. Пригласив для совместной работы невролога, мы решили выработать новый подход к лечению и реабилитации этой категории больных.
В период с февраля 2014 г. по ноябрь 2014 г. нами отобраны 32 пациента с повреждениями локтевого сустава (переломы головки лучевой кости, проксимального отдела локтевой кости и дистального метаэпифиза плечевой кости), у которых были признаки тревожно-депрессивного состояния. Все они были работоспособного возраста (от 23 до 48 лет) и прооперированы в нашей клинике с соблюдением протоколов оперативного лечения и программ реабилитации пациентов с повреждениями ЛС.
Существенная роль в проявлении болевого синдрома принадлежит серотонинергическому компоненту. Причем, между оппиоидным и серотонинергическим компонентами имеется определенный синергизм действия в регуляции болевого порога. У человека нейроны, содержащие серотонин, находятся в ядрах шва мозга и центральном сером околоводопроводном веществе. В условиях физиологии они обеспечивают определенный уровень содержания серотонина в организме. Отклонение его содержания в ту либо иную сторону изменяет порог болевой чувствительности. В частности, снижение содержания серотонина отмечается при хроническом депрессивном состоянии, которое сопровождается значительным понижением порога болевой чувствительности.
Пациенты были осмотрены неврологом и обследованы по визуально-аналоговой шкале (ВАШ) и шкалам DN4 (опросник для оценки интенсивности боли) и HADS (госпитальная шкала тревоги и депрессии) [7].
Таблица 1. Результаты расширенного неврологического осмотра
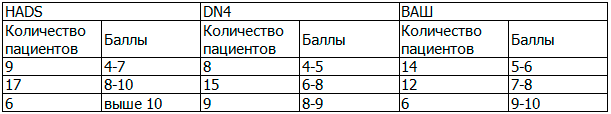
Получены следующие результаты по HADS: у 9 пациентов 4-7 баллов (нет тревоги и депрессии), у 17 – 8-10 баллов (субклинически выраженная тревога и депрессия), у 6 – более 10 баллов (клинически выраженная тревога и депрессия).
По DN4: у 8 пациентов 4-5 баллов, у 15 – 6-8 баллов, у 9 – 8-9 баллов. У всех 32 пациентов получено более 4 баллов (нейропатическая боль).
По результатам ВАШ у всех пациентов было более 5 баллов: у 14 – 5-6 баллов, у 12 – 7-8 баллов и у 6 – 9-10 баллов.
Пациенты были разделены в две группы. Группа контроля (15 человек), они получали стандартную метаболическую и терапию нестероидными противовоспалительными средствам (НПВС) в поликлинике по месту жительства. И исследуемая группа (17 человек), это пациенты, которые получали специфическую терапию тревоги (табл. №2).
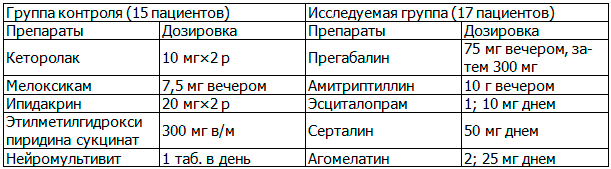
На амбулаторном этапе в контрольной группе назначался: кеторолак 10мг 2 раза в день (5-10 дней), затем переводили на мелоксикам 7,5 мг вечером (14 дней). Ипидакрин 20 мг 2 раза в день (30 дней). И этилметилгидроксипиридина сукцинат 300 мг в/м (10 дней), затем его же продолжали в таблетках по 100 мг 3 раза в день (30 дней). Так же назначали нейромультивит по 1 таб. в день до 30 дней.
В исследуемой группе назначали прегабалин 75 мг вечером, через пять дней повышали дозу до 150 мг. 8 (47%) пациентам из 17 потребовалось повышение до 300 мг в сутки и один пациент – 450 мг в сутки. Так же амитриптилин в стартовой дозе 10мг вечером. При хорошей переносимости 20 мг вечером (30 дней). 7 (41,1%) человек переводили на эсциталопрам 10 мг днем, 4 (23,5%) - на серталин 50 мг днем, 6 (35,2%) на агомелатин 25 мг днем до 6 мес.
Таблица 2. Группы пациентов
В группе контроля – боль снизилась до 5-6 баллов по ВАШ к 30 дню, затем незначительный регресс до 4-5 баллов в течение 60 дней. Баллы по HADS не улучшились, даже у 6(40%) пациентов показатели стали хуже из-за хронизации боли. По DN4 у всех пациентов наблюдались явные признаки нейропатии (более 4баллов) к 30 дню терапии. Показатели менее 4 баллов снизились у 3 (20%) исследуемых к 60 дню терапии. Объем движений в локтевом суставе увеличился на 8-10о сгибание-разгибание и ротационные движения на 10-15о.
В исследуемой группе за первые 5 дней снизились баллы по ВАШ до 5. Через 30 дней ВАШ 2-3 балла. У 6(35,2%) пациентов ВАШ к 30 дню – 0 баллов. По DN4 у 11(64,7%) пациентов к 30 дню снизились до 4-5 баллов. По HADS к 30 дню до 7-9. К окончанию курса лечения (90 дней) у всех пациентов было менее 7 баллов. В течение первых 12 дней приема препаратов, все они отмечали улучшение переносимости реабилитационных мероприятий (ЛФК) и общего настроя относительно исхода болезни. По окончании курса терапии боль не рецидивировала. Дальнейшее развитие комплексного регионального болевого синдрома (КРБС) прекратилось. Объем движений в локтевом суставе увеличился на сгибание-разгибание (0-15о -120о), пронация-супинация (65-75о). У двух пациентов была плохая переносимость прегабалина в виде головокружения, в результате чего мы вынуждены были прекратить специфическое лечение и у данных больных процесс реабилитации проходил очень долго и болезненно.
В группе контроля было выраженное снижение темпов реабилитации. Плохой настрой на положительный исход лечения. У шести больных сформировалась стойкая хроническая нейропатическая боль.
Таким образом, нами разработаны протоколы диагностики и лечения больных с тревожно-депрессивными состояниями. Своевременная диагностика и терапия в группе риска по тревоге у пациентов с повреждениями ЛС позволяет ускорить сроки реабилитации и улучшить функциональные результаты этих пациентов.
