Введение. На повреждения коленного сустава (КС) приходится до 25% всех повреждений опорно-двигательного аппарата [13, 20]. С ростом популярности активного отдыха, развитием игровых и экстремальных видов спорта увеличивается и частота травм КС [10].
Повреждения связочного аппарата занимают первое место и составляют до 50% среди травм КС. У спортсменов частота внутрисуставных повреждений КС достигает 75% от общего числа травм. Из них на повреждение крестообразных связок приходится до 92%, а на повреждения менисков - до 84% [11].
Застарелые повреждения гиалинового хряща, менисков и крестообразных связок достигают 79%, что является причиной развития дегенеративно-дистрофических изменений в КС, снижает качество жизни пациентов и приводит к нетрудоспособности [10].
Успех в лечении внутрисуставных повреждений КС зависит от своевременной эффективной диагностики [11, 12, 25]. В настоящее время для исследования внутрисуставной патологии используется рентгенография, УЗИ, КТ, МРТ.
Наиболее информативным методом определения патологии внутрисуставных структур КС является артроскопия (АС) [9]. Проводя непосредственную визуализацию, пальпацию и оценку функции вовлеченных в патологический процесс структур можно установить связи между конкретными повреждениями с их клиническими проявлениями, получить наиболее достоверную информацию [1]. Однако артроскопия выполняется с диагностической целью крайне редко, и даже с целью лечения повреждений КС лишь у 20% пациентов!
В последние годы для диагностики патологии внутрисуставных структур КС широко используется УЗИ. Оно неинвазивно, экономично по сравнению с МРТ, позволяет выполнять многоплоскостное сканирование, оценивать и структуру и функцию внутрисуставных структур с учетом клинических проявлений, проводить многократные исследования для мониторинга выявленных ранее изменений [11]. Но к недостаткам метода можно отнести высокую операторозависимость [21].
Несмотря на успехи в совершенствовании методов исследования удельный вес диагностических ошибок достигает 83% [1, 11, 14, 18, 22, 32]. На амбулаторном этапе лишь у 20-23% пациентов с травмой КС устанавливается правильный диагноз [10]. 45% пациентов поступает в стационары с застарелыми повреждениями связок и хронической нестабильностью. Из них только у 20-40% амбулаторно поставлен верный диагноз [19].
Проведено немало исследований с целью определения диагностических возможностей ультразвуковой диагностики внутрисуставной патологии КС, однако единого мнения относительно эффективности сонографии нет. По разным данным точность УЗИ варьирует от 61 до 84% [20, 28]. До сих пор при интерпретации ультрасонограмм возникают затруднения в использовании классификаций повреждений внутрисуставных структур КС. Сохраняются разногласия в отношении достоверности дифференциально-диагностических признаков патологии отдельных внутрисуставных структур КС; нередко имеются несоответствия заключений нескольких специалистов ультразвуковой диагностики при обследовании КС у одного и того же пациента, особенно в отношении повреждений передней крестообразной связки и менисков.
В связи с этим возникает вопрос: «Какова же истинная эффективность ультразвуковой диагностики патологии отдельных внутрисуставных структур коленного сустава?».
Цель нашей работы - с помощью артроскопической верификации и применения принципа обратной связи специалистов оценить истинную эффективность ультразвуковой дифференциальной диагностики патологии внутрисуставных структур коленного сустава.
В литературе мы не встретили работ по применению принципа обратной связи, т.е. взаимодействия специалистов с целью определения эффективности и улучшения качества ультразвуковой диагностики.
Материалы и методы. Нами проанализированы результаты обследования 400 коленных суставов у 392 пациентов с травматическим анамнезом, которые в период с 2006 по 2011 г. находились на оперативном лечении в ортопедическом отделении КБ №2 г. Ярославля. Среди обследованных было 173 мужчины и 219 женщин в возрасте от 14 до 76 лет. Исследовано 210 правых и 190 левых суставов в сроки от 5 дней до 6 месяцев с момента получения травмы.
Амбулаторно перед госпитализацией на артроскопию всем пациентам было выполнено УЗИ КС специалистом отделения функциональной диагностики НУЗ Дорожной Клинической Больницы на станции Ярославль ОАО «РЖД».
Специалисты, проводившие УЗИ и артроскопию, были постоянными (100% АС выполнены автором исследования).
Все наблюдения по временному принципу разделены на четыре группы: первые 100 изученных суставов составили 1-ю группу, каждые 100 последующих - 2, 3 и 4-ю группы соответственно. Характеристики сравниваемых групп по полу и возрасту пациентов статистически значимо не отличались.
УЗИ проводилось на сканере Philips EnVisor, линейным датчиком с частотой 10-12 МГц по стандартной методике в соответствие с принципами полипозиционности, контрлатерального сравнения и дополнялось функциональными тестами.
АС выполнялась по стандартной методике на оборудовании фирмы Karl Storz с использованием 30* оптики и набора инструментов. В ходе лечебной артроскопии мы проводили оценку достоверности данных УЗИ для каждой внутрисуставной структуры КС по отдельности.
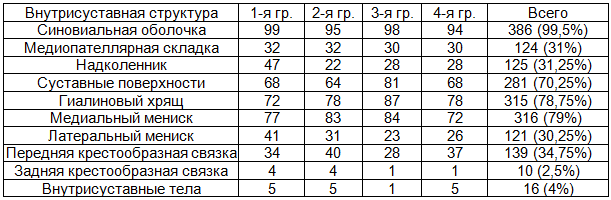
Среди выявленных изменений внутрисуставных структур доминировала патология синовиальной оболочки - 386 (96,5%), гиалинового хряща - 315 (78,75%), разрывы медиального мениска - 316 (79%), структурные изменения суставных поверхностей бедренной и большеберцовой костей - 281 (70,25%). Реже диагностировали патологию надколенника - 125 (31,25%), патологическую медиопателлярную складку - 124 (31%), повреждения передней крестообразной связки - 139 (34,75%) и разрывы латерального мениска - 121 (30,25%), в единичных наблюдениях - внутрисуставные тела и повреждения задней крестообразной связки (табл. 1).
Таблица 1. Структура выявленной внутрисуставной патологии КС
Осуществляя артроскопическую верификацию данных УЗИ, мы использовали принцип обратной связи, т.е. взаимодействия специалистов по артроскопии и лучевой диагностике, который заключался в само и взаимообучении (доктор лучевой диагностики изучал специализированную литературу и видеоматериалы по диагностической артроскопии, семиотике и классификации повреждений внутрисуставных структур КС с целью формирования правильного представления о возможной анатомической картине внутрисуставных повреждений с последующей правильной их лучевой интерпретацией; специалист по артроскопии изучал литературу по ультразвуковой диагностике, чтобы понимать, как конкретный вид повреждения внутрисуставных структур КС может быть описан в протоколе УЗИ на «лучевом» языке; доктора присутствовали во время проведения исследований друг у друга). Также принцип обратной связи заключался в совместном выяснении и устранении возможных причин несоответствия данных АС и УЗ диагностики и внесении изменений в протокол УЗИ в соответствии с классификациями повреждений отдельных внутрисуставных структур КС.
Результаты сравнения данных УЗИ и АС мы разделили на группы соответствия, когда данные УЗИ совпадали с артроскопическими, и несоответствия, когда данные УЗИ не совпадали с артроскопическими.
В группе соответствия мы разделяли результаты на истинно положительные, где патология, выявленная при УЗИ, подтвердилась во время АС диагностики, и истинно отрицательные, когда патологии не было обнаружено как при УЗИ, так и во время АС.
В группе несоответствия мы также разделяли ложно положительные, когда патология, выявленная во время УЗ диагностики, не подтвердилась при АС исследовании, и ложно отрицательные результаты, где патология при УЗИ не определялась, но была выявлена во время АС диагностики.
В процессе нашего исследования процент соответствия данных АС и УЗИ по патологии основных ВСС КС увеличился. Полное соответствие артроскопических и ультразвуковых диагнозов возросло с 38% до 75%. Процент несоответствия данных артроскопической и ультразвуковой диагностики снизился.
Для оценки результатов и сравнения их с данными литературы, в каждой группе исследования, по стандартной методике мы рассчитали показатели, наиболее часто используемые в оценке эффективности диагностических мероприятий: чувствительность, специфичность, точность, прогностическая ценность положительного (ПЦПТ) и отрицательного тестов (ПЦОТ) [4].
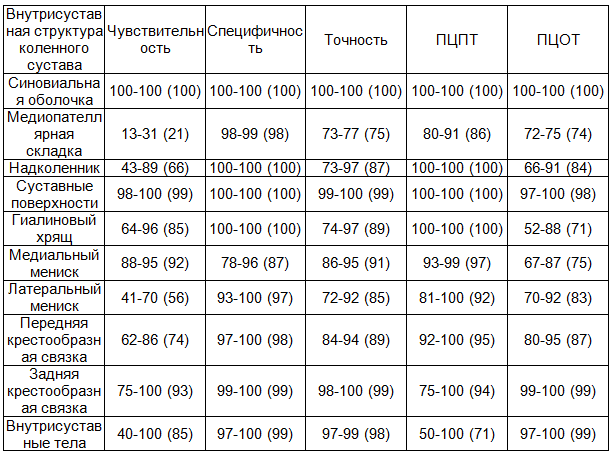
Результаты и обсуждение. Мы обратили внимание на то, что диагностическая эффективность УЗИ для отдельных внутрисуставных структур КС различна. Поэтому мы оценили эффективность УЗ диагностики дифференцированно, для каждой внутрисуставной структуры по отдельности. Показатели информативности УЗИ достигли своего максимума в 3-й и 4-й группах (табл. 2).
Таблица 2. Показатели (в %) эффективности УЗИ в оценке патологии отдельных внутрисуставных структур КС (диапазон (min-max) и средняя величина (М)
В связи с тем, что количество наблюдений с повреждением задней крестообразной связки и наличием внутрисуставных тел было небольшим (табл. 1), наши данные по указанным нозологиям имеют лишь относительную статистическую значимость.
В литературе представлены различные мнения относительно диагностической эффективности УЗИ в оценке состояния отдельных внутрисуставных структур.
Так, в исследовании [16] чувствительность и специфичность УЗИ в диагностике синовита составила 70,2 и 87% соответственно. Аналогичные показатели при верификации поражений гиалинового хряща составили 83,2 и 76,5%, а в работе [7] они оказались немного выше - 92,2 и 83,2% .
По данным [11], информативность сонографии в диагностике повреждений костных структур, синдрома медиопателлярной складки сведена к минимуму: показатель специфичности УЗ диагностики болезни Кенига составляет 20%, субхондральных переломов, хондромаляции надколенника и мыщелков бедренной и большеберцовой костей - 0%.
В исследованиях [20] по артроскопической верификации данных УЗИ применительно к повреждениям медиального мениска чувствительность ультразвукового метода составила 89%, специфичность - 64%, точность - 74%, ПЦПТ - 62%, ПЦОТ - 96%. В диагностике повреждений латерального мениска УЗ метод показал хорошие результаты с чувствительностью 78%, специфичностью 90%, точностью 87%, ПЦПТ 81% и ПЦОТ 90%. При травматических изменениях гиалинового хряща в доступных для эхолокации областях показатели составили 66%, 97%, 89%, 88% и 89% соответственно. Относительно патологии суставных поверхностей бедренной и большеберцовой костей точность УЗИ в доступных для локации зонах составила 89%, ПЦПТ - 88%, ПЦОТ - 89%. Чувствительность УЗИ диагностики патологической медиопателлярной складки составила 28%, точность - 87%, ПЦПТ - 66%.
Сравнительный анализ данных УЗИ и результатов инвазивных методов исследования, проведенный С.П. Мироновым и соавт. [18], продемонстрировал высокую чувствительность (93,7-96%) и специфичность (80-100%) УЗ диагностики патологии менисков. Точность УЗИ в верификации повреждений медиального мениска составила 62%, латерального мениска - 55%. Между тем, в исследовании [3] чувствительность и специфичность УЗИ применительно к повреждениям латерального и медиального мениска у больных без перелома костных структур составила 61% и 93% соответственно, а у больных остеоартрозом КС - 85% и 91% соответственно.
Литературные данные об эффективности УЗ диагностики повреждений передней крестообразной связки противоречивы. Ряд авторов полагает, что из-за невысокой чувствительности использование УЗИ для выявления патологии ПКС ограничено [31-33]
В то же время, по данным [9, 12, 20, 24, 29, 30, 33] чувствительность метода варьирует от 66 до 95%, специфичность - от 90 до 98%, точность - от 79 до 83,2%, ПЦПТ - от 66 до 98,2%, ПЦОТ - от 84,3 до 96%. Чувствительность и специфичность УЗ диагностики повреждений крестообразных связок у больных без перелома костных структур составляет 10 и 84%, а у пациентов с остеоартрозом - 47 и 85% соответственно [3]. Показатели чувствительности, специфичности и точности УЗИ для пациентов с повреждениями ЗКС составляют 87,5%, 100% и 98,5% соответственно; для выявления внутрисуставных тел специфичность метода составляет 66,7% [3].
В ходе настоящего исследования удалось достичь высоких показателей эффективности сонографии, причем отмечалась положительная динамика параметров диагностической ценности УЗИ в верификации патологии синовиальной оболочки, надколенника, в доступных локации зонах суставных поверхностей бедренной и большеберцовой костей, в доступных локации областях гиалинового хряща, латерального и медиального менисков, что свидетельствует об эффективности примененного нами принципа обратной связи специалистов и является доказательством высокой эффективности УЗ диагностики внутрисуставной патологии КС.
Мы попытались определить и устранить возможные ошибки артроскопической и УЗ диагностики. Причины несоответствия данных АС и УЗ диагностики, по нашему мнению, можно разделить на объективные (обусловленные особенностями методов диагностики) и субъективные (обусловленные действиями специалистов, проводящих исследование).
К объективным причинам мы отнесли:
- конституциональные и посттравматические особенности анатомии КС. Вследствие глубокого расположения ПКС визуализируется только её дистальный фрагмент, а при ограничении максимальной флексии КС по причине синовита, гипертрофии жирового тела, болевого синдрома эхолокация её ёще более затруднена. Повреждение ПКС не определяется при УЗИ, когда культя связки находится в анатомичном положении, или на её месте располагается крупная инфрапателлярная синовиальная складка. УЗ визуализация глубоко расположенных ВСС может затрудняться выраженным подкожно-жировым слоем, отёком сустава, а также избыточным количеством синовиальной жидкости. Напротив, структурные изменения синовиальной оболочки дифференцируются лучше при наличии внутрисуставного выпота.
- Физические особенности методов исследования.
Из особенностей УЗИ это эффект анизотропии, по причине которого естественные гипоэхогенные зоны в структуре менисков и связок ошибочно могут интерпретироваться врачом лучевой диагностики как зоны повреждения. Это ограниченная проникающая способность УЗ луча (ультразвук не проникает через костную ткань, не огибает суставные поверхности, поэтому визуализация гиалинового хряща, суставных поверхностей бедренной и большеберцовой кости, обращенные в межмыщелковую область, а так же большая часть суставной поверхности наколенника затруднена). Суставные поверхности большеберцовой кости визуализируются только в периферических сегментах, а также межмыщелковое возвышение. Основные зоны лучевой оценки толщины и структуры гиалинового хряща располагаются по передней и задней поверхности нагружаемых зон мыщелков бедренной кости при сгибании КС под углом 70-90о. По причине затухания сигнала в глубине эхолокации имеются ограничения в визуализации свободного края менисков и ПКС. Необходимо использовать исключительно высокочастотные датчики с частотой 7-12 МГц, оптимальных режимов сканирования, что позволяет лоцировать неполные повреждения и дегенеративные изменения менисков в «красной» зоне, дистального сегмента ПКС, тогда как эндоскопически возможно обнаружить дегенеративные изменения мениска лишь в «белой» зоне. На УЗ сканерах с малой разрешающей способностью невозможно достичь четкой дифференцировки гиалинового хряща, что не позволяет эффективно оценить его структуру.
Из ограничений АС необходимо отметить сложность эндоскопической визуализации заднего рога медиального мениска, заднего отдела сустава, дистального сегмента ЗКС, проксимальных неполных повреждений ПКС с сохранением нормальной её топографии, невозможность диагностики неполных и дегенеративных повреждений менисков.
- К объективным причинам несоответствия данных можно отнести отсутствие единой АС и УЗ классификация повреждений внутрисуставных структур КС, что не позволяет практическому врачу и специалисту лучевой диагностики разговаривать на одном, понятном для обоих, языке; отсутствие чётких количественных критериев УЗ оценки повреждений менисков, гиалинового хряща, поэтому проводится только субъективная оценка структурных изменений без использования более объективных критериев.
К субъективным причинам несоответствия данных АС и УЗ диагностики, по нашему мнению, можно отнести:
- недооценку клинической информации и невнимательность специалистов во время проведения диагностики;
- незнание особенностей анатомии КС (например, анатомическое «окно» сухожилия подколенной мышцы в области заднего рога латерального мениска может интерпретироваться врачом лучевой диагностики как его повреждение, крупная культя передней крестообразной связки - как новообразование, параартикулярные оссификаты могут приниматься за внутрисуставные тела);
- неверное использование терминологии и классификаций повреждений внутрисуставных структур КС в протоколе УЗИ;
- субъективность в оценке функциональных тестов во время УЗ диагностики без контралатерального сравнения, а большая часть врачей вообще их не проводят;
- несоблюдение методики полипозиционного сканирования;
- незнание эффекта анизотропии, когда естественные гипоэхогенные зоны в структуре менисков и связок интерпретируются врачом УЗ диагностики как участки их повреждения.
Заключение. Благодаря использованию принципа обратной связи в работе специалистов по артроскопии и ультразвуковой диагностике количество диагностических ошибок уменьшилось, что позволило получить максимально возможные показатели эффективности ультразвуковой дифференциальной диагностики патологии внутрисуставных структур коленного сустава.
Ультразвуковой метод исследования эффективен в диагностике патологии синовиальной оболочки, надколенника, суставных поверхностей бедренной и большеберцовой костей, гиалинового хряща, медиального и латерального мениска, задней крестообразной связки, что позволяет широко использовать его в качестве первичного метода диагностики повреждений внутрисуставных структур КС, а также для мониторирования выявленных изменений. Исключение составляют недоступные для эхолокации сегменты передней крестообразной связки, гиалинового хряща, суставных поверхностей.
Поскольку диагностическая эффективность УЗИ для отдельных внутрисуставных структур КС различна, то для выбора оптимальной тактики лечения практическим врачам необходимо учитывать показатели эффективность УЗД для каждой внутрисуставной структуры по отдельности.
УЗИ должно выполняться специалистом, имеющим большой опыт работы с костно-суставной патологией и понимание особенностей анатомии и клинических признаков патологических изменений внутрисуставных структур КС, непременно высокочастотными датчиками (7-12 МГц) с использованием оптимальных режимов сканирования и проведением функциональных тестов обязательно в сравнении с контрлатеральной стороной.
УЗИ будет иметь максимальную информативность при отсутствии факторов, затрудняющих эхолокацию, а именно синовита, отёчного, болевого синдрома, а также ограничения сгибания КС, поскольку при этом визуализация ПКС, суставных поверхностей, проведение функциональных тестов затруднены.
Описательную часть протокола УЗИ целесообразно формулировать на лучевом языке с подробным описанием эхоструктуры каждого внутрисуставного анатомического образования, а заключение - на травматологическом, с использованием классификаций повреждений менисков, связок, хрящевого покрова с целью адекватного восприятия этой информации практическими врачами.
С этой же целью в протокол УЗИ необходимо включить анатомическую схему КС, где врач лучевой диагностики будет отмечать локализацию и объём выявленных внутрисуставных патологических изменений, что улучшит восприятие полученной информации.
Не только внедрение в практику новых методов обследования, наличие современного оборудования, но и непрерывное само- и взаимообучение специалистов позволит достигнуть максимальной эффективности диагностических мероприятий.
