Введение. Метаболический синдром (МС) - комплекс метаболических, гормональных и клинических нарушений, в основе которых лежит инсулинорезистентность и компенсаторная гиперинсулинемия [8]. В индустриальных странах распространённость МС среди населения старше 30 лет составляет 10-20%, в США — 25%. Расчеты экспертов предполагают, что к 2025 г. число страдающих этим недугом во всем мире составит 300 млн. человек. Одним из важных аргументов изучения МС является его атерогенный потенциал. Согласно данным скандинавского исследования Kuopio Ischaemic Heart Disease Risk Factor Study, среди больных с МС риск развития ишемической болезни сердца (ИБС) в 3–4 раза выше, смертность от ИБС в 3 раза выше по сравнению с пациентами без метаболических нарушений [9]. Не менее важным осложнением МС является сахарный диабет 2 типа. Оказалось, что риск развития сахарного диабета в течение 5 лет у лиц с МС и преддиабетом оказался самым высоким — 40%, что в 2,5 раза выше по сравнению с группой больных с преддиабетом без МС [10]. С учетом высокого риска сердечно-сосудистых осложнений МС должен рассматриваться как серьезная медико-социальная проблема.
При МС имеет место перегрузка организма калориями, гиподинамия, нарушения метаболизма, не вызывает сомнения факт патофизиологической гетерогенности МС, с преобладанием ИР. Каждый из вышеперечисленных факторов, изолированно или в совокупности, инициирует процесс апоптоза [4]. Апоптоз - программированная клеточная гибель, энергетически зависимый, генетически контролируемый процесс, который запускается специфическими сигналами и избавляет организм от ослабленных, ненужных или повреждённых клеток [3]. Апоптоз в последние годы стал предметом интенсивных исследований. Это говорит о понимании роли данного процесса не только в судьбе отдельных клеток и тканей, но и его значении в возникновении и развитии ряда заболеваний, в том числе и процессах старения. Звеном, регулирующим запуск процесса апоптоза, является белок р53. Высокая активность протеина р53 приводит к процессам преждевременного старения [7]. Преждевременное старение способствует раннему развитию возрастной патологии - ИБС, артериальной гипертонии, онкологических заболеваний, сахарного диабета 2–го типа, а возникновение болезней ускоряет темп старения человека [1].
Одной из основных задач современной профилактической медицины является увеличение продолжительности активной жизни индивидуума. Создаются и внедряются в практику препараты, способные увеличивать продолжительность жизни, получившие название геропротекторы. На данный момент ни один геропротектор не представил неоспоримой доказательной базы по своей эффективности. В проводимых нами ранее исследованиях была установлена взаимосвязь между процессом инсулинорезистентности и концентрацией белка р53 [6]. Одним из препаратов, способных уменьшить инсулинорезистентность, является сиофор (метформин). На основании этого сформулирована цель исследования.
Цель исследования: Изучить воздействие препарата сиофор (метформин) на процесс апоптоза у пациентов с метаболическим синдромом.
Материал и методы. Диагностика МС была основана на критериях, предложенных экспертами Всероссийского общества кардиологов (2009) [2]. Критериями исключения из исследования являлись: возраст старше 60 и моложе 30 лет, хронические заболевания в стадии обострения, тяжелая неконтролируемая артериальная гипертензия, аутоиммунные заболевания, заболевания системы крови, острые бактериальные и вирусные инфекции в ближайшие 3 месяца, злокачественные новообразования, беременность, декомпенсация сахарного диабета 2-го типа, сахарный диабет 1- го типа, гипотиреоз, тиреотоксикоз, прием глюкокортикоидов, давность хирургического вмешательства менее 6 месяцев.
Первоначально в исследование было включено 70 человек с МС в возрасте от 30 до 60 лет - 49,00 (41,00; 54,00) лет. Все пациенты дали информированное согласие на участие в исследовании. До конца исследования прием препарата продолжили только 62 пациента в возрасте 48 (39,0; 53,0) лет, их них 41 (66%) мужчина и 21 (34%) женщина. Группу контроля составили 70 человек без признаков МС, сопоставимых по возрасту 47,0 (40,0; 52,0) лет и полу (40 мужчин – 57,14% и 30 женщин – 42,86%) с больными.
Всем пациентам проводили антропометрическое обследование (измерение роста (м), массы тела (кг), окружности талии (ОТ) и окружности бедер (ОБ) (см), отношения окружности талии к окружности бедер (ОТ/ОБ); индекса массы тела (ИМТ) = вес/рост² и биохимическое исследование крови, взятой утром натощак после 12 часов голодания. В исследование углеводного обмена входило определение глюкозы (ммоль/л) натощак, уровня инсулина сыворотки крови (мкЕд/мл) с помощью набора «Insulin AccuBind Elisa» методом ИФА, рассчитывали индекс ИР по формуле (HOMA-IR)=глюкоза (ммоль/л) * инсулин (мкЕд/мл)/22,5. Повышение данного показателя более 2,77 свидетельствует о наличии ИР. Выявление артериальной гипертонии осуществлялось путем офисного измерения артериального давления по методу Короткова с соблюдением соответствующих рекомендаций ВНОК (мм.рт.ст.). Липидный спектр сыворотки оценивали по содержанию общего холестерина (ОХС) (ммоль/л), триглицеридов (ммоль/л), холестерина липопротеидов высокой плотности (ХС ЛПВП) (ммоль/л), холестерина липопротеидов низкой плотности (ХС ЛПВП) (ммоль/л). Холестерин липопротеиов очень низкой плотности (ХС ЛПОНП) вычисляли по формуле Фридвальда: ХС ЛПОНП = ОХС – ХС ЛПНП – ХС ЛПВП. Коэффициент атерогенности (КА) рассчитывали по формуле = (ОХС – ХС ЛПВП) / ХС ЛНВП. Процесс апоптоза оценивали по концентрации белка p53 сыворотки крови (U/мл) с помощью набора фирмы Bender MedSystems (Австрия) методом ИФА.
В табл. 1 представлена сравнительная характеристика пациентов с МС и группы контроля.
Таблица 1. Сравнительная характеристика показателей пациентов с метаболическим синдромом и группы контроля
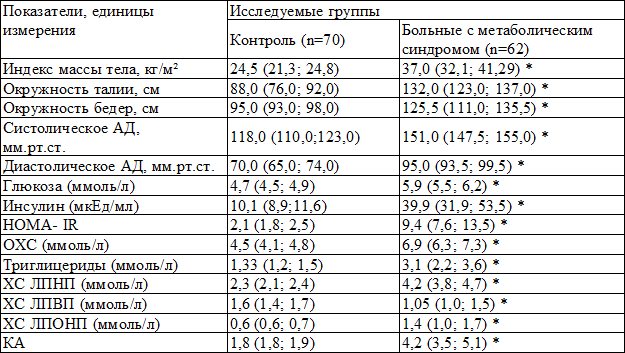
Примечание: * р<0,05- при сравнении исследуемой группы и контроля
Всем пациентам были даны рекомендации по питанию: питание должно быть частым, малыми порциями при суточной калорийности пищи не более 1500 ккал; последний прием пищи – за полтора часа до сна. Основа питания – сложные углеводы с низким гликемическим индексом, они должны составлять до 50–60% пищевой ценности. Кроме этого, были даны разъяснения по поводу ведения правильного образа жизни с изменением пищевых привычек и дозированных физических нагрузок. Лечение сиофором (фирма «Berlin-Chemie», Германия) начинали с 500 мг в сутки в течение недели (для минимизации проявления побочных эффектов со стороны желудочно – кишечного тракта), с последующим доведением дозы до 1700 (850 мг два раза в день) мг в сутки в течение года. Прием препарата продолжался на протяжении года с контролем всех показателей через 3, 6, 9 и 12 месяцев.
Статистический анализ результатов проводили на IBM с помощью пакета программ STATISTICA 7,0 (StatSoft, версия 7, USA). Распределение показателей отличается от нормального, поэтому данные представлены в виде Me (LQ;UQ), где Ме – медиана – центральное значение признака в выборке, справа и слева от которого расположены равные количества объектов исследования; LQ – нижний квартиль; UQ – верхний квартиль. Межгрупповые отличия оценивали непараметрическим критерием Манна – Уитни. Различия считались достоверными при уровне значимости р<0,05.
Результаты. Содержание белка р53 в сыворотке крови пациентов с МС 1,85 (1,72; 2,2) U/мл, в контрольной группе 0,96 (0,91; 0,99) U/мл, р<0,05. Уровень инсулина сыворотки крови при МС достиг 46,8 (37,2; 59,4) мкЕд/мл, в группе контроля 10,1 (8,9; 11,6) мкЕд/мл, р<0,05. Индекс HOMA – IR 14,3 (9,4; 16,1) и 2,1 (1,8; 2,5) соответственно, р<0,05.
У пациентов с МС процесс апоптоза интенсифицирован, о чем свидетельствует увеличение белка р53 почти в 2 раза по сравнению с контрольной группой. Уровень инсулина сыворотки крови в 4 раза выше, чем в группе контроля. Индекс инсулинорезистентности в 5,2 раза превышает нормальные величины.
В результате приема метформина отмечена положительная динамика исследуемых показателей (табл. 2).
Таблица 2. Динамика показателей белка р53, инсулина и индекса HOMA-IR на фоне приема метформина при метаболическом синдроме
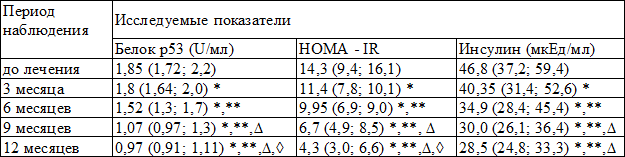
Примечания: * - р<0,05 достоверность различий показателей всех временных интервалов по сравнению с параметрами до лечения, ** - через 3 месяца лечения и остальными временными интервалами, ∆ - через 6 месяцев и 9; 12 месяцев, ◊ - через 9 месяцев и 12 месяцев
Прием метформина привел к тому, что уровень белка р53 за 12 месяцев достиг уровня показателей контрольной группы - 0,97 (0,91; 1,11) U/мл. Статистически значимые изменения белка р53 возникают уже через 3 месяца приема метформина и сохраняются во всех временных интервалах. По индексу инсулинорезистентности имеет место аналогичная ситуация. Уровень инсулина в сыворотке крови не имеет статистически значимых отличий между 9 и 12 месяцами приема, показатели в остальных временных интервалах статистически значимы.
Обсуждение. При проведении корреляционного анализа у пациентов с МС выявлены сильные положительные связи между концентрациями белка р53 и инсулина, содержанием белка р53 и HOMA–IR - (r+0,72, р<0,05); (r+0,81, р<0,05), соответственно. Инсулинорезистентность и гиперинсулинемия, лежащие в основе МС, ускоряют процессы старения, в данном случае, путем увеличения концентрации индуктора апоптоза – белка р53, высокая концентрация которого является маркером преждевременного старения. Этот факт нашел подтверждение в нашем исследовании, проводимом ранее: биологический возраст и коэффициент скорости старения у пациентов с МС увеличены [5]. В свою очередь, ускоренный темп старения организма определяет повышенный риск раннего развития возрастной патологии, влияя на качество и продолжительность жизни.
На основании вышеизложенных фактов назначение метформина у пациентов с МС весьма обоснованно. Метформин не только непосредственно воздействует на инсулинорезистентность, как пусковой механизм преждевременного старения, но и обладает рядом благоприятных кардиоваскулярных и метаболических эффектов. Снижение инсулинорезистентности происходит за счет восстановления чувствительности тканей к инсулину путем: увеличения количества аффинных к инсулину рецепторов, через стимуляцию тирозинкиназы повышается активность инсулиновых рецепторов, активизируются экспрессия и перемещения из внутриклеточного пула на клеточную мембрану транспортеров глюкозы. Вышеперечисленные процессы приводят к увеличению поглощения глюкозы органами-мишенями инсулина - печенью, скелетной мускулатурой, жировой тканью. Метформин замедляет процесс всасывания углеводов в желудочно–кишечном, стабилизирует и уменьшает массу тела, а также снижение отложения висцерального жира, подавляет повышенную адгезию моноцитов к эндотелию сосудов, тем самым, влияет на пусковые механизмы развития атеросклеротического поражения. Следует отметить, что в настоящее время рациональная терапия МС метформином, обладающим благоприятным спектром фармакологических эффектов, в сочетании с нефармакологическими методами, является эффективным способом коррекции инсулинорезистентности и позволяет существенно повлиять на качество жизни пациентов. В результате приема метформина за 12 месяцев концентрация белка р53 в сыворотке крови снизилась с 1,85 (1,72; 2,2) U/мл до 0,97 (0,91; 1,11) U/мл.
Заключение. Метформин обладает геропротекторными свойствами в отношении апоптотической активности сыворотки крови пациентов с метаболическим синдромом, что позволяет рекомендовать его назначение для коррекции данного процесса.
