В современной медицинской литературе метаболический синдром (МС) рассматривается как важная медико-социальная проблема, охватывающая до 25% взрослого населения. Основными диагностическими критериями МС, согласно данным Национальной образовательной программы США (Adult Treatment Panel III (ATP III 2001 г.) являются: абдоминальное ожирение (ИМТ≥30, ОТ≥80), гипергликемия натощак (≥6,1 ммоль/л), гипертриглицеридемия (≥1,7 ммоль/л), снижение уровня антиатерогенной фракции липопротеидов высокой плотности (ЛПВП≤1,3 ммоль/л), АД≥130/85 мм рт.ст., микроальбуминурия (≥30 мг/г) [21;27]. Кроме того, в последнее время высказывается мнение, что неалкогольная жировая болезнь печени должна быть включена в диагностические критерии метаболического синдрома, что связано с высокой частотой ее встречаемости у пациентов с МС [2; 4; 8; 27].
Неалкогольная жировая болезнь печени (НЖБП) как самостоятельная нозологическая единица была выделена в 1980 г. [26]. Было отмечено, что у пациентов с избыточной массой тела и СД 2 типа, не употребляющих алкоголь в гепатотоксических дозах, выявляются изменения сходные с картиной ее алкогольного поражения [26].
Истинная распространенность НЖБП неизвестна, что связано с малосимптомным течением болезни и отсутствием четких объективных критериев постановки диагноза. В США на долю НЖБП приходится 69% хронических диффузных болезней печени. При избыточной массе тела различные формы НЖБП выявляют у 58-74%, а при морбидном ожирении – у 95% больных [12].
По некоторым данным распространенность НЖБП и ее основных нозологических форм – стеатоза и неалкогольного стеатогепатита в популяции взрослого населения России очень высока и составляет 27%, 21,7% и 4,5% соответственно [20]. Так, при ожирении стеатоз печени развивается в 95–100% случаев и сопровождается стеатогепатитом в 20–47% пациентов. Тяжесть нарушения обмена глюкозы коррелирует с тяжестью поражения печени: стеатоз печени развивается у 60% больных, страдающих СД типа 2, а стетогепатит развивается у ¼ из них. Гиперлипидемия отмечается у 35–80% пациентов с неалкогольным стеатогепатитом.
Этиология НЖБП.
К этиологическим факторам, приводящим к развитию вторичного стеатогепатита и НЖБП, относятся [17]:
- быстрое похудение;
- синдром избыточного бактериального роста;
- синдром мальабсорбции как следствие оперативных вмешательств на тонкой кишке, заболеваний тонкого кишечника;
- длительное парентеральное питание;
- лекарственные препараты (глюкокортикоиды, эстрогены, нестероидные противовоспалительные препараты, тетрациклин, амиодарон).
Патогенез развития НЖБП.
Установлено, что в основе формирования НЖБП лежит патологические внутри- или внеклеточное отложение капель жира. C.Day и O.James была предложена и доказана теория «двух толчков», согласно которой на 1-м этапе происходит избыточное поступление липидов в гепатоциты с формированием стеатоза (первый толчок), с дальнейшим развитием воспаления и стеатогепатита (2-й толчок) [11].
Согласно последним научным концепциям, ведущую роль в патогенезе НЖБП отводят нарушению углеводного и липидного обмена, а в качестве момента, запускающего каскад метаболических нарушений, рассматривают инсулинорезистентность.
Начальным звеном развития НЖБП является накопление в цитоплазме гепатоцитов липидов, в первую очередь триглицеридов. Считается, что это нарушение обмена липидов обусловлено ИР, причем на ранних стадиях болезни большее значение имеет печеночная ИР – состояние, характеризующееся высоким содержанием инсулина в портальной, но не в периферической крови. ИР рассматривается как сложный патологический процесс, сопровождающийся компенсаторной гиперинсулинемией. Гиперинсулинемия вызывает повышенный липолиз, приводит к неконтролируемому глюконеогенезу, влияет на строение и функционирование митохондрий. Кроме того, гиперинсулинемия стимулирует избыточный липогенез, нарушает окисление жирных кислот, снижает выведение из гепатоцитов липопротеидов очень низкой плотности. Все это приводит к накоплению капель триглицеридов и других липидов в паренхиме печени и развитию апоптоза гепатоцитов [8].
При висцеральном ожирении активизируются процессы периферического липолиза, что приводит к повышению продукции свободных жирных кислот (СЖК), которые через систему воротной вены поступают в печень и приводят к возникновению стеатоза печени. Наряду с этим в печеночных клетках снижается образование гликогена, усиливаются процессы гликогенеза и глюконеогенеза. Длительно существующее повышение СЖК в гепатоците обусловливает истощение функциональной способности митохондрий, индуцирует микросомальное окисление липидов системой цитохрома Р450 2Е1 с образованием активных форм кислорода, а развивающийся при этом оксидативный стресс приводит к повышению выработки провоспалительных цитокинов с образованием воспалительной реакции в печени и формированием НАСГ [19].
Таким образом, патологическая цепочка, приводящая к развитию поражения печени выглядит следующим образом: МС → ИР и дислипидемия → стеатоз → воспаление + окислительный стресс → стеатогепатит →фиброз печени → цирроз печени [8].
Стеатоз проявляется накоплением жировых включений в гепатоцитах, преимущественно в виде триглицеридов, составляющих не менее 5% от массы печени. При сочетании стеатоза с воспалительно-некротическими процессами в печени можно говорить о развитии неалкогольного стеатогепатита (НАСГ) [13].
НАСГ является самостоятельной нозологической единицей и подразделяется на первичный и вторичный. Первичный ассоциируется с эндогенными нарушениями углеводного и липидного обмена (СД 2 типа, избыточная масса тела, гиперлипидемия), а вторичный чаще связан с внешними факторами, такими как синдром мальабсорбции, болезни накопления, синдром избыточного бактериального обсеменения тонкой кишки. Популяционные исследования свидетельствуют о том, что 60-80% криптогенного цирроза печени являются результатом НАСГ [13-15].
Клиническая картина заболевания неспецифична. Большинство пациентов не предъявляют жалоб, а при прицельном опросе удается выявить астенический и диспептический синдромы: быструю утомляемость, слабость, а также периодическую тяжесть, дискомфорт в левом подреберье, не имеющие четкой связи с какими-либо провоцирующими факторами. Нарастающие диспептические жалобы, кожный зуд, желтуха, признаки портальной гипертензии, малые печеночные знаки выявляются, как правило, при исходе стеатогепатита в цирроз печени. На этом этапе у 1/3 больных отмечают снижение мышечной массы, трудно распознающееся из-за ожирения [1, 2].
Увеличение размеров печени формируется у большей части пациентов, страдающих как стеатозом печени, так и стеатогепатитом. Край печени плотноэластический, закругленный, безболезненный. Часто выраженное ожирение затрудняет пальпацию печени. Увеличение в размерах селезенки более характерно для трансформации процесса в цирроз печени [15].
НЖБП характеризуется относительно доброкачественным течением со стабильным и, в большинстве случаев, не прогрессирующим течением. Однако у 20-40% больных НАСГ заболевание прогрессирует с развитием выраженного фиброза печени, у 20% из них в течение 20-ти лет формируется цирроз печени с развитием печеночно-клеточной недостаточности [3, 23].
Диагностика.
При подозрении на НЖБП прежде всего необходимо исключить следующие факторы, приводящие к поражению печени [9, 10, 16, 28, 29, 30]:
- повреждение печени токсической, лекарственной, вирусной (гепатит В и С), алиментарной природы;
- употребление этанола в гепатотоксичной дозе ≥21г (для женщин) и ≥40 г (для мужчин) в день в течение 1 года до исследования;
- сывороточное железо (10,7-30,4 мкмоль/л), трансферрин (2-4 г/л) и ферритин сыворотки крови, общая железосвязывающая способность крови (при наличии смуглых кожных покровов и гиперпигментации кожных складок);
- уровень церулоплазмина в плазме в пределах нормы и отсутствие колец Кайзера-Флейшера (для исключения болезни Вильсона-Коновалова);
- электрофорез белков сыворотки: альфа фракция глобулинов в пределах нормы (исключает дефицит альфа1-антитрипсина);
С целью верификации диагноза пациентам с выявленными диффузными изменениями паренхимы печени необходимо назначить [5, 6, 7, 31, 32]:
- Биохимическое исследование крови. Показатели биохимического исследования крови у пациентов со стеатозом не изменены. При НАСГ выявляется повышение уровня сывороточных трансаминаз и их соотношения АЛТ/АСТ ≥ 1. В случае выявления цитолитического синдрома и при исключении первичного повреждающего фактора, состояние пациента расценивается как стеатогепатит. Как правило, повышение уровня сывороточных трансаминаз не превышает 3–5 норм. Более характерно преобладание АЛТ над АСТ. Если же соотношение АСТ/АЛТ≥2, это можно рассматривать как неблагоприятный прогностический признак и высокую вероятность трансформации стеатогепатита в цирроз печени. Повышение гамма-глутамилтранспептидазы может быть как изолированным, так и сочетающимся с повышением щелочной фосфатазы. Обычно эти показатели увеличиваются не более чем в 2 раза по сравнению с нормой. Гипербилирубинемия за счет обеих фракций отмечается менее чем у ¼ больных и не превышает нормального значения более чем в 2 раза.
- УЗИ: позволяет верифицировать наличие гепатомегалии, косвенно оценить степень выраженности стеатоза печени и выявить признаки формирования портальной гипертензии. УЗИ признаками НЖБП являются диффузное увеличение яркости печеночной паренхимы (эхогенность печени выше, чем почек и селезенки), нечеткость сосудистого рисунка и дистальное затухание эхосигнала. Если содержание жира в печени превышает 30%, метод УЗИ характеризуется высокой диагностической точностью в выявлении НЖБП. Его специфичность достигает 89%, чувствительность 93%.
- Эзофагогастродуоденоскопия проводится для обнаружения варикозного расширения вен пищевода у пациентов с трансформацией стеатогепатита в цирроз печени.
- КТ – основным КТ признаком НЖБП является снижение рентгенологической плотности печени на 3-5 ед. (норма 50-75 ед.) при этом она меньше, чем рентгенологическая плотность селезенки, более высокая плотность внутрипеченосных сосудов и нижней полой вены по сравнению с плотностью печеночной ткани.
- МРТ: использование фазово-контрастного препарата позволяет определить количественное содержание жировой ткани.
- Биопсия печени и морфологическое исследование является золотым стандартом диагностики НЖБП и позволяет оценить некровоспалительную активность заболевания, степень стеатоза, стадию и распространенность фиброза печени.
В силу инвазивности процедуры выполнение биопсии печени на уровне поликлинического звена нецелесообразно, хотя именно гистологическая картина в ряде случаев позволяет сделать окончательный вывод о генезе и тяжести поражения печени.
Для стеатогепатита характерна крупнокапельная, а иногда и менее выраженная мелкокапельная жировая дистрофия гепатоцитов, поражающая преимущественно 3-ю зону ацинуса. Крупные одиночные липидные капли визуализируются в цитоплазме и смещают ядро к периферии клетки. Развивается баллонная дистрофия клеток. Могут обнаруживаться тельца Мэллори, однако, в меньшем количестве, чем при поражении печени алкогольного генеза. Воспалительные изменения представлены внутридольковыми инфильтратами, состоящими из лимфоцитов, мононуклеарных фагоцитов и полиморфно-ядерных лейкоцитов. Фиброзные изменения выявляются вначале в 3-й зоне ацинуса и могут прогрессировать с образованием септ и исходом в цирроз печени. Для унификации морфологической оценки степень активности и стадию фиброза выставляют на основании классификации Е. Вrunt (2000) [21, 22].
Таблица 1. Классификация Е. Вrunt
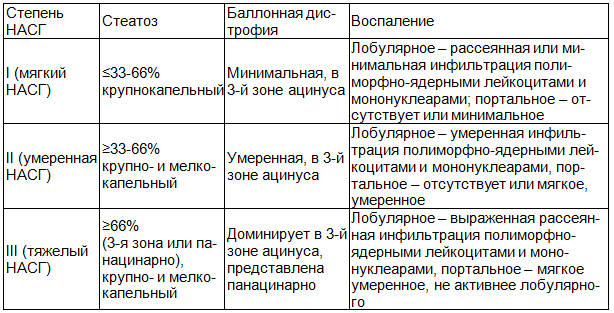
Терапия НЖБП
Существует вероятность обратного развития жировой дистрофии печени, НАСГ и даже НАСГ с трансформацией в цирроз печени на фоне плавного снижения массы тела (1,5-2 кг в мес.) и лекарственной терапии. Быстрая потеря массы тела способствует прогрессированию НЖБП с нарастанием степени выраженности стеатоза и фиброза печени [16, 18, 24, 25].
Таким образом, терапия НЖБП направлена на профилактику цирроза печени как исхода неалкогольного стеатогепатита.
Основными направлениями терапии у пациентов с НЖБП являются:
- полный отказ от приема алкоголя;
- снижение массы тела при ожирении;
- применение диеты с ограничением жиров и углеводов;
- адекватные физические нагрузки;
- нормализацию показателей углеводного, липидного и пуринового обмена;
- нормализацию состояния микробиоценоза кишечника.
Основополагающим является нормализация массы тела, что автоматически приведет к уменьшению выраженности инсулинорезистентности и позволит разорвать порочный круг болезни. Однако снижение массы тела не должно быть стремительным и превышать 1000 г в неделю, так как это приводит к ухудшению течения заболевания, повышению уровня трансаминаз в сыворотке крови, а также индекса гистологической активности НЖБП. В качестве инсулиносентитайзеров при лечении НЖБП в широкой клинической практике применяют бигуаниды (метформин). При применении метформина в течение 6 месяцев отмечается снижение активности или нормализации уровня трансаминаз, улучшение показателей липидного спектра, уменьшение массы тела. Положительная динамика биохимических показателей и уменьшение выраженности стеатоза отмечали также на фоне применения глитазонов 2-го поколения в течение 3–12 месяцев [2, 4, 10, 18].
С целью профилактики развития сердечно-сосудистых осложнений у пациентов с МС оправдано назначение липидоснижающих средств – статинов и периферических блокаторов липазы.
Как самостоятельное направление может рассматриваться применение «эссенциальных» фосфолипидов, как препаратов с доказанной мембранопротективной и гепатопротективной активностью.
Заключение. Таким образом, представленный краткий обзор свидетельствует о том, что проблемы метаболического синдрома в настоящее время вышли за рамки сердечно-сосудистой патологии и приобрели масштаб междисциплинарной патологии. Практически все компоненты метаболического синдрома являются факторами риска развития стеатоза и фиброза печени, что требует обязательного включения в алгоритм обследования тучных пациентов печеночных показателей и проведения терапии, направленной на улучшение метаболических процессов и предотвращения развития цирроза печени.
