Актуальность проблемы. Язвенная болезнь (ЯБ) относится к числу наиболее распространенных заболеваний и является важнейшей медико-социальной проблемой. Болезнь поражает людей в активном, творческом возрасте, часто становясь причиной временной и стойкой утраты трудоспособности [1-3]. Установление связи инфекции Helicobacter pylori (H.pylori) с гастродуоденальными заболеваниями (ГДЗ) позволила по-новому подойти к лечению ЯБ [9].
Уже почти 30 лет продолжается интенсивное изучение микроорганизма H. pylori. В 1997 г. были разработаны первые рекомендации Маастрихт-1, касающиеся диагностики инфекции, показаний для антихеликобактерной терапии [4, 30]. В дальнейшем в связи с получением новых данных о свойствах возбудителя, расширением спектра заболеваний были разработаны рекомендации Маастрихт-2 (2000) и Маастрихт-3 (2005) [2-6]. Последний пересмотр основного документа произошел в 2010 г. (Маастрихт-4) [1].
Для лечения хеликобактериоза рекомендованы следующие схемы лечения [7-8]:
-тройная стандартная терапия;
-последовательная терапия;
-квадротерапия без препаратов висмута;
-квадротерапия на основе препаратов висмута.
Современная фармакотерапия ЯБ включает различные группы лекарственных средств, действие которых направлено на основные звенья патогенеза ульцерогенеза. Однако эрадикационная терапия не предупреждает развития на месте язвенного дефекта рубцовой ткани, которая приводит к деформации стенки и стенозу [10-14]. Поэтому, патогенетическое лечение должно включать мероприятия, направленные на ускорение репаративных процессов слизистой оболочки двенадцатиперстной кишки (СОДПК). Применяемые в настоящее время методы эндоскопического лечения направлены в основном на защиту поверхности язвы от воздействия агрессивных факторов пищеварительных соков и стимуляции процесса регенерации [15], но они технически сложны в выполнении, обременительны для пациентов и, также не исключают развития рубцовой деформации слизистой оболочки (СО).
Хеликобактерная теория ульцерогенеза не решила в полной мере вопросы профилактического и противорецидивного лечения ЯБ. Высокая частота рецидивов и осложнений предопределяет необходимость поиска препаратов, направленных на сокращение сроков рубцевания, улучшение качества регенерации, повышение защитных свойств СО гастродуоденальной зоны, не обладающих побочными эффектами, не вызывающих привыкания и экономически доступных для пациентов [16-18].
В течение многих лет в медицине успешно применяются протеолитические ферментные препараты (ПФП) [19,20]. В качестве альтернативы традиционным подходам энзимотерапия находит широкое применение при лечении заболеваний различной этиологии. Клиническими и экспериментальными исследованиями установлен широкий спектр их фармакологической активности. ПФП обладают противовоспалительным, дегидратационным, антикоагуляционным, репаративным и опосредованным антибактериальным свойствами [21-24]. Среди них наибольшее распространение получили ферменты протеолитические, которые составляя систему протеолиза, играют существенную роль в таких важнейших биологических процессах, как обмен белков, свертывание крови, фибринолиз, иммунные реакции, регуляция артериального давления, процессы дифференциации и метаболизма соединительной ткани [25]. Ферменты выполняют важные защитные функции, обезвреживая как экзогенные, так и эндогенные токсические вещества [26].
Чрезвычайно важным представляется установленная способность иммобилизованных ПФП улучшать проникновение антибиотиков в очаг воспаления [27]. Так, при лечении гнойно-воспалительных раневых процессов, в качестве местного протеолитического средства применяется «Имозимаза», являющийся селективным некролитическим препаратом. В отличие от аналогичных лекарственных средств он нетоксичен и гипоаллергичен, обладает пролонгированным действием, быстро и эффективно очищает поврежденные ткани от денатурированных белков и создает благоприятные условия для регенерации [28-29].
Цель исследования - изучение процессов регенерации СО гастродуоденальной зоны при применении в комплексной терапии больных язвенной болезнью двенадцатиперстной кишки (ЯБДПК) препарата инзимол, полученного в результате иммобилизации бактериальных протеиназ на полиэтиленоксиде (ПЭО).
Материалы и методы исследования. В исследование были включены 105 больных с не осложненным течением ЯБДПК в стадии обострения. Среди них было 76 (72,4%) мужчин и 29 (27,6%) женщин в возрасте от 21 до 54 лет (средний возраст составил 32,2±2,8 года).
У больных ЯБДПК проводилось сравнительное изучение терапевтической эффективности эрадикационной и комбинированной терапии с применением ПФП инзимол. В зависимости от тактики лечения все больные были распределены с учетом таких факторов, как характер сопутствующей патологии, стадия заболевания, локализация язвы, что позволило провести сравнительную оценку сравниваемых параметров.
Дана оценка эффективности различных методов лечения. Все обследованные 105 больных ЯБДПК в соответствии с задачами исследования были рандомизированы на три группы.
I группа (n=50) больных - которым проводилась тройная стандартная терапия + дополнительно инзимол pеr os по 1 таблетке, содержащей 150ПЕ х 3 раза/день (курс лечения 10 дней);
II группа (n=26) больных, которым проводилась тройная стандартная терапия + дополнительно эндоскопические вливания инзимола по 150 ПЕ (в 10 мл дистиллированной воды) через день. Курс лечения составил в среднем 5 вливаний;
III группа - контрольная (n=29 больных), пролеченные только по тройной стандартной схеме эрадикации.
Для оценки структуры СО ДПК больных использовали морфологические методы исследования. Морфологические признаки оценивали по визуально-аналоговой шкале, предложенной Л.И. Аруиным.
На рис. 1-4 представлены морфологические изменения, обнаруженные в гистологических препаратах СОДПК обследованных больных:
1) отечность собственной пластинки, инфильтрация лимфоцитами, плазматическими клетками, единичными нейтрофилами; сгруппированные железы характеризуются расширенными протоками и плохой дифференцировкой клеток (рис. 1);
2) неравномерное утолщение ворсинок с булавовидными изменениями их дистальных отделов; дистрофия энтероцитов, полиморфно-клеточная инфильтрация стромы; деформация кишечных крипт; некрозы и местное слущивание покровного эпителия (рис. 2);
3) участки атрофии с кистозными расширениями крипт; инфильтрация лимфогистиоцитарными элементами; разрастание коллагеновых и мышечных волокон; деструкции базальных мембран эпителиальной выстилки (рис. 3);
4) изменения пилорических желез, местами окаймленные узкими темными полосками полулунной формы с расширенными протоками (рис. 4).
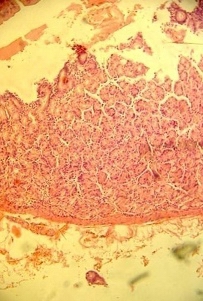
Рис. 1. Инфильтрация собственной пластинки СО. Окраска гематоксилин эозином. Увеличение х200
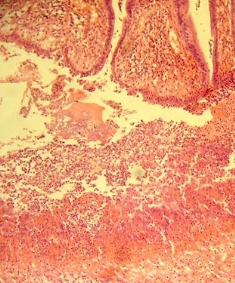
Рис. 2. Дистрофия энтероцитов, деформация кишечных крипт. Окраска гематоксилин эозин. Увеличение х200
Результаты проведенных эндоскопических исследований показали, что во всех 3-х изучаемых группах пациентов ЯБДПК выявлялись язвенный дефект различных размеров, изменения периульцерозной зоны с гиперемией, отеком, т.е. наблюдалось выраженное обострение заболевания. Визуальная картина воспалительного процесса была подтверждена морфологическим изучением биоптатов СОДПК. У всех обследованных выявлена различной степени активность дуоденита с характерными для ульцерозного процесса изменениями СОДПК и обсемененность инфекцией Н.рylori.
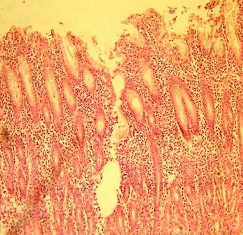
Рис. 3. Разрастание коллагеновых волокон, деструкция базальных мембран. Окраска гематоксилин эозином. Увеличение х200
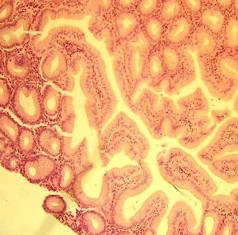
Рис. 4. Изменения пилорических желез. Расширение протоков желез. Окраска гематоксилин эозином. Увеличение х400
Результаты исследований. Динамика регенераторных процессов СО гастродуоденальной зоны при различных способах лечения: морфологический анализ прицельно взятых биоптатов показал, что после проведенного лечения, у больных I и II групп (у 92,7% и у 98,8% соответственно) отмечалась положительная динамика. Сравнительная характеристика структурных изменений СОДПК у исследуемых больных с разными методами лечения представлена в табл. 1.
Отличительной особенностью динамики изменений в СОДПК у больных I группы обнаруживались умеренно выраженные признаки воспаления только в единичных случаях. Все сравниваемые показатели после лечения имели достоверно высокие отличия (р<0,001) с аналогичными данными, полученными до начала лечения больных – в стадии обострения ЯБДПК. Только увеличение количества бокаловидных клеток и гипертрофия дуоденальных желез, как показатели сохраняющегося умеренно выраженного воспалительного процесса, наблюдались у 7 и 8 пациентов этой группы, но при этом достоверно (р<0,01) отличались от начальных показателей, выявленных до лечения. Инфильтрация всех слоев СО ДПК была умеренной, с преобладанием плазматических клеток. В покровном эпителии преобладали зрелые, дифференцированные клетки. Дистрофические изменения клеток (3,8±0,9%) выявлялись на вершинах желудочных валиков и верхушках ворсин.
Во II группе пациентов наблюдались более отчетливые изменения, характеризующие эффективность данного метода лечения. Признаки активного воспаления, фиброзирования, дистрофические, дисрегенераторные и атрофические изменения в СОДПК отсутствовали. Все показатели с высокой степенью достоверности отличались от начальных изменений. Ворсинки были покрыты энтероцитами со светлой цитоплазмой, хорошо выраженной щеточной каймой, в криптах обнаруживалось большое количество бокаловидных клеток.
Таблица 1. Морфологические изменения (%) у больных ЯБДПК с разными методами лечения (M±m)
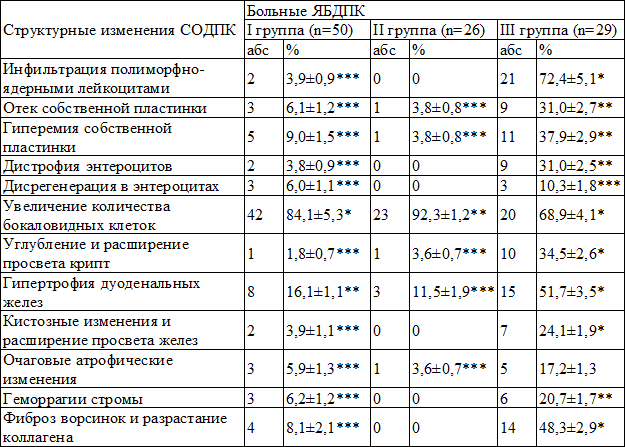
Примечание: статистические различия с исходными данными (до начала лечения): *р<0,05; **р<0,01; *** р<0,001
У пациентов III группы хотя и отличались от морфологических признаков, обнаруженных до лечения, но у большинства обследованных они имели меньшую степень достоверности (р<0,05 и р<0,01) отличий. У 72,4±5,1% в собственной пластинке сохранялась обильная инфильтрация плазматическими клетками, лимфоцитами. Эпителий был уплощен. В эпителии сохранялись дистрофические изменения. Более чем у 1/3 больных ЯБДПК сохранялись изменения, отражающие процессы, дистрофии, дисрегенерации и атрофии. Особенность гистологической картины в I и II группах больных заключалась в отсутствии изменений, характерных для фазы обострения ЯБ.
На микрофото представлены характерные морфологические изменения после лечения больных ЯБДПК ПФП инзимол, в сравнении с результатами больных, получавших только базисную эрадикационную схему терапии (рис. 5-8).
1) умеренная полиморфно-ядерная инфильтрация; энтеролизация в зоне язвенного дефекта с формированием эпителиального слоя (рис. 5);
2) формированием грануляционной ткани к центру язвенного дефекта (рис. 6);
3) лейкоцитарная инфильтрация в очагах энтеролизации; покровный эпителий некротизирован и слущен, изъязвление СО (рис. 7);
4) диффузный воспалительный инфильтрат; отек, диапедезные кровоизлияния; кишечные крипты деформированы, кистозно расширены (рис. 8).
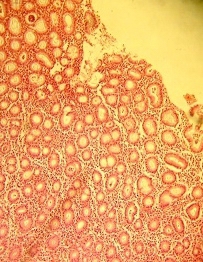
Рис. 5. Стадия заживления язвы. Окраска гематоксилин эозином. Увеличение х200
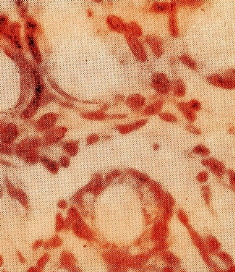
Рис. 6. Грануляционная ткань у края язвы. Окраска гематоксилин эозином. Увеличение х400
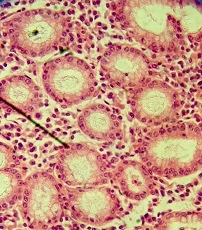
Рис. 7. Лейкоцитарная инфильтрация в очагах энтеролизации. Окраска гематоксилин-эозином. Увеличение х200
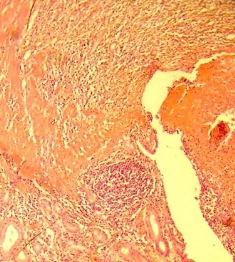
Рис. 8. Эпителий СО некротизирован и слущен, изъязвление. Окраска гематоксилин эозином. Увеличение х200
Проведенные в 3-х группах больных морфологические исследования подтвердили данные, полученные при эндоскопии. При применении инзимола исчезают или существенно уменьшаются признаки воспаления, дисрегенерации и дистрофии, происходит замещение дефекта грануляционной тканью.
Морфологические изменения СО в I и II группах больных приведены на рис. 5, 6. Морфологические изменения СО в III группе больных приведены на рис. 7, 8.
При проведении морфометрических исследований в гистологических препаратах биоптатов больных ЯБДПК до и после лечения разными методами, мы обращали внимание на толщину СО, как показателей дистрофии и дисрегенерации, на толщину подслизистого слоя ДПК (показатель выраженности инфильтративного процесса), а проводили подсчет слизистых клеток, отражающих восстановление процессов регенерации и защитных свойств СОДПК.
Морфометрические исследования показали, что у всех больных до лечения наблюдались выраженное уменьшение толщины СО до 876,2±37,1 мкм, и утолщение подслизистого слоя - до 274,5±14,7 мкм, которые с высокой степенью достоверности отличались от аналогичных показателей значений нормы (р<0,001 и р<0,05 соответственно).
Таблица 2. Морфометрические показатели (M±m) СО
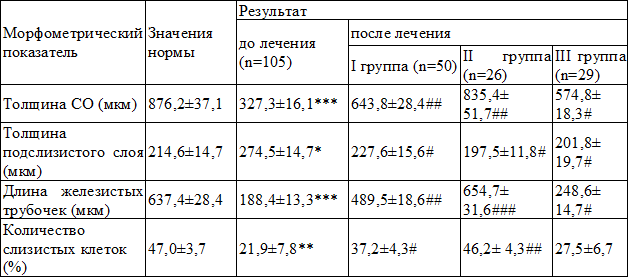
Примечания: показатели достоверности по сравнению с нормой: * - р<0,05; ** - р<0,01; ***- р<0,001); показатели достоверности до и после лечения: # - р<0,05; ## - р<0,01; ### - р<0,001
В стадии обострения у больных, по сравнению со значениями нормы, наблюдалось достоверное уменьшение размеров железистых трубочек (р<0,001) и уменьшение относительного количества слизистых клеток (р<0,01).
Сравнительный анализ морфометрических данных позволил установить, что у пациентов, пролеченных методом комплексной терапии с применением инзимола, наблюдается выраженная положительная динамика, проявляющаяся уменьшением воспалительных, дистрофических процессов, восстановлением регенерации и защитных свойств СО.
Заключение. Проведенные нами исследования морфологических и морфометрических параметров СО у больных в динамике позволили установить характер и распространенность воспалительно-дистрофических изменений, степень регенераторных нарушений, оценить состояние слизеобразования, провести сравнительную оценку эффективности проводимой терапии. Эти данные подтверждают противовоспалительные, противоотечные, регенераторные и цитопротекторные свойства ПФП инзимол. Эффективность инзимола в комплексной терапии больных ЯБДПК значительно выше, чем базисные эрадикационные схемы лечения.
Свойства ПФП очищать поверхность ран от фибрина и денатурированных белков являются перспективным при эндоскопическом лечении больных ЯБДПК. Скорость заживления язвенного дефекта при комплексном лечении обусловлены снятием фибринового налета и доступности к пораженной слизистой других препаратов. Препарат освобождает поверхность язвы от некротизированных клеток, фибрина, стимулирует процесс заживления.
