Введение. По данным IARC (Международного агентства по изучению рака) ежегодно на планете раком пищевода заболевает 0,4 млн. человек, умирает – 0,3 млн. В России среди онкопатологии данное заболевание находится на шестом месте. В структуре смертности от злокачественных заболеваний рак пищевода занимает третье место (6,4 на 100000 жителей). Пятилетняя выживаемость составляет около 6%. Основной причиной ранних летальных исходов у инкурабельных больных являются нарастающая дисфагия, кахексия. До 2 стадии больные потенциально излечимы хирургическим путем. В 3 стадии малорезектабельны. На 4 стадии инкурабельны [2-4, 6, 9].
Одной из основных проблем при неоперабельном раке пищевода является устранение дисфагии и восстановление энтерального питания. Вследствие высокой запущенности заболевания не менее 50% больных раком пищевода уже изначально нуждаются в симптоматическом лечении, преимущественно направленном на устранение дисфагии [1, 5, 7, 8, 10].
Целью исследования было проведение медико-экономического обоснования метода, создание медико-экономического стандарта (МЭС) для больных с бластоматозным поражением пищевода нуждающихся в стентировании. Задачи включали определение показания к методу, оценку клинической эффективности метода, оценку экономической эффективности метода, создание медико-экономического стандарта для данного метода и нозологии на примере субъекта федерации.
Материалы и методы. В Красноярском крае на базе краевого онкодиспансера, НИИ проблем Севера СО РАМН, краевого госпиталя для ветеранов войн с января 2007 г. проводится эндопротезирование при различных заболеваниях пищевода. В своей работе мы используем саморасправляющиеся стены M.I Tech (Корея), Ella (Чехия). Показанием к эндопротезированию пищевода являлись: опухолевые обструкции пищевода, послеоперационные рецидивы опухоли в зоне анастомоза, первичные или метастатические опухоли средостения (вызывающие компрессию пищевода), трахеоэзофагеальные свищи, перфорации пищевода, свищи эзофагогастроанастомозов, доброкачественные стриктуры пищевода [3]. За 2007-2012 г. нами проведено стентирование пищевода 180 больным (112 мужчин, 68 женщин). Возраст больных от 23 до 89 лет.
Статистическую обработку данных производили с использованием программного пакета «IBM SPSS 19.0». Описательная статистика результатов представлена в виде абсолютных значений, процентных долей и их стандартных ошибок для анализируемых качественных показателей, медианы и перцентилей – для количественных признаков. Сравнение качественных признаков производилось с использованием критерия χ2 с поправкой на непрерывность. Для сравнения количественных признаков использовали непараметрический критерий Манна-Уитни. Различия считали статистически значимыми при р<0,05.
Результаты и обсуждение. В табл. 1 указаны количество больных, заболевания при которых проводилось стентирование. В табл. 2 указаны осложнения и летальность за 2007-2012 г.
Таблица 1. Пациенты, перенесшие стентирование пищевода по нозологии (n=180)

Таблица 2. Осложнения и летальные исходы пациентов, перенесших стентирование пищевода (n=180)
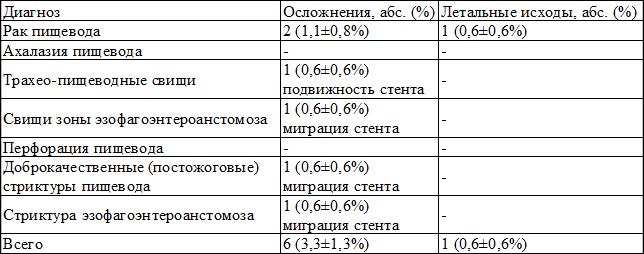
Как видно из табл. 2, летальность составила менее 1% и только у больного раком пищевода, в первый год освоения методики. Осложнения в основном связаны с подвижностью, а иногда и миграцией стентов и составили 3,3±1,3%. В дальнейшей практике при циркулярных стриктурах от эндопротезирования воздерживались ввиду частой миграции стентов. При протяженных стриктурах - 10 см. и более миграция стента была отмечена только в одном случае, в остальных смещений стента не было. Считаем необходимым проводить замену стента у больных с доброкачественными постожоговыми стриктурами через 7-8 месяцев. Более длительное пребывание ведет к фрагментации, нарушению целостности стента и как следствие, к сложностям в удалении. В случаях стентирования при бластоматозном процессе миграции отмечено не было. Был случай фрагментации стента, что по всей видимости связано с особенностями материала изготовления и прорастания опухолевым процессом слабые места стента. Важен вопрос о выборе стента. Считаем что для всех уровней пищевода, пораженных опухолевым процессом, кроме кардии. возможно установка нитиноловых саморасправляющихся стентов. В зоне кардии рекомендуем устанавливать металлические стенты. Они с более жестким каркасом и сплошным плетением. На рис. 1 - некоторые виды стентов.
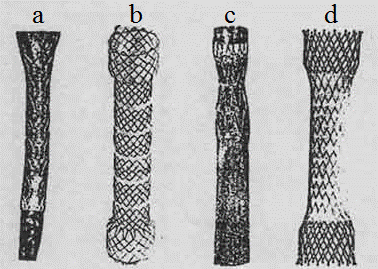
Рис. 1. a) Покрытый антирефлюксный стент FerX Ella, b) покрытый стент Choo stent, c) покрытый антирефлюксный стент Gianturco, d) покрытый стент Memotherm
Самооценку состояния больных после стентирования проводили по разработанному нами опроснику с учетом основных четырех жалоб предъявляемыми пациентами (рис. 2-5). При этом основным клиническим критерием считали купирование дисфагии, а так же способность к самообслуживанию.
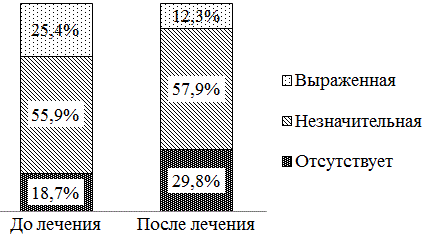
Рис. 2. Результаты самооценки пациентами ощущения общей слабости до и после стентирования пищевода
Из рис. 2-5 видно значительное улучшение состояния пациентов по данным самооценки и почти 100% купирование дисфагии. Различия в самооценке состояния пациентов до и после лечения во всех случаях носили статистически значимый характер (р<0,05).
Проведенный анализ выживаемости после стентирования по данным полученным за период 2007-2012 г. позволяет говорить о том, что средняя продолжительность жизни пациентов составила 336 дней, при этом 25% умерли в сроки до 136 дней, 50% (медиана) дожили до 331 дня и 25% прожили более 499 дней. В тоже время ретроспективный анализ периода выживаемости инкурабельных онкологических больных после гастростомии показал, что при средней продолжительности жизни 333 дня, показателю 75 перцентиля соответствует 461 день жизни, что более чем на месяц (38 дней) меньше аналогичного показателя при стентировании (р<0,05).
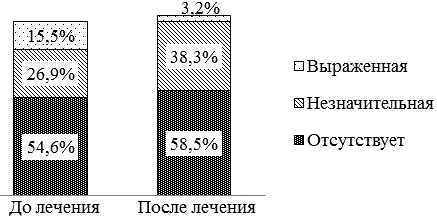
Рис. 3. Результаты самооценки пациентами ощущения боли до и после стентирования пищевода
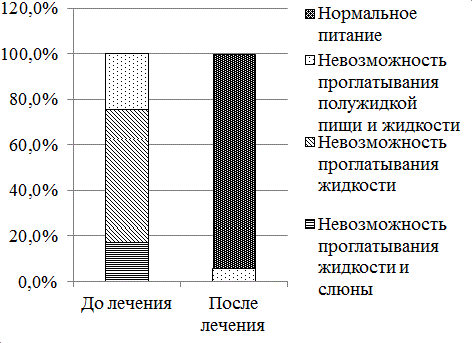
Рис. 4. Результаты самооценки пациентами акта приема пищи до и после стентирования пищевода.
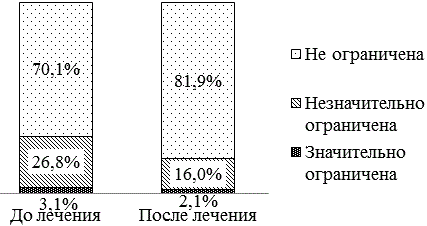
Рис. 5. Результаты самооценки пациентами возможности к самообслуживанию до и после стентирования пищевода.
Таким образом, сравнительный анализ продолжительности жизни после установки пищеводных стентов в одном случае и гастростомы - в другом, позволят говорить о более благоприятном прогнозе при первом варианте устранения стеноза пищевода. Оценку экономической эффективности метода проводили калькуляцией всех фактических затрат при стентировании пищевода и сопоставляли с уже имеющимся тарифом МЭС 1100030 (наложение гастростомы), утвержденного согласительной комиссии системы обязательного медицинского страхования от 24.09.08 г. (табл. 3).
Таблица 3. Сравнительная экономическая оценка стентирования пищевода и гастростомы
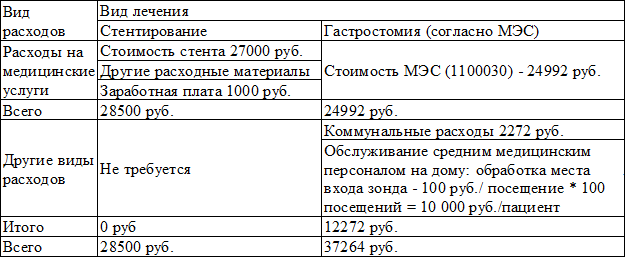
В результате с введением нового однодневного МЭС (стентирование пищевода) для амбулаторной хирургии в поликлинике или дневном стационаре дополнительные расходы составляют 245560 руб. в год, с учетом расходов на посещение пациентов с гастростомами средним медицинским персоналом экономия составит – 613480 руб. (табл. 4).
Таблица 4. Экономическая оценка вариантов лечения больных со стенозом пищевода
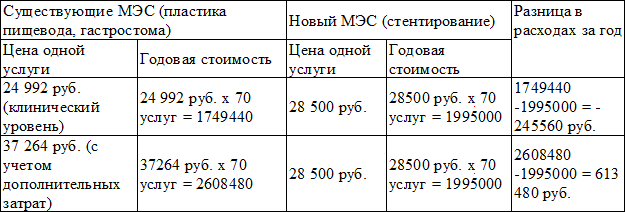
Заключение. Таким образом, внедрение нами с января 2007 г. в Красноярском крае эндопротезирования саморасправляющимися стентами стенотических поражений пищевода позволило:
1) Определить показания к методу.
2) Практически доказать его эффективность, как при онкопатологии, так и при доброкачественных стриктурах пищевода.
3) Оценить клиническую эффективность, показав улучшение качества жизни пациентов после восстановления физиологического акта питания, снижения болевого синдрома, уменьшение общей слабости, увеличение продолжительности жизни. При этом у многих пациентов сохраняется способность к трудовой деятельности.
4) Оценить экономическую эффективность метода.
Калечащая и дорогостоящая госпитальная помощь при гастростомии больным с бластоматозным поражением пищевода может быть заменена на амбулаторную, в виде эндоскопического стентирования, либо в отдельных случаях лечением в условиях дневного стационара. Расчеты экономической эффективности позволяют говорить о том, что при калькуляции явных и скрытых расходов стентирование может быть альтернативой традиционно применяемому методу гастростомии, а так же лечению по квотам в федеральных центрах, с учётом их недостаточного количества, высокой стоимости транспортных расходов и рисков для ослабленных пациентов.
Результатом нашей работы стало решение заседания согласительной комиссии системы обязательного медицинского страхования от 7 апреля 2010 г.:
1) утвердить пункты и приложения Тарифного соглашения системы ОМС на 2010 г. в части перераспределения средств на дневные стационары;
2) утвердить медико-экономический стандарт - «Стентирование пищевода в условиях стационара одного дня». Тариф пролонгируется по сей день, с учетом инфляционной составляющей.
