Введение. В настоящее время интенсивной терапии панкреонекроза принадлежит одна из ведущих ролей в определении исхода заболевания [5,6]. По выполнении лапароскопического дренирования брюшной полости проведение широко комплекса лечебных мероприятий позволяет значительно улучшить течение заболевания: снизить число гнойных осложнений, а при их развитии уменьшить тяжесть течения абдоминального сепсиса. При этом ведущим патогенетическим моментом, определяющим направление течения патологического процесса является синдром кишечной недостаточности (СКН) [1]. Развивающийся парез кишечника является причиной не только метаболических расстройств, но и избыточной бактериальной контаминации верхних отделов тонкой кишки, усиленной бактериальной транслокации и эндотоксиновой агрессии, запуская механизмы тяжелого абдоминального сепсиса и полиорганной недостаточности [2,7]. В качестве ведущего лечебного мероприятия в борьбе со звеньями СКН в настоящее время рассматривается раннее энтеральное питание [4], при этом способ и сроки начала нутритивной явились причиной оживленной дискуссии на заседании «Круглый стол: диагностика и лечение острого панкреатита» (Санкт-Петербург, 2014), а необходимость начала энтерального питания утверждена в принятых «Национальных рекомендациях» по лечению острого панкреатита [3]. На практике нередко мы сталкиваемся с фактом непереносимости определенной питательной смеси, что согласно принципам энтерального питания требует его прекращения или смены нутриента, что, практически, не выполнимо в условиях стандартной больницы скорой помощи.
Поэтому требует более детального изучения как клиническое течение, так и исходы острого панкреатита в зависимости от переносимости питательных смесей. Кроме того, необходима разработка новых подходов к нутритивной поддержке при панкреонекрозе с учетом переносимости больными энтерального питания.
Цель исследования: оценить эффективность энтеральной поддержи больных панкреонекрозом с позиций синдрома кишечной недостаточности.
Материал и методы. Нами проведена оценка клинического течения и исходов панкреонекроза у 113 больных тяжелым острым панкреатитом, находившихся в экстренных отделениях клиник в период 2008-2014 г., в зависимости от типа энтеральной поддержки и переносимости питательной смеси. Кроме того, в качестве метода лабораторного контроля оценивали уровень бактериального липополисахарида - эндотоксина (ЭТ), как, показатель, напрямую отражающий выраженность проявлений СКН. Определение уровня липополисахаридов проводили с помощью LAL-теста (хромогенный тест) набора реактивов (HIT302) Hycult Biotech. Забор крови в основной группе и определение исследуемых показателей проводили при поступлении больного и далее ежедневно до 10 суток при положительной динамике заболевания и 14 суток при тяжелом течении процесса, т.е. срока формирования гнойников. Полученные показатели оценивали в сопоставлении с клиническими проявлениями заболевания.
Средний возраст больных составил 37±6,4 года. Мужчин 85 (75%), женщин 28 (25%). В 101 (90%) случаях пусковым моментом заболевания явилось злоупотребление алкоголем, в 6 (5%) случаях переедание, в 6 (5%) этиологический фактор выяснить не представилось возможным.
Ретроспективное (на основании анализа протоколов хирургических вмешательств, компьютерных томограмм, результатов аутопсии) распределение больных групп сравнения по степени поражения поджелудочной железы, развитию гнойных осложнений и летальности (табл. 1).
Таблица 1. Тяжесть поражения поджелудочной железы и исходы в группе больных
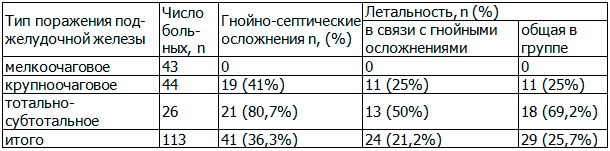
Из данных табл. 1 отчетливо прослеживается увеличение летальности с увеличением объёма поражения поджелудочной железы, при этом при крупноочаговом панкреонекрозе гнойно-септические осложнения являются основной причиной летальности, в то время как при массивном поражении около трети больных погибает до развития гнойного процесса вследствие интоксикации и тяжелого системного воспалительного ответа, ещё треть больных умирает вследствие тяжёлого сепсиса и аррозивных кровотечений при развитии гнойных осложнений.
Все больные получали адекватную инфузионную, дезинтоксикационную, антисекреторную и антибактериальную терапию в условиях ПИТ или в хирургическом отделении при согласовании объёма инфузии с врачом анестезиологом-реаниматологом. Как ведущий хирургический этап лечения 100% больных основной группы выполнялось лапароскопическое дренирование брюшной полости. Ключевым моментом в комплексном лечении больных считали эндоскопическую установку назоеюнального зонда для проведения энтерального питания. В своей работе мы применяли следующие питательные смеси: «Берламин® Модуляр», «Нутризон», «Фрезубин оригинал с пищевыми волокнами». Сроки нахождения зонда варьировали в соответствии с тяжестью течения патологического процесса от 5 до 27 суток.
Статистическую обработку результатов проводили вариационно-статистическим методом с использованием пакета прикладных программ Micrоsoft Office Excеl 2013, а также пакет Mathcad 14.0. на IBM PC/AT «Pentium-IV» и «iCore 7» в среде Windows XP и Windows 7. Для определения значимости различий между исследуемыми признаками использовали параметрические и непараметрические методы статистики (t-критерий Стьюдента - для количественных признаков и χ2 для качественных признаков. Из непараметрических методик использовался критерий U-критерия Манна-Уитни. При оценке динамики лабораторных показателей выраженности СКН в группе применяли дисперсионный анализ повторных измерений. Различия считались статистически значимыми при p<0,05.
Результаты. С самых ранних этапов использования энтерального зондового кормления в лечении больных панкреонекрозом мы сталкивались с фактом клинической регистрации непереносимости питательных смесей. Под последним понимаем развитие тошноты, диарея, усиление сброса застойного содержимого по назогастральному зонду, в ряде случаев подобная клиническая ситуация сопровождалась гипернатриемией, гиперкальциемией, азотемией. Окончательное решение о непереносимости конкретной питательной смеси принимали после коллегиальной оценки отсутствия фактов нарушения режима введения, дозировки смеси или правил ухода за зондом. Из 113 больных те или иные клинические проявления непереносимости смеси зарегистрированы в 40 (35,3%) случаев. Характер непереносимости в зависимости от вида питательной смеси представлен в табл. 2.
Таблица 2. Характер непереносимости смеси
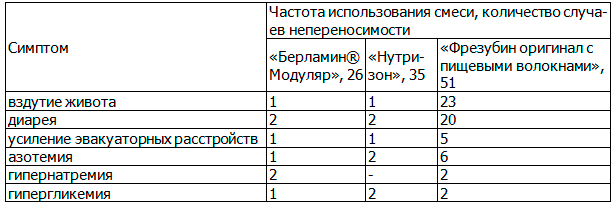
Мы видим, что наибольшая частота непереносимости смеси отмечается при использовании препарат «Фрезубин», при этом при его применении у одного больного может наблюдаться несколько симптомов, при этом непереносимость препарата «Фрезубин», практически в 50% (25 случаев). Смесь «Нутризон» характеризовалась наибольшей переносимостью - 80%.
Развитие в первую очередь осложнений со стороны желудочно-кишечного тракта, на наш взгляд, не могло, не отразится на течении СКН. С этой целью, мы оценили динамику ЭТ в 1-й группе сравнения в зависимости от характера усвоения смеси. Нами ретроспективно оценён данный показатель отдельно среди больных мелкоочаговым панкреонекрозом, а также в группе крупноочагового панкреонекроза, среди пациентов, имевших и не имевших гнойно-септических осложнений. Динамика уровня ЭТ представлена в табл. 3, 4.
Таблица 3. Уровень плазменного ЭТ в зависимости от переносимости энтерального питания в группе мелкоочагового панкреонекроза
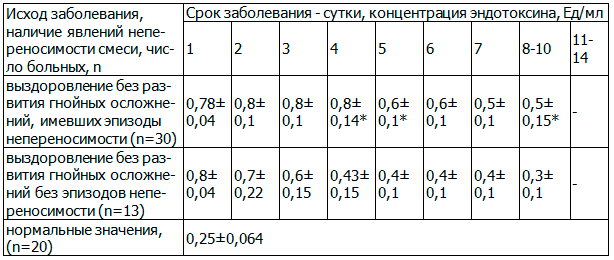
Примечание: * - (p<0,05) различия достоверны с показателями соответствующих суток (критерий Манна-Уитни).
Из представленных в табл. 3 данных мы видим, что острый панкреатит средней тяжести также характеризуется развитием СКН, начиная с первых суток заболевания, при этом, несмотря на благоприятный исход, развивающаяся непереносимость энтерального питания поддерживает высокий уровень эндотоксиновой агрессии, сохраняющийся при купировании клинической картины заболевания.
Таблица 4. Уровень плазменного ЭТ в зависимости от переносимости энтерального питания в группе крупноочагового панкреонекроза
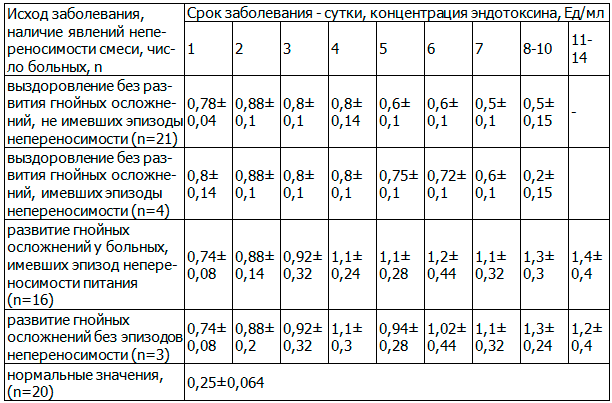
Из данных табл. 4 также прослеживается динамика нарастания уровня ЭТ при развитии непереносимости энтерального питания. При этом суммарно в случае развития элементов непереносимости питательных смесей при проведения энтерального питания риск развития гнойных осложнений при панкреонекрозе возрастает в 5,25 раза (p<0,01).
Кроме того, в группе тотально-субтотального панкреонекроза выжившие больные в 100% имели гнойные осложнения. Непереносимость питательной смеси зафиксирована в 7 случаях, при этом 5 больных погибли до развития гнойных осложнений, связи, с чем объективно оценить у них индивидуальную непереносимость энтерального питания не представлялось возможным. С нашей точки зрения с учетом объёма поражения ткани поджелудочной железы и забрюшинной клетчатки, говорить о ведущей роли неэффективного энтерального питания в усилении СКН, приведшей к гнойным осложнениям, у данной категории больных считаем неправомочным.
Обсуждение. Представленные в исследовании данные отражают современные взгляды на патогенез формирования инфицированного панкреонекроза с позиций синдрома кишечной недостаточности. Работа показывает, что «повальное увлечение» в последние годы проведением энтеральной нутритивной поддержки при панкреонекрозе сопряжено с увеличением частоты непереносимости питательных смесей, характеризующейся не только стандартными клинико-лабораторными проявлениями, но и усугублением синдрома кишечной недостаточности. При этом с увеличение объёма поражения поджелудочной железы отмечается клинически значимое отражение непереносимости питательных смесей - пятикратное увеличение частоты гнойных осложнений. При этом при отсутствии явлений непереносимости отмечается положительная как клиническая, так и лабораторная динамика течения заболевания.
На наш взгляд, отказ от энтерального кормления и переход на полную парентеральную поддержку не может быть единственным выходом при развитии непереносимости питательных смесей при панкреонекрозе, поскольку в подобной ситуации становится невозможной коррекция энтеральной недостаточности, как основного патогенетического механизма инфекционных осложнений. Выходом в данной ситуации можно было бы считать применение методик энтеросорбции в комплексе с энтеральной поддержкой. Данные методы требую накопления клинического опыта и продолжения исследований в этой области.
