Частота хронического неспецифического цервицита в поликлинических отделениях составляет до 70% [1,2]. Доказана роль неспецифических цервицитов в генезе невынашивания беременности, возникновении воспалительных заболеваний органов малого таза, развитии инфекционных осложнений в родах и послеродовом периоде. Общеизвестно значение данной патологии в индукции неопластических процессов шейки матки. Для данной патологии в последнее десятилетие характерно отсутствие четко выраженной клинической картины, склонность к длительному течению, рецидивированию. В качестве основополагающей причины хронизации воспалительного процесса все чаще упоминается иммунологические нарушения [1-3].
В настоящее время особое внимание уделяется системе толл-подобных рецепторов (TLR), отвечающих за распознавание компонентов клеточной стенки бактерий, активацию каскада провоспалительных цитокинов, формирование колонизационной резистентности. TLR являются связующим звеном между врождённой и адаптивной иммунной системой [5,7]. Поддерживая чрезмерную активацию Th2-профиля цитокинов, происходит перевес провоспалительных цитокинов, и инициируется хронизация процесса. Каждый конкретный TLR играет важную роль в быстром распознавании специфических микробных компонентов, включая бактерии, грибы, вирусы и некоторые простейшие. TLR2 и функционально ассоциированые с ним TLR1 и TLR6 могут распознавать пептидогликаны большинства видов бактерий и компоненты грибов. TLR3 способен распознавать двуцепочечную РНК, обнаруживающуюся во время цикла репликации большинства вирусов. TLR4 определяет липополисахариды грамотрицательных бактерий, TLR9 распознает одноцепочечные рибонуклеиновые кислоты (РНК) некоторых вирусов, гипометилированные гуанин-цитозин участки двойной дезоксирибонуклеиновой кислоты (ДНК) бактерий и ДНК, образующейся при репликации вирусов, таких как вирус простого герпеса [4,5,7,8]. Учитывая важнейшую роль TLR в реализации врожденного иммунного ответа, можно предположить, что дефекты на уровне самих рецепторов, на уровне различных компонентов, участвующих в передаче сигнала, а также факторов, регулирующих их функцию, могут способствовать развитию инфекционных и воспалительных заболеваний. Полиморфизм генов предполагает, что с одного и того же гена может быть скопировано несколько структурно отличающихся копий одного и того же белка. При этом часть скопированных вариантов или не обладает активностью, или может иметь противоположную функцию. В случае TLR полиморфизм может приводить к нарушению распознавания инфекционных агентов и дисбалансу функционирования системы врожденного иммунитета, что в конечном итоге будет проявляться как повышение чувствительности к инфекциям и развитие хронических воспалительных заболеваний [6-8].
Определение точечных нуклеотидных мутаций промоторных участков генов TLR может дать возможность прогнозировать исход заболевания и подобрать адекватную схему лечения.
Цель исследования – провести анализ генетической предрасположенности к нарушению иммунного ответа при хроническом неспецифическом цервиците.
На базе центра планирования семьи и репродукции ГБУЗ «Воронежская областная клиническая больница №1» и женской консультации ГУЗ «Клинического родильного дома №2» г. Волгограда были обследованы 96 женщин с хроническим неспецифическим цервицитом (основная группа) и 24 женщины без патологии шейки матки (контрольная группа). Исследование у пациенток проводилось при наличии информированного согласия, соответствовали этическим принципам, предъявляемым Хельсинской декларацией Всемирной Медицинской Ассоциации (World Medical Assotiation Declaration of Helsinki).
Особое значение в исследовании уделялось тщательному анализу анамнеза заболевания пациенток. Принималось во внимание продолжительность заболевания, частота рецидивов, проводимая ранее терапия.
Для исследования точечных нуклеотидных полиморфизмов (SNP) генов TLR использовались образцы ДНК, выделенной из ядросодержащих клеток периферической крови. Забор биологического материала для проведения лабораторных исследований проводился в период отсутствия острых и ремиссии хронических соматических заболеваний более 6 месяцев, а также при условии исключения приема медикаментов и принятия лечебных процедур. Идентификация полиморфных аллелей генов осуществлялась методом аллельспецифической полимеразной цепной реакции с последующей электрофоретической детекцией в агарозном геле. На всех стадиях проведения молекулярно-генетических исследований использовались реактивы и методики, разработанные ООО НПФ «Литех» (г. Москва). Генотипирование промоторных участков проводилось по следующим полиморфным маркерам: Arg753Gln – для TLR 2; Phe412Leu – для TLR 3; Asp299Gly - для TLR 4; Ser249Pro – для TLR 6; T-1237С - для TLR 9.
При сравнении групп по количественным признакам использовался U-критерий Манна-Уитни при уровне значимости р<0,05. Статистический анализ результатов молекулярно-генетических исследований включал оценку частоты распределения аллелей генов, генотипов и их комбинаций, анализ таблиц сопряженности. Частоту аллелей генов и генотипов вычисляли методом прямого подсчета. Статистическую оценку проводили по показателю OR (odds ratio — отношение шансов) с вычислением 95% доверительного интервала для OR (95% CI). Достоверность различий частот распределения изучаемых признаков в исследуемых группах определяли по критерию Фишера.
При детальном изучении анамнеза заболевания обследованных больных установлено, что у 69,3% пациенток длительность заболевания составила от 2 до 5 лет. Ранее лечение по поводу цервицита проходили 84,2% больных, не лечились - 15,8%. Во время предыдущих курсов лечения, в основном, назначались антибактериальная терапия и местная санация влагалища. Частота обострений варьировала от 1 до 3 обострений в течение года.
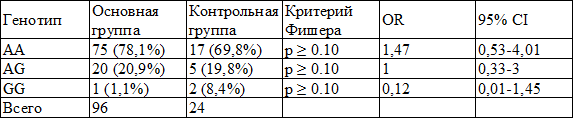
В ходе молекулярно-генетического исследования частота аллеля A полиморфного маркера гена TLR 2 выявлена у 88,6% испытуемых основной группы и 82% контрольной группы (р<0,01; OR=6,17; 95% CI =2,63-14,5), а аллеля G – 11,4% и 18% соответственно (р>0,1; OR=0,16; 95% CI=0,06-0,38). Но встречаемость гомозиготы AA, гетерозиготы AG и мутантной гомозиготы GG в исследуемых группах не различались (табл. 1).
Таблица 1. Распределение аллельных вариантов полиморфного маркера гена (Arg753Gln) TLR 2
При молекулярно-генетическом исследовании распределения полиморфного варианта Phe412Leu промоторной области TLR 3 и полиморфного варианта Asp299Gly промоторной области TLR 4 значимых отличий в исследуемых группах также обнаружено не было (табл. 2,3).
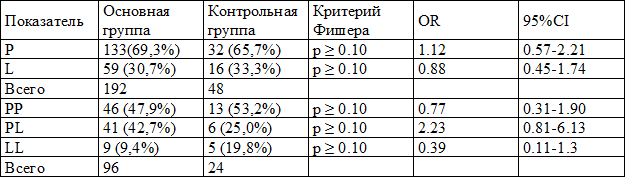
Таблица 2. Распределение частот аллелей и генотипов полиморфного маркера Phe412Leu гена TLR 3
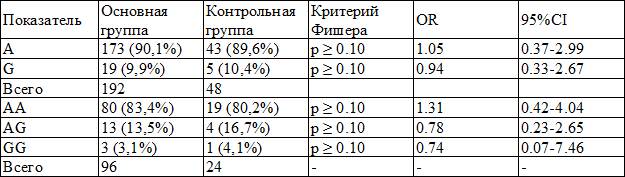
Анализ частоты встречаемости аллельных вариантов полиморфного локуса T-1237С в промоторной части гена TLR 9 позволил установить значимое увеличение частоты встречаемости гетерозиготного генотипа TC в основной группе по сравнению с контрольной группой (53,2% против 25%; р<0,05; OR=3,4; 95% CI=1,24 – 9,3). Однако, частоты встречаемости аллелей и гомозигот ТТ, CC значимо между группами не различались. Так, аллель Т был выявлен у 69,3% больных основной группы и у 78,2% женщин контрольной группы (p ≥ 0,1; OR=0,59; 95% CI =0,27-1,26), а аллель С у 30,7% и 21,8% соответственно (p ≥ 0,1; OR=1,68; 95% CI =0,78-3,6). Гомозигота ТТ обнаружена у 42,7% и 67,7% испытуемых в основной и контрольной группах (p ≥ 0,1; OR=0,37; 95% CI =0,14-0,95). Соответственно гомозигота CC определялась у 4,1% и 8,3% женщин исследуемых групп (p ≥ 0,1; OR=0,46; 95% CI =0,08-2,72).
Таблица 3. Распределение частот аллелей и генотипов полиморфного маркера Asp299Gly гена TLR 4
Частоты встречаемости аллелей и генотипов полиморфного маркера гена TLR 6 распределились следующим образом: аллель P встречался у 49% и 31% пациентов основной и контрольной групп (р<0,05; OR=2,32; 95% CI=1,17 – 4,61), а аллель S в 51% и 69% случаях соответственно (р<0,05; OR=0,42; 95% CI=0,21 – 0,85). При этом, отмечено значительное увеличение частоты обнаружения генотипа PP у пациенток основной группы, который встречался в 37% случаев против 4% в контрольной группе (р<0,01; OR=13,8; 95% CI=1,78 –106,5), частота встречаемости гомозиготы SS в исследуемых группах не различались. Гетерозиготы SP встречались у 44,8% испытуемых контрольной группы и у 22,9% пациенток основной группы (р<0,05; OR=0,35; 95% CI=0,13 – 0,89).
При дальнейшем анализе, выявлена корреляционная зависимость между наличием мутантной гомозиготы PP TLR 6 и длительностью заболевания. Так, средняя продолжительность заболевания на момент обследования у женщин без мутации в гене TLR 6 в основной группе составила- 2,5±1,2 года, а у пациенток, носительниц мутантной гомозиготы PP гена TLR 6 - 3,9±1,01 год (p<0,01) (табл. 4).
Таблица 4. Длительность заболевания в основной группе к моменту обследования
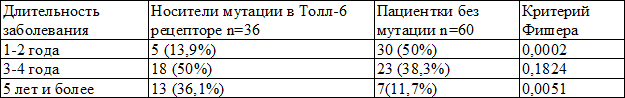
Можно заключить, что среди пациенток с хроническим неспецифическим цервицитом мутантные гомозиготы PP в гене TLR 6 (Ser249Pro) встречается в 9,2 раза чаще, чем среди женщин, не имеющих данного заболевания. В 3,6 раза чаще течение хронического неспецифического цервицита длительностью менее 2 лет наблюдалось у пациенток без мутации в гене TLR 6. Кроме того, у таких больных в 3 раза реже данное заболевание длилось более 5 лет. Следовательно, выздоровление наступало скорее, нежели у больных, имеющих в своем генотипе мутантную гомозиготу PP TLR 6.
Таким образом, иммуногенетическое обследование профиля гена TLR 6 (Ser249Pro) у женщин с цервицитом позволяет прогнозировать течение неспецифического цервицита и может быть основой для индивидуализации профилактических и лечебных мероприятий у данной группы пациенток.
