Йодиды являются неспецифическими антикоагулянтами [1-3]. Йод, являясь активным антикоагулянтом 2 группы, усиливает секрецию гепарина тучными клетками, повышая липолитическую и фибринолитическую активность крови [4-6]. Если раньше этот эффект связывался в основном с его антитромбиновым действием (анти-IIa), то теперь доказано блокирующее влияние гепарина почти на все факторы свертывания, принадлежащие к сериновым протеиназам - на факторы XIIa, XIa, IXa и Xa [1, 2, 6, 7]. Это действие реализуется через физиологический антикоагулянт - антитромбин III. Гепарин резко усиливает инактивирующее действие антитромбина III на все перечисленные выше ферментные факторы свертывания. По мере снижения в плазме концентрации антитромбина III противосвертывающее действие гепарина все более и более ослабляется, становясь вообще малозаметным при концентрации антитромбина III ниже 15-30% нормы [1, 2].
При изучении переносимости, безопасности нового лекарственного средства ФС-1 на здоровых лицах установлено, что ФС-1 обладает дозозависимым антикоагулянтным фармакологическим действием на гемостаз [8], что согласуется с данными литературы [1-7].
Цель клинического исследования: оценка влияния терапевтических доз нового лекарственного средства ФС-1 на гемостаз при туберкулезе.
Материалы и методы.
Объект исследования - новое лекарственное средство ФС-1, представляющее собой раствор комплексного соединения йода с полидентатными лигандами, в качестве которых были ассоциаты карбогидратов и пептидов. Активной субстанцией лекарственного средства является йодно-полимерный комплекс.
Субъекты исследования - лица в возрасте от 18 до 65 лет с туберкулезом легких с множественной лекарственной устойчивостью, выделяющие устойчивые штаммы микобактерий туберкулеза (далее - МБТ) к противотуберкулезным препаратам (далее - ПТП) первого ряда.
Статистическая обработка - для проверки достоверности результатов исследования был применен критерий χ2.
Основные показатели гемостаза, выбранные для изучения: акгтивированное парциальное тромбопластиновое время (далее - АПТВ), протромбиновый индекс (далее - ПТИ), протромбиновое отношение (далее - ПО), тромбиновое время, фибриноген. Показатели гемостаза регистрировались до начала исследования, затем через 14, 30, 60, 90, 120, 150, 180 дней применения комбинированной терапии.
Дизайн исследования: рандомизированный, плацебоконтролируемый, одноцентровой.
Схема терапии
До начала клинических исследований субъекты исследования были рандомизированы в 3 группы. Все субъекты исследования получали стандартную противотуберкулезную терапию (далее - ПТП) препаратами второго ряда. В основных группах субъекты исследования дополнительно получали ФС-1, в группе контроля - плацебо. ПВР включали капреомицин, амикацин, фторхинолоны: офлоксацин / левофлоксацин / мофлоксацин; тиазиды: протионамид / этдионамид; циклосерин; ПАСК; пасканат. В табл. 1 приведены дозы и схемы применения ФС-1.
Таблица 1. Дозы и схемы применения ФС-1 на курс лечения при туберкулезе с МЛУ
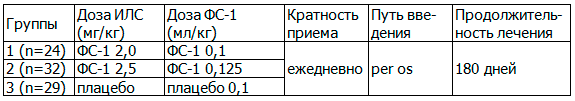
Результаты исследования. В табл. 2 приведено распределение субъектов исследования по клиническим формам. Табл. 2 свидетельствует о том, что между исследуемыми группами достоверных различий по клиническим формам заболевания не обнаружено, то есть по указанным признакам группы однородные и возможно их сравнение в ходе клинических исследований.
Таблица 2. Распределение субъектов исследования по клиническим формам туберкулеза легких, %

Результаты анализа показателей гемостаза представлены в виде качественных показателей по признакам «ниже нормы», «норма» и «выше нормы», в абсолютных цифрах и рассчитаны методом критерия χ, где Р - уровень значимости, указывающий на статистически достоверные различия между показателями гемостаза основных групп и плацебо.
Анализ показателей гемостаза в течение 6 месяцев исследования показал, что достоверных различий по АПТВ между исследуемыми группами не наблюдалось, за исключением 3 месяца, когда в 3-й контрольной группе (плацебо) показатель АПТВ был у 45,5% выше нормы, тогда как в 1-й группе - у 20,8%, во 2-й - у 17,4%, последнее имело достоверные различия с группой плацебо (P<0,05), табл. 3.
Таблица 3. Сравнительная динамика АПТВ
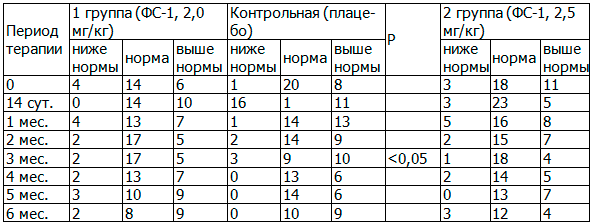
Примечание: здесь и далее Р - статистически достоверные различия между качественными показателями гемостаза основных и контрольной группах.
Анализ протромбинового индекса показал, что достоверных различий между группами, в том числе основными и контрольной, достоверных различий не обнаружено (табл. 4).
Таблица 4. Сравнительная динамика протромбинового индекса, абс.
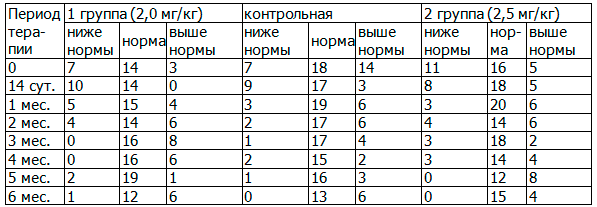
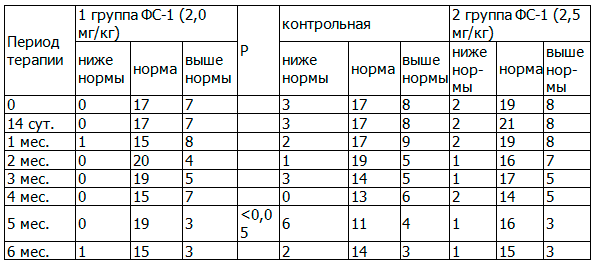
Анализ динамики тромбинового времени показал, что спустя 4, 5 месяцев терапии удельный вес пациентов с повышенным тромбиновым временем становится меньше во всех группах, включая контрольную, хотя достоверные различия обнаружены между 2-й основной и контрольной группами через 4 месяца (табл. 5).
Таблица 5. Сравнительная динамика тромбинового времени, абс.
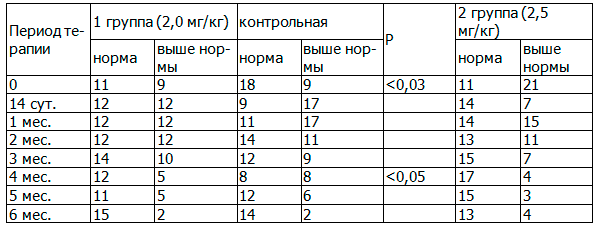
Последнее свидетельствует о том, что ФС-1 способствовало нормализации тромбинового времени у большинства пациентов, если еще учитывать, что до начала исследования во 2-й основной группе удельный вес пациентов с гипокоагуляцией был выше (65,6%), чем во всех остальных группах: в 1-й основной группе - 45,0%, в контрольной - 33,3%.
Анализ динамики показателя гемостаза фибриногена в течение 6 месяцев исследования показал, что достоверных различий между группами не выявлено, за исключением 5-го месяца терапии, когда удельный вес пациентов с нормальным фибриногеном оказался выше, чем в контрольной группе, и составил 86,4%, против 57,9%, (Р<0,05), (табл. 6). Во второй основной группе этот показатель была также высок - 84,2%.
Таблица 6. Сравнительная динамика фибриногена, абс.
Из вышеизложенного следует, что применение ФС-1 в комплексной противотуберкулезной терапии в дозах 2,0 и 2,5 (мг/кг) массы тела в течение 6 месяцев способствуют нормализации показателей гемостаза и не вызывают гипокоагуляцию у больных туберкулезом с множественной лекарственной устойчивостью.
