Введение. Иммунная система человека и животных является, как известно, одной из наиболее чувствительных систем живого организма. Органы иммунной системы первыми реагируют на любые внешние воздействия [4, 16, 17]. Вместе с тем, сведения о влиянии длительного радиационного воздействия по отношению к селезенке, важнейшему периферическому органу иммунной системы, в научной литературе фактически отсутствуют. Имеющиеся по этому вопросу данные касаются лишь сочетанных (радиационных, химических) воздействий, как следствий техногенных аварий и химических выбросов в атмосферу при работе производственных предприятий [5,6,13]. Несмотря на наличие исследований, указывающих на структурно-функциональные изменения селезенки и ее белой пульпы при самых различных внешних воздействиях [19], данные об изменчивости и восстановительных процессах этих структур в результате хронических воздействий радиационного фактора низкой интенсивности в научной литературе отсутствуют.
Следует также отметить, что, несмотря на наличие многочисленных современных исследований, посвященных морфологии лимфоидного аппарата селезенки, в том числе и у экспериментальных животных [7,14,15,18], вопросам микроанатомии и микротопографии, клеточного состава иммунных структур этого органа, почти не уделяется внимание. Нет, в частности, данных о структурно-функциональных характеристиках лимфоидных структур (периартериальных лимфоидных муфт, лимфоидных узелков и др.), их размерных показателях, микротопографии у мышей, что не правомочно, учитывая их широкое использование в медико-биологических экспериментах.
Цель исследования - изучение структурных характеристик иммунных образований селезенки у мышей после экспериментального воздействия радиационного фактора низкой интенсивности.
Материалы и методы. В качестве материала исследования взята селезенка 84 мышей - самцов линии F1(CBAxC57BL6), массой 25-30 гр, из которых группу контроля составляет 12 мышей. Животные содержались на стандартном пищевом рационе с двухнедельным карантином в условиях вивария.
Общая длительность эксперимента составила ~ 230 сут. (8 месяцев). Облучение проводили с помощью гамма-установки ГОБО-60 с источником Cs137. Экспериментальные животные (72 мыши) подвергались общему равномерному гамма-облучению в течение 70 суток при мощности дозы 25 сГр в час. Облучение проводилось 1 раз в неделю по 2 часа в утреннее время суток. Доза гамма-облучения за одну неделю составляет 50 сГр. Суммарная доза облучения для животных за 70 суток составляет 500 сГр. Доза облучения у различных групп животных являлась единственным фактором, который влиял экспериментальных животных. Доза облучения лабораторных животных – 500 сГр, с учетом разницы в продолжительности жизни и чувствительности к радиационному воздействию животных (мышей) и человека, соответствует дозе облучения 170 сГр для человека. Доза облучения 170 сГр соответствует предельно допустимому уровню, характерному для межпланетных пилотируемых полетов [13]. Из эксперимента мышей выводили сразу же после его окончания (12 мышей), а также в реабилитационном периоде (после воздействий) через 9, 14, 30, 60 и 90 суток (по 12 мышей в каждой группе). Контрольную группу (не подвергавшихся облучению) выводили из эксперимента также непосредственно после его окончания.
Животные забивались методом цервикальной дислокации (смещение шейных позвонков иглой, после применения эфирного наркоза). Гибели мышей во время облучения, в реабилитационном периоде не наблюдали.
Лимфоидные структуры селезенки после ее фиксации в нейтральном формалине изучали на срезах, окрашенных гематоксилином-эозином. Использовали методику точечного счета, по Глаголеву А.А. [3] в модификации Стефанова С.Б. [12]. Статистическая обработка данных включала вычисление средне арифметических показателей и их ошибки, достоверность различий определяли методом доверительных интервалов. Эксперимент проводился на базе государственного научного центра Российской Федерации института медико-биологических проблем РАН и Первого Московского государственного медицинского университета им И.М. Сеченова.
Результаты исследования и их обсуждение. Мы провели анализ числа разных типов клеток лимфоидного ряда в лимфоидных узелках без центров размножения в селезенке мышей непосредственно после окончания воздействия радиационного фактора (на площади 880 мкм2 гистологического среза) (табл. 1). Согласно данным табл. 1, у мышей экспериментальной группы в лимфоидных узелках (без центров размножения), по сравнению с контролем, абсолютное содержание малых лимфоцитов уменьшается в1,71 раза (р<0,05), ретикулярных клеток – в 1,88 раза (р<0,05), макрофагов – в 1,5 раза (р>0,05).
По сравнению с контролем, в составе лимфоидных узелков мышей экспериментальной группы, по сравнению с контролем, количество средних лимфоцитов почти не изменяется, а деструктивно измененных клеток лимфоидного ряда увеличивается существенно (в 7,57 раза, р<0,05).
В отличие от контроля, в составе лимфоидных узелков без центра размножения у мышей экспериментальной группы большие лимфоциты, плазматические клетки и митотически делящиеся клетки на гистологических препаратах селезенки единичные или отсутствуют.
Мы изучили количество разных типов клеток лимфоидного ряда в красной пульпе селезенки мышей непосредственно после окончания воздействия радиационного фактора (на площади 880 мкм2).
Таблица 1. Количество разных типов клеток лимфоидного ряда в лимфоидных узелках без центров размножения в селезенке мышей непосредственно после окончания воздействия радиационного фактора (X±Sx; min-max); на площади880 мкм2).
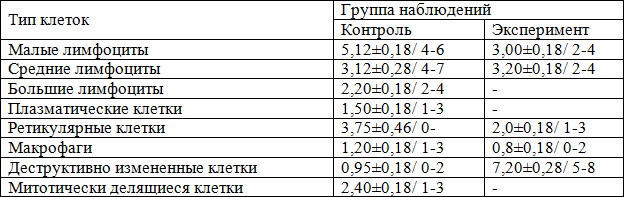
Примечание: здесь и далее в контрольной и экспериментальной группах по 12 наблюдений. Прочерк (-) означает отсутствие признака. При отсутствии (единичном наличии) клеток определенного типа в обеих группах они в табл. не указаны
Таблица 2. Количество разных типов клеток лимфоидного ряда в красной пульпе селезенки мышей непосредственно после окончания воздействия радиационного фактора (X± Sx; min-max); на площади 880 мкм2)
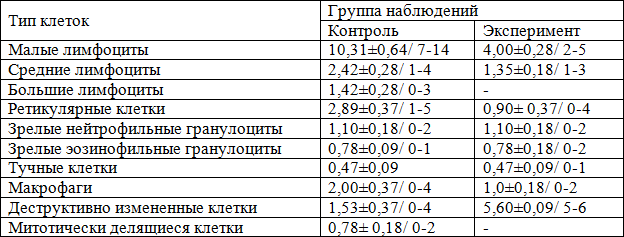
Согласно данным табл. 2, у мышей экспериментальной группы, сравнительно с контролем, в красной пульпе селезенки абсолютное содержание (плотность, количество) малых лимфоцитов уменьшается в 2,58 раза (р<0,05), средних лимфоцитов – в 1,79 раза (р<0,05), ретикулярных клеток – в 3,21 раза (р<0,05), макрофагов – в 2,0 раза (р<0,05).
В экспериментальной группе у мышей в составе красной пульпы селезенки, по сравнению с контролем, возрастает абсолютное содержание деструктивно измененных клеток лимфоидного ряда (в 3,66 раза, р<0,05). В красной пульпе селезенки мышей экспериментальной группы, по сравнению с контролем, большие лимфоциты и митотически делящиеся клетки лимфоидного ряда почти не определяются (отсутствуют или единичные).
Заключение. После 70 суток радиационного воздействия происходит снижение уровня иммунной защиты, морфологическим эквивалентом которой является лимфоидная ткань.
Известно, что малые лимфоциты и макрофаги являются наиболее активными участниками иммунных реакций [10,11], снижение их содержания отражает развитие иммунодефицитных состояний [1]. Вместе с уменьшением лимфоцитопоэтических процессов (отсутствие юных форм клеток лимфоидного ряда – митотически делящихся клеток, плазмобластов, больших лимфоцитов после облучения) нарастает уровень клеточной деструкции лимфоидной ткани. Соответствующие нашим результатам данные приводят А.И. Андреев [2], исследовавшие действие средневолнового ультрафиолетового излучения на лимфоидные структуры у мышей.
Выявленные факты в целом соответствуют и концепции М.Р. Сапина [8] о значительной структурно-функциональной динамичности органов иммунной системы в целом, ее лабильности, способности реагировать на действие любых внешних и внутренних факторов, не всегда адекватных.
Таким образом, в результате комплексного морфологического исследования были получены новые и ценные данные о структурной организации белой пульпы селезенки мышей в условиях нормы. Полученные материалы доказали повреждающее долговременное действие радиации низкой интенсивности по отношению ко всем компонентам белой пульпы этого органа, а также достаточно высокие ее регенераторные возможности.
