Введение. На сегодняшний день хроническая рецидивирующая крапивница (ХРК) занимает одно из ведущих мест в аллергопатологии и представляет собой сложную медико-социальную проблему [8]. В структуре ХРК выделяют аутоиммунную форму (ХАК), которая по данным разных авторов составляет от 30 до 50% [10, 12]. Пациенты с аутоиммунным механизмом развития крапивницы имеют наиболее тяжелое течение заболевания и с трудом поддаются лечению. Иммунные механизмы с участием цитокинов играют главную роль в патогенезе ХАК и до настоящего времени остаются мало изученной проблемой. Известно, что при аутоиммунных заболеваниях происходит активация CD4+ популяции по типу Th1, которая характеризуется избыточным синтезом интерферона-гамма (ИФН-γ) и ИЛ-17 [11]. Высокие концентрации ИФН-γ могут запускать аутоиммунный процесс и оказывать регулирующее действие на рецепторы клеток-мишеней [14]. Противоположным действием обладает ИЛ-10, который подавляет этот процесс и участвует в реакциях аутоиммунитета [16]. Участие в патогенезе ХАК ИЛ-18 доказано в плане фактора, высвобождающего гистамин [15]. В настоящее время актуальным направлением в лечении больных с аутоиммунным механизмом крапивницы является применение внутривенных иммуноглобулинов, одним из которых является отечественный препарат Габриглобин. Однако влияние данного препарата на иммунокомпетентные клетки (ИКК) больных ХАК не изучено. В последние годы проводятся многочисленные исследования с применением тестов ex vivo с целью изучения влияния лекарственных препаратов на состояние клеток иммунной системы, прогнозирования развития аллергических заболеваний [5, 6]. Метод ex vivo по мнению большинства исследователей должен занять центральное место в современной иммунодиагностике [9]. Преимуществами данного метода перед методами in vitro является использование цельной крови без выделения клеточных культур, что упрощает методику анализа и снижает нежелательную активацию или гибель клеток. Также, культивирование клеток крови идет в более естественном окружении, сохраняется баланс всех гуморальных факторов, что соответствует условиям in vivo.
Цель работы. Отработка диагностически значимой дозы препарата Габриглобин для оценки влияния данного препарата на продукцию цитокинов ИКК у больных ХАК.
Материалы и методы. В исследование было включено 22 пациента с хронической аутоиммунной крапивницей до и после лечения препаратом Габриглобин. Средний возраст пациентов составил 47±12 лет. В контрольную группу вошло 15 здоровых лиц, сопоставимых по полу и возрасту с основной группой. Диагноз ХАК устанавливался на основании жалоб, данных анамнеза, клинической картины, длительности заболевания, анализа данных сопутствующих заболеваний. Для подтверждения диагноза всем пациентам ставилась проба с аутосывороткой [13]. В исследование были взяты пациенты, имеющие положительную пробу с аутосывороткой диаметром 7 мм и более, которая является диагностическим критерием ХАК [4]. Подбор диагностически значимой дозы Габриглобина производился на 15 здоровых донорах методом ex vivo, в основе которого лежала запатентованная работа Исаченко Е.Г. о способе оценки резервных возможностей ИКК [7]. Критерий, по которому подбиралась диагностически значимая доза Габриглобина был процент здоровых людей с максимальной выработкой цитокинов ИЛ-10, ИЛ-17, ИЛ-18 и ИФН-γ ИКК [2]. В работе были использованы концентрации Габриглобина 1:1, 1:3, 1:10. Пациентам до и после лечения препаратом Габриглобин был проведен тест ex vivo с диагностически значимыми концентрациями данного препарата.
Способ осуществления метода ex vivo
1 этап – забор крови. Кровь отбирали из локтевой вены в стерильную силиконизированную пробирку с гепарином. Далее кровь разбавляли в 5 раз стерильной питательной средой 199 с глутамином («Биолот», Санкт-Петербург).
2 этап – инкубация крови, стимулированной Габриглобином для выработки ИКК цитокинов ИЛ-10, ИЛ-17, ИЛ-18 и ИФН-γ. Для этого в 3 пробирки добавляли по 675 мкл разбавленной в 5 раз крови, далее в 1-ю пробирку - 75 мкл Габриглобина в концентрации 1:1, во 2-ю – 75 мкл Габриглобина в концентрации 1:3, в 3-ю – 75 мкл Габриглобина в концентрации 1:10. Пробирки инкубировали в термостате в течении 6 часов при 37°С. Затем охлаждали и центрифугировали 5 минут при 800g. Супернатант отбирали и замораживали при -20°С.
3 этап – определение концентрации цитокинов ИЛ-10, ИЛ-17, ИЛ-18 и ИФН-γ в супернатанте методом иммуноферментного анализа наборами ЗАО «Вектор-Бест» (г. Новосибирск).
Статистическая обработка результатов проводилась на персональном компьютере с помощью пакета прикладных программ «STATISTICA 6.0». Качественные переменные описывались абсолютными и относительными частотами, количественные переменные представлялись в виде медианы (Ме) и интерквартильного размаха от 25 до 75%. Сравнение количественных признаков в независимых группах проводили по методу Манна-Уитни, в зависимых – с использованием критерия Вилкоксона. Результаты считали достоверными при р<0,05.
Результаты исследования и их обсуждение. В ходе работы были получены следующие результаты. Как видно из данных табл. 1, у 67% здоровых людей максимальная выработка ИКК ИЛ-10 наблюдалась при концентрации Габриглобина 1:3, у 22% - при концентрации 1:10 и лишь у 11% при концентрации препарата 1:1. Из этого следует, что оптимальной концентрацией Габриглобина для выработки ИКК ИЛ-10 является концентрация 1:3. При изучении показателей выработки ИКК ИЛ-17 было установлено, что у 50% здоровых людей максимальная выработка ИКК достигалась при концентрации Габриглобина 1:3, у 30% - при концентрации Габриглобина 1:1 и у 20% - при концентрации 1:10. Поэтому, оптимальную концентрацию Габриглобина для выработки ИКК ИЛ-10 составляет концентрация 1:3. Также в работе было установлено, что у 70% здоровых доноров максимальная продукция ИКК ИЛ-18 наблюдалась при концентрации Габриглобина 1:10, у 20% - при концентрации 1:1 и лишь у 10% - при концентрации 1:3. Из это следует, что диагностически значимой концентрацией Габриглобина по выработке ИКК ИЛ-18 является концентрация 1:10. При исследовании показателей продукции ИФН-γ было выявлено, что оптимальной концентрацией Габриглобина является концентрация 1:3, так как у 60% здоровых людей максимальная продукция этого цитокина ИКК была именно при концентрации Габриглобина 1:3 и лишь у 40% - при концентрации 1:10.
Таблица 1. Отработка диагностически значимых доз препарата Габриглобин в тесте ex vivo на здоровых людях
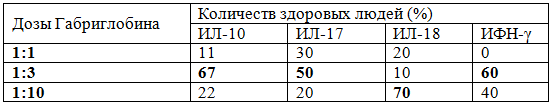
Таким образом, при изучении показателей продукции ИКК ИЛ-10, ИЛ-17, ИЛ-18 и ИФН-γ было выявлено, что диагностически значимая концентрация Габриглобина для выработки ИЛ-10, ИЛ-17, ИФН-γ составила концентрация 1:3, а для ИЛ18 – концентрация 1:10.
Следующим этапом работы было изучение влияния диагностически значимых доз препарата Габриглобин на выработку ИКК цитокинов ИЛ-10, ИЛ-17, ИЛ-18 и ИФН-γ у больных ХАК в сравнении с показателями цитокинов у здоровых людей. Как видно из данных табл. 2, в группе больных ХАК наблюдался достоверно более высокий уровень ИЛ-17 (р=0,00123). Это согласуется с данными об участии ИЛ-17 в развитии аутоиммунной патологии и о повышенном уровне данного цитокина у больных ХАК [3, 16]. При изучении показателей цитокинов ИЛ-10, ИЛ-18 и ИФН-γ в группе больных по сравнению с контрольной группой достоверных различий выявлено не было.
Следующим разделом работы было сравнительное исследование изучаемых цитокинов с диагностически значимыми концентрациями Габриглобина у больных ХАК до и после лечения данным препаратом. Согласно полученным результатам (таблица 2) было выявлено достоверное снижение уровня ИЛ-10 (р=0,0277) в группе больных ХАК после лечения препаратом Габриглобин по сравнению с группой больных до лечения. Этот факт можно объяснить тем, что после лечения препарат Габриглобин способствует связыванию и изменению свойств иммунных комплексов, а также выведению патологических аутоантител при аутоиммунной патологии [1]. При изучении показателей цитокинов ИЛ-17, ИЛ-18 и ИФН-γ у больных ХАК до и после лечения препаратом Габриглобин достоверных различий выявлено не было.
Таблица 2. Сравнительная оценка влияния диагностически значимых доз препарата Габриглобин на выработку цитокинов ИКК у больных ХАК до и после лечения данным препаратом и здоровых лиц
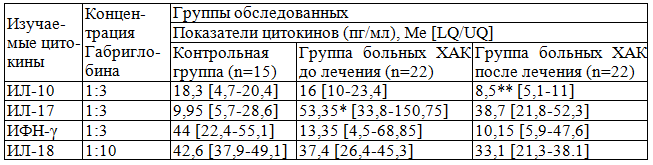
Примечания: *- достоверность различий показателей цитокинов у больных до лечения и здоровых людей; ** - достоверность различий показателей цитокинов у больных до и после лечения
Выводы
1. Отработана диагностически значимая концентрация препарата Габриглобин для ИЛ-10, ИЛ-17, ИФН-γ в тесте ex vivo, которая составляет 1:3, а для ИЛ-18 – концентрация 1:10.
2. Сравнительный анализ выработки ИКК ИЛ-10, ИЛ-17, ИЛ-18 и ИФН-γ под влиянием диагностически значимых концентраций препарата Габриглобин показал достоверно более высокий уровень ИЛ-17 в группе больных ХАК до лечения по сравнению с аналогичными показателями в группе здоровых лиц.
3. У больных ХАК после лечения препаратом Габриглобин в тесте ex vivo был выявлен более низкий уровень ИЛ-10 по сравнению с больными до лечения.
