Введение. Охрана здоровья ребенка должна начинаться с пренатального периода. В настоящее время среди неблагоприятных факторов, которые могут оказывать влияние на организм будущей матери, значительную роль играют лекарственные средства [2]. По данным венгерской службы контроля за врожденными аномалиями, тератогены окружающей среды бывают причиной возникновения аномалий развития плода приблизительно в 3% случаев, из них 1% приходится на долю лекарственных препаратов [9]. Результаты исследований зарубежных авторов показывают, что 64-83% женщин принимают во время беременности хотя бы один лекарственный препарат [12]. По данным Всемирной организации здравоохранения (ВОЗ), в течение беременности женщина в среднем принимает 5 фармакологических препаратов [4].
Встает вопрос о переносимости или вреде препарата для будущего ребенка, который является «дополнительным пациентом», что требует строгого выбора показаний для лечения матери. Для перехода чужеродных веществ через плаценту решающую роль играет их низкая молекулярная масса (менее 600-800), характерная для большинства фармацевтических средств [1]. Концентрация лекарственных препаратов на фетальной стороне плаценты может достигать 20-80% концентрации в организме матери [11].
Лекарственную терапию при серьезных заболеваниях (бронхиальная астма, сахарный диабет, эпилепсия, тяжелые инфекции и т.д.) обязательно следует проводить во время беременности, но избегать назначения, так называемых «поддерживающих беременность», препаратов и других нерациональных терапевтических веществ, поскольку риск их применения нередко превосходит приносимую ими пользу [15]. По данным американского врача-тератолога L.Holmes [10] известно не более 30 лекарственных препаратов, тератогенное и эмбриотоксическое действие которых доказано.
Если отрицательное действие лекарственных средств во всех областях медицины почти всегда имеет обратимый характер, устранимо при отмене или даже снижении дозы, то в акушерстве оно может оказаться фатальным: ребенок, родившийся с медикаментозно обусловленным нарушением внутриутробного развития, будет страдать от него в течение всей жизни [7]. При этом речь идет не только о грубых анатомических (морфологических) дефектах, выявляемых сразу после рождения и чаще всего инвалидизирующих человека, но и о функционально-метаболических нарушениях, психических и поведенческих отклонениях, которые могут проявиться в любом периоде постнатального онтогенеза [14]. В перинатологии, как ни в одной другой области медицины, требуется умение ограничить число используемых медикаментов вследствие крайней непредсказуемости лекарственных взаимодействий [5].
Известно, что ферментные системы у плода не вполне развиты. Отсюда следует вывод о недостаточном, либо неполном разрушении лекарств в его организме. Особенно это очевидно, когда речь идет о ранних стадиях эмбриогенеза [13]. Система конъюгации лекарств с глюкуроновой кислотой начинает полноценно функционировать только через 50 дней от момента рождения. Следовательно, те препараты, которые были введены матери незадолго до родов, могут оказывать действие на ребенка еще достаточно долго [5]. В настоящее время оспаривается польза широко рекламируемых и назначаемых поливитаминных препаратов для беременных, поскольку потребность в витаминах восполняется сбалансированным питанием, а жирорастворимые витамины в высоких дозах могут быть токсичными для плода [6].
В большинстве стран мира для организации безопасного лечения во время беременности введена специальная маркировка лекарственных средств. Она содержит информацию о степени риска применения препарата во время беременности и уровне исследований, доказывающих его безопасность. Например, классификация, введенная правительством Австралии (An Australian categorization of risk of drug use in pregnancy) и Управлением питания и медикаментами США (FDA – US Food and Drug Administration), очень схожи и содержат 5 основных категорий от «А» (безопасные) до «D» (противопоказанные во время беременности). Выделяют также категорию «Х», в которую включены препараты, абсолютно противопоказанные во время беременности [8].
Изучение влияния лекарственной терапии матери на раннюю адаптацию младенцев в настоящее время остается окончательно нерешенной и актуальной проблемой.
Цель настоящего исследования – определение фармакотерапии в антенатальном периоде и особенностей адаптации новорожденных.
Методы. Проведено ретроспективное когортное исследование на основании медицинской документации (журнал родов, диспансерные карты беременных – ф. №113, истории родов – ф. №96/у, истории развития новорожденных – ф. №097/у) родильного отделения Областной клинической больницы г. Архангельска за период 2012-2013 г. Критерием включения в группу обследуемых новорожденных был относительно благоприятный фон беременности и родов (доношенная одноплодная беременность; отсутствие тяжелых осложнений беременности (преэклампсия, эклампсия); отсутствие обострений хронических заболеваний; роды per vias naturalis; отсутствие слабости родовых сил, потребовавшей медикаментозного родоусиления). Критерием исключения являлась неонатальная желтуха при изоиммунном конфликте по эритроцитарным антигенам. На основании представленных критериев проанализирована медицинская документация 100 беременных и родильниц и их новорожденных. При анализе материала сформировали две группы младенцев. Основную (I) группу составил 51 доношенный новорожденный от матерей, наблюдавшихся в течение беременности в женских консультациях города Архангельска. В группу сравнения (II) включены 49 доношенных новорожденных от матерей, наблюдавшихся во время беременности в женских консультациях районов области.
Статистическая обработка результатов проводилась с помощью пакета статистических программ SPSS 18.0. Подчинение количественных данных закону нормального распределения оценивалось с помощью критерия Shapiro-Wilk. Параметрические данные описаны средними значениями (М) и стандартными отклонениями (SD); непараметрические – с помощью медианы (Mе), первого и третьего квартилей (Q1; Q3). Качественные признаки представлены как абсолютные частоты и процентные доли, сравнение – с помощью точного критерия Фишера. Сравнивали группы по количественным признакам с использованием Mann-Whitney U-test. Для данных, имеющих нормальное распределение, использовали параметрический t-test Стьюдента. Связь между переменными рассчитывали с помощью коэффициента корреляции Кендалла (τ). Критический уровень значимости (р) принимался равным 0,05. Для определения категории токсичности лекарственного средства использовали американскую классификацию FDA, основанную на данных экспериментальных и клинических исследований [8].
Результаты и их обсуждение. Все женщины на ранних сроках беременности встали на учет в женские консультации. Средний возраст родильниц исследуемой выборки (100 человек) составил 28±5,6 лет. При анализе возрастного состава отмечено двое юных первородящих 17 лет. Примерно одинаковое количество женщин направлялись для родоразрешения в областную клиническую больницу из областного центра и районов Архангельской области (51% и 49%, соответственно). Анализ трудовой занятости показал преобладание работающих женщин (83%). Отсутствие регистрации брака отмечено в 32% случаев, каждая пятая из этих женщин вынуждены воспитывать детей в одиночку. 31% женщин являлись первобеременными, 16% повторнобеременными первородящими (имели в анамнезе аборты и выкидыши) и 53% повторнобеременными повторнородящими.
Анализ экстрагенитальной патологии (миопия, хронический пиелонефрит, вегетососудистая дистония) и осложнений беременности (анемия, кольпит, угроза выкидыша, фетоплацентарная недостаточность, многоводие, маловодие) у женщин, наблюдавшихся в течение беременности в женских консультациях города Архангельска (n=51) и районов области (n=49) не выявил статистически значимых различий.
При анализе диспансерных карт отмечено, что 39% беременных не назначались лекарственные средства в сроке до 12 недель гестации. 48% женщин в указанном сроке получали до 4-х лекарственных препаратов и 13% беременных получали от 5 до 14 лекарственных средств в первом триместре беременности. Наиболее часто назначались фолиевая кислота, поливитамины, папаверин, витамин Е, дюфастон. Общее количество наименований лекарственных препаратов составило 28.
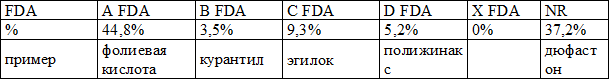
При оценке токсичности лекарств во время беременности по классификации FDA отмечено, что в 1 триместре из общего количества назначаемых лекарственных препаратов 37% относились к категории неидентифицированных (табл. 1), т.е. отсутствует информация о влиянии лекарственного препарата на плод и новорожденного.
Таблица 1. Распределение лекарственных средств по категориям токсичности в первом триместре беременности
В сроке от 13 до 26 недель гестации 42% беременным не назначались лекарственные средства. 48% женщин в указанном сроке получали до 4-х лекарственных препаратов и 10% беременных подвергались полипрагмазии, получая от 5 до 8 лекарственных средств во втором триместре беременности. Наиболее часто в эти сроки назначались поливитамины, папаверин, препараты железа, курантил, магний. Общее количество наименований лекарственных препаратов составило 24.
Таблица 2. Распределение лекарственных средств по категориям токсичности во втором триместре беременности
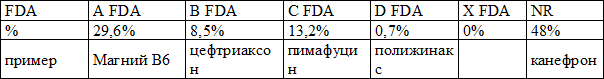
При оценке токсичности лекарств во время беременности по классификации FDA отмечено, что во 2 триместре из общего количества назначаемых лекарственных препаратов половина относились к категории неидентифицированных (табл. 2), что свидетельствует об отсутствии систематических исследований токсического действия на развитие плода.
В сроке от 27 недель до родов только 17% беременным не назначались лекарственные средства. 50% женщин в указанном сроке получали до 4-х лекарственных средств, и 33% беременным назначалось от 5 до 11 лекарственных препаратов в третьем триместре беременности. Наиболее часто в эти сроки назначались препараты железа, курантил, поливитамины, папаверин, гинипрал. Общее количество наименований лекарственных препаратов составило 30.
Таблица 3. Распределение лекарственных средств по категориям токсичности в третьем триместре беременности

При оценке токсичности лекарств во время беременности по классификации FDA отмечено, что в 3 триместре из общего количества назначаемых лекарственных препаратов примерно половина относились к категории неидентифицированных (табл. 3). При назначении лекарственного средства в период беременности следует тщательно оценивать соотношение ожидаемого терапевтического эффекта для будущей матери и возможного риска для плода.
Максимальное количество лекарственных препаратов, назначенных за весь период беременности, составило 16. Только 11% женщин не подвергались медикаментозной терапии.
Таблица 4. Среднее количество назначенных лекарственных препаратов беременным, проживающим в г. Архангельске и районах области
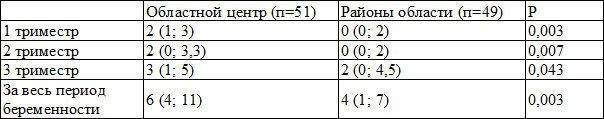
Примечание: здесь и далее данные представлены как Mе (Q1; Q3)
Отмечено, что в областном центре лекарственные препараты назначались в 1,5-2 раза чаще, чем в районах области. Получены статистически значимые различия (табл. 4). Возможно, это связано с более высокой приверженностью к лекарственной терапии и лучшим материальным положением городских жительниц по сравнению с женщинами из районов области.
Оценка состояния новорожденных по шкале Апгар на 1 минуте составила в I группе (n=51) 8 (7; 8) баллов, во II группе (n=49) 8 (8; 8) баллов, U=1160, Z=-0,81, р=0,41; на 5 минуте 8 (8; 9) и 9 (8; 9) баллов, соответственно, U=1174, Z= -0,58, р=0,56.
Таблица 5. Антропометрические показатели новорожденных
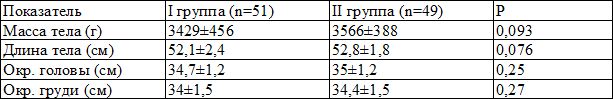
Анализ антропометрических показателей новорожденных обеих представленных групп не выявил статистически значимых различий (табл. 5).
Таблица 6. Показатели гемограммы новорожденных на вторые сутки жизни
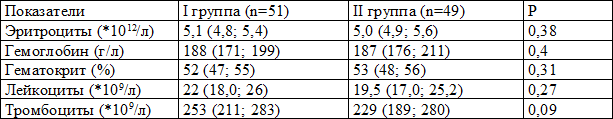
При оценке гематологических показателей на вторые сутки жизни не было выявлено статистически значимых различий в обеих группах детей по содержанию тромбоцитов, лейкоцитов, эритроцитов, уровню гемоглобина и гематокрита (табл. 6).
Таблица 7. Показатели эозинофилов в крови новорожденных на вторые сутки жизни
![]()
При сравнительном анализе отмечены статистически значимые различия показателей эозинофилов (табл. 7) в крови новорожденных I и II групп, что может указывать на высокий риск аллергоидной реакции при высокой медикаментозной нагрузке в антенатальном периоде. Проявления токсической эритемы в раннем неонатальном периоде положительно коррелировали с количеством лекарственных препаратов в течение беременности, τ=0,32, р=0,001.
Большинство новорожденных находились в роддоме на исключительно грудном вскармливании, около 20% младенцев обеих групп нуждались в докормах. Максимальная убыль массы тела у новорожденных I группы составила 5,7% (4; 7), во II группе 5% (4; 7), U=1103, Z = -1,01, р=0,31.
У младенцев I группы в раннем неонатальном периоде превалировала желтуха неуточненной этиологии (37% детей), также отмечены внутриутробная гипотрофия (6%) и хроническая гипоксия (6%), родовая травма (4%) в виде кефалогематомы и перелома ключицы, кардиопатия (2%) – подозрение на врожденный порок сердца. В детскую больницу переведено 3 (5%) младенца для обследования и лечения. 45% детей выписывались домой с заключением «здоров».
У детей II группы наблюдались: кефалогематома (4%), внутриутробная гипотрофия (8%), гидронефроз почки (2%), кардиопатия (4%) – подозрение на врожденный порок сердца. По сравнению с 1 группой реже наблюдалась неонатальная желтуха неуточненной этиологии (18%), потребовавшая фототерапии, χ2=4,42, df=1, p=0,035. В детскую областную больницу переводились 3 (6%) ребенка для обследования и лечения. 64% детей выписаны домой здоровыми. Отмечена статистически значимая взаимосвязь между количеством лекарственных препаратов в третьем триместре беременности и неонатальной желтухой, τ = 0,38, р=0,001.
Выводы
1. Во время беременности 89% женщин получают лекарственные препараты.
2. От 10% женщин в первом триместре гравидарного периода до 33% беременных в третьем триместре подвергаются полипрагмазии (от 5 до 11 лекарственных препаратов).
3. Отмечена статистически значимая взаимосвязь между количеством лекарственных препаратов в третьем триместре беременности и неонатальной желтухой.
4. Проявления токсической эритемы в раннем неонатальном периоде положительно коррелировали с количеством лекарственных препаратов в течение беременности.
5. Поскольку данных о клинической фармакологии во время беременности недостаточно, в этот период жизни женщины желательно избегать назначения лекарств, если только не имеется абсолютных показаний к их применению.
6. Любое вмешательство в здоровье будущей матери, тем более медикаментозное, должно быть жестко определено, регламентировано и четко обосновано, чтобы исключить неблагоприятный эффект.
