Актуальность проблемы. В настоящее время инсульт рассматривается не только как отдельная неврологическая проблема, но и исследуется во взаимосвязи с уровнем функционирования всех звеньев многосложного аппарата кровообращения. Одним из важных направлений исследований является изучение цереброгенных влияний на сердечно-сосудистую систему, степень изменения вегетативного баланса и регуляции сердечного ритма, что во многом определяет возможность рецидива заболевания, развития аритмического синдрома и усугубление течение ишемической болезни сердца (ИБС) [1-2,6].
Поэтому больные с перенесенным ишемическим инсультом, особенно когда он является проявлением мультифокального атеросклероза, относятся к группе высокого абсолютного риска сердечно-сосудистых событий и нуждаются в своевременном проведении дифференцированных превентивных воздействий [3-5].
В ряде исследований были проанализированы показатели вариабельности сердечного ритма (ВСР) и аритмического синдрома в остром и раннем реабилитационном периодах ишемического инсульта, установлено снижение у таких пациентов всех показателей вегетативной регуляции сердечной деятельности, были проанализированы влияния локализации ишемического очага, патогенетического подтипа инсульта [8-12].
Но при ведении таких больных, тем более при возрастающих возможностях современной терапии, важен и долгосрочный реабилитационный прогноз, на который влияет как степень нарушения вегетативной регуляции, так и наличие сопутствующей кардиальной патологии.
Материалы и методы. Проведено комплексное клинико-функциональное обследование 32 больных ИБС (средний возраст 67±2,1 лет) в позднем реабилитационном периоде ишемического инсульта (от 6 до 12 месяцев после перенесенного острого нарушения мозгового кровообращения).
У всех обследуемых диагностированы различные клинические проявления ишемической болезни сердца: стенокардия, перенесенный инфаркт миокарда, пароксизмальные нарушения ритма, хроническая сердечная недостаточность. Характер и локализация очагового поражения головного мозга распознавались по данным амбулаторных карт, результатам осмотра невролога, протоколам компьютерной или магнитно-резонансной томографии. Все больные разделялись на 3 группы: I группа – 14 пациетов с инсультом в бассейне левой среднемозговой артерии (ЛСМА), II группа – 10 больных с инсультом в бассейне правой среднемозговой артерии (ПСМА) и III группа - 8 больных с острым нарушением мозгового кровообращения (ОНМК) в вертебро-базилярном бассейне (ВББ). Контрольную группу (ГК) составили 20 практически здоровых лиц (с отсутствием неврологических нарушений и заболеваний сердечно-сосудистой системы), средний возраст 57,2±5,3 года.
Всем пациентам было проведено клинико-анамнестическое исследование с детализацией факторов риска и данных о сопутствующей кардиальной патологии, наличии атеросклероза экстракраниальных артерий.
Инструментальное обследование включало проведение суточного мониторирования ЭКГ по Холтеру (ХМЭКГ) При этом обращалось внимание на характер нарушений сердечного ритма и проводимости, ишемических изменений.
Оценка вариабельности сердечного ритма (ВСР) включала в себя такие показатели, как:
- SDNN – стандартное отклонение NN, отражающее все циклические компоненты, ответственные за вариабельность в течение периода записи;
- SDNN index (SDNNi) – среднюю 5-минутных стандартных отклонений NN интервалов, вычисленных за 24 часа, отражающий вариабельность с цикличностью менее 5 минут;
- pNN50 – количество случаев, в которых разница между длительностью последовательных NN, превышает 50 мс, отражает быстрые высокочастотные колебания в структуре ВСР.
- спектральный анализ ВСР с определением следующих компонентов: мощности высокочастотных (HF), низкочастотных (LF) и очень низкочастотных колебаний (VLF).
Статистическая обработка данных проводилась с помощью программ Microsoft Excel 2010, Statistica 6.0 (StatSoft).
Результаты и обсуждение. При анализе показателей средних значений частоты сердечных сокращений (ЧСС) и циркадного индекса (отношение дневной и ночной ЧСС) выявлено резкое снижение циркадных показателей сердечного ритма, что свидетельствует о значительном истощении регуляторных механизмов организма, возникших в результате перенесенного нарушения мозгового кровообращения, и непосредственного влияния имеющейся кардиальной патологии. Статистически значимое снижение циркадного индекса (p<0,01) выявлено во всех группах больных, что является прогностически неблагоприятным для возможного развития аритмий (табл. 1).
Таблица 1. Сравнение показателей циркадной динамики ЧСС у обследуемы
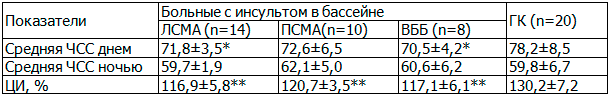
Примечания: здесь и далее *p<0,05 при сравнении с ГК, ** p<0,01 при сравнении с ГК.
Анализ выявленных у обследуемых с мультифокальными проявлениями атеросклероза нарушений сердечного ритма показал, что наиболее часто регистрировались наджелудочковые аритмии: одиночная экстрасистолия (НЖЭС) – 100% случаев, парная (68,7%) и групповая НЖЭС (31,3%). Пароксизмы наджелудочковой тахикардии (НЖТ), преимущественно короткие, обнаружены у 18,8 % больных. Особое внимание обращают на себя эпизоды фибрилляции предсердий (ФП), которые были выявлены у 25 % обследованных. Большое количество наджелудочковых нарушений ритма и эпизодов фибрилляции предсердий характерно и для раннего периода инсульта [7]. Желудочковые нарушения ритма были представлены одиночной экстрасистолией (ЖЭС) – у 66,7% лиц, парной и групповой ЖЭС – у 18,8%. Пароксизмы желудочковой тахикардии выявлены у 3% больных.
Нарушения проводимости в виде блокады ножек и ветвей пучка Гиса, эпизодов атриовентрикулярной блокады установлены у 15,6% пациентов; эпизоды синоатриальной блокады, выскальзывающие комплексы, клинически значимые паузы зарегистрированы у 6% больных в позднем периоде инсульта. Следует учитывать, что проведение проб с физической нагрузкой было затруднено наличием двигательных расстройств у больных в результате перенесенного инсульта.
При изучении показателей ВСР во всех группах обследуемых установлено достоверное значительное снижение как статистических, так и частотных параметров при сравнении с контрольной группой (табл. 2). Следует отметить, что у больных перенесших ОНМК в бассейне левой среднемозговой артерии (ЛСМА) были снижены показатели суммарной регуляции сердечной деятельности (параметр VLF, p<0,05), а у больных с ишемическим инсультом в ВББ была снижена мощность высокочастотного компонента спектра, в обоих случаях в сравнении с группой с ОНМК в бассейне правой среднемозговой артерии (ПСМА).
Таблица 2. Показатели ВСР у пациентов с ИБС в позднем периоде инсульта
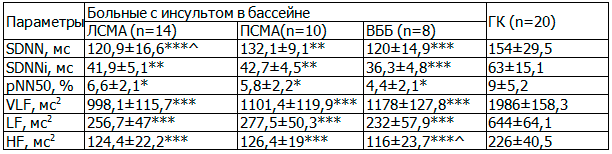
Примечания: *** p<0,001 при сравнении с ГК, ^ p<0,05 при сравнении с группой ПСМА.
Среди пациентов в позднем реабилитационном периоде инсульта у 12 (37,5%) был диагностирован перенесенный инфаркт миокарда. При сравнении показателей ВСР у этих больных и обследуемых без инфаркта в анамнезе (табл. 3) было выявлено статистически достоверное снижение у этой группы лиц показателя суммарной регуляции сердечной деятельности (VLF, p<0,01), а также ослабление влияния вегетативной нервной системы (LF, p<0,01 и HF, p<0,05). Кроме этого отмечалось также снижение всех циклических влияний на регуляцию ВСР – уменьшение показателя SDNNi (p<0,05).
Таблица 3. Показатели ВСР у обследуемых с перенесенным инфарктом миокарда

У 20 больных (62,5%) была выявлена хроническая сердечная недостаточность (ХСН), При сравнительном анализе показателей вариабельности сердечного ритма у таких пациентов (n=20) и лиц без явлений ХСН (n=12). У пациентов с недостаточностью кровообращения было выявлено снижение общей вариабельности сердечного ритма – показатели SDNN (p<0,05), SDNNi (p<0,01) и преобладание симпатического компонента вегетативной нервной системы – параметра LF (*p<0,05) при спектральном анализе.
Таблица 4. Влияние ХСН на регуляцию сердечного ритма
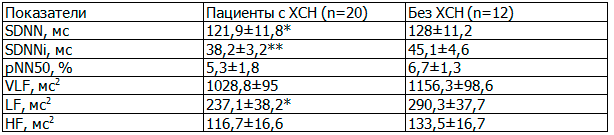
Таким образом, проведенное исследование показывает значение анализа нарушений сердечного ритма и его регуляции у больных с ИБС в позднем периоде ишемического инсульта. Установлено, что наличие у больных таких проявлений мультифокального атеросклероза, как перенесенный ишемический инсульт и ИБС оказывает взаимоотгягощающее влияние на все уровни регуляции сердечного ритма, включающее как центральные, так и кардиоцеребральные патологические воздействия. На показатели вегетативного баланса в позднем реабилитационном периоде инсульта влияют такие факторы как особенности клинических проявлений ИБС, перенесенный инфаркт миокарда, характер сердечных дизритмий, наличие ХСН. Полученные данные показывают, что больные с предшествующими эпизодами ОНМК нуждаются в углубленном кардиологическом обследовании, включающем холтеровское мониторирование ЭКГ, с целью определения тактики высокодифференцированных реабилитационных воздействий.
