Введение. Рак молочной железы – лидирующая онкологическая патология. Ежегодно в мире регистрируют более 1000000 новых случаев рака молочной железы. В России в 2005 г. было выявлено 49548 новых случаев заболевания, что составляет примерно пятую часть (19,8%) всех опухолей у женщин, а число умерших составило 22830 (17,3%) [3]. Лечение больных раком молочной железы включает несколько этапов, таких как хирургическое лечение (радикальная резекция молочной железы или мастэктомия) в сочетании с химиолучевым лечением. Показаниями для выполнения радикальной мастэктомии являются: локализация опухоли в центральном секторе молочной железы, местно-распространенная форма заболевания, небольшой размер молочной железы, отказ больной от сохранения молочной железы. Таким образом, большая часть больных нуждаются в расширенном хирургическом лечении, таком как радикальная мастэктомия по Маддену [4]. Серома или лимфоцеле является самым распространенным осложнением после радикальной мастэктомии. В различных публикациях частота развития серомы после хирургического лечения рака молочной железы составляет от 25% до 81% оперированных больных [4,8-11]. Существует несколько способов профилактики лимфореи после радикальных мастэктомий. Наиболее распространенным является использования миопластики подмышечной области после выполнения хирургического пособия. Мышечный лоскут может быть взят из малой грудной мышцы, передней зубцатой мышцы и широчайшей мышцы спины [2]. Использование метода миопластики подмышечной области при радикальных мастэктомиях позволило на 98,2% уменьшить объем лимфореи на 14-й день, тем самым, сократив срок госпитализации на 14 дней [1,2]. Многие хирурги пытаются использовать адгезивные компоненты с целью снижения лимфореи после радикальных мастэктомий. Данные препараты «запечатывают» лимфатические и кровеносные сосуды, а также удерживать кожные лоскуты в контакте с грудной стенкой [5]. Фибриновый клей, распыленный в область послеоперационных ран после выполнения мастэктомии, снижал объеме лимфорейной жидкости. В своей статье Johnson с соавторами использовали фибринвый клей после радикальных мастэктомий и показали уменьшение в объемах лимфорейной жидкости [7]. В свою очередь Gilly с соавт. Установили [6], что использование фибринового клея значительно снижает объем лимфорейной жидкости и время пребывания больных в стационаре, однако не влияет на частоту развития лимфореи.
Цель исследования - оценка непосредственных результатов хирургического лечения рака молочной железы (РМЖ), выполненного путем распыления фибринового клея в комбинации с миопластикой подмышечной области.
Материалы и методы. Материалом исследования послужили 60 больных, верифицированным РМЖ, которым на этапе комплексного лечения была выполнена радикальная мастэктомия по Маддену (РМЭ): 30 пациентов (контрольная группа) – стандартная мастэктомия по Маддену и 30 пациентам (исследуемая группа) – мастэктомия по Маддену с комбинацией профилактических методов: распыление фибринового клея «Тиссукол кит» фирмой «Baxter» объемом 2 мл или 3 мл и миопластикой подмышечной области малой грудной мышцей. Методика выполнения операции в исследуемой группе отличалась от стандартной мастэктомии по Маддену следующим: после удаления молочной железы с опухолью и единым блоком подмышечной, подключичной и подмышечной клетчаток выполнялось распыление фибринового клея «Тиссукол-кит» фирмы «Baxter» объемом 2 или 3 мл в подмышечную область (рис. 1). По объему распыленного клея 30 больных распределились следующем образом: 2 мл фибринового клея было распылено - 11(36.6%) пациентам, 3 мл фибринового клея было распылено - 19(63.4%) пациентам. Фибриновый клей «Тиссукол кит» приготовлялся непосредственно перед нанесением на операционное поле путем смешивания лиофилизированного порошка Тиссукола и раствора апротинина. Фибриновый клей «Тиссукол кит» является двухкомпонентным, следовательно второй компонент приготовлялся путем смешивания лиофилизированного Тромбина 500 МЕ и раствора хлорида кальция. Для растворения компонентов фибринового клея использовалось специальное устройство «Фибринотерм» фирмы «Baxter». В ходе распыления фибринового клея операционное поле покрывалось равномерным слоем препарата, который образовывал «фибриновую пленку» на поверхности (рис. 2).
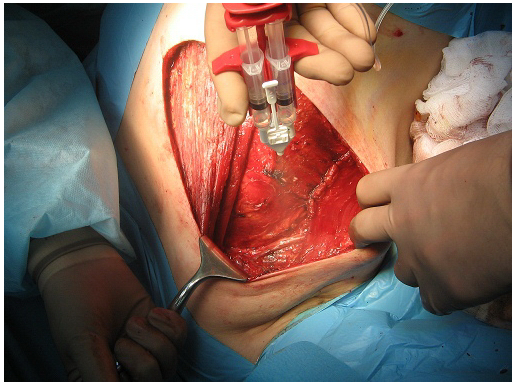
Рис. 1. Распыление фибринового клея
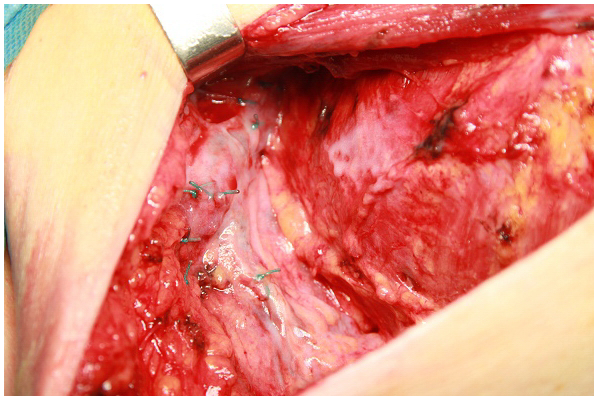
Рис. 2. «Фибриновая пленка»
Распыление выполнялось при помощи электрического распылителя «Изиспрей» фирмы «Baxter». Затем выполнялась миопластика подмышечной области мышечным трансплантантом из малой грудной мышцы. Медиальный край малой грудной мышцы отсекался от места прикрепления к грудной стенке (рис. 3).
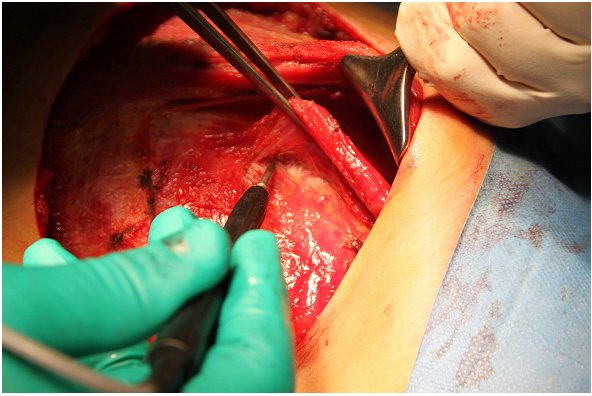
Рис. 3. Отсечение медиального края малой грудной мышцы
Далее мышечный лоскут укладывался вдоль подмышечных сосудов, тем самым заполняя пространство после выполнения регионарной лимфаденэктомии (ЛАЭ). Затем широчайшая мышца спины подшивалась к грудной стенке. Мышечный лоскут из малой грудной мышцы подшивался к грудной стенке. Подшивание лоскутов выполнялось плетеной рассасывающейся шовной нитью Викрил 3-0, фирма «Johnson & Johnson». Далее мобилизованные кожные лоскуты подшивались к грудной стенке. Таким образом, выполнялась миопластика подмышечной области с целью редукции объема пространства, оставленного после выполнения ЛАЭ (рис. 4). Далее выполнялось дренирование послеоперационной раны двумя силиконовыми дренажами. Послойное ушивание раны.
Результаты и обсуждение. Внедрение методики распыления фибринового клея в комбинации с миопластикой подмышечной области малой грудной мышцы показал высокую эффективность в отношении снижения продолжительности послеоперационной лимфореи и общего объема лимфы.
Таблица 1. Продолжительность лимфореи в группах больных

Как видно из табл. 1, новые хирургические методики значительно снижали продолжительность лимфореи. В контрольной группе продолжительность лимфореи составила 30.6±4,1 дня. В группе фибринового клея и миопластики продолжительность лимфореи составила 19,6±4,6 дня. Общий объем лимфы в послеоперационном периоде у больных в исследуемой группе составил 1464±678 мл, в контрольной группе 4368±1717 мл. В исследуемой группе использовался фибриновый клей разных дозировок: 2 мл и 3 мл. Логично предположить, что при увеличении дозировки фибринового клея продолжительность лимфореи и объем лимфы должны уменьшаться. Однако, в настоящей работе статистически значимых различий на продолжительность лимфореи не получено (Р<0.245). Отсутствие данного эффекта может быть объяснено малым количеством больных в выборках. Однако, продолжительность лимфореи при использовании фибринового клея 2 мл была незначительно меньше, и составил 17,8±4 дня, а при использовании фибринового клея 3 мл - 20,6±4.8 дней. Распыление фибринового клея и выполнение миопластики не повлияло на частоту послеоперационных осложнений. В исследуемой группе был 1 (1,1%) случай нагноения раны, в контрольной группе 2 (2.2%) случая; в исследуемой группе было 3 (3,3%) случая краевых некрозов раны, в контрольной группе 6 (6,6%) случаев. В обеих группах не было отмечено диастаза раны и развития кровотечения.
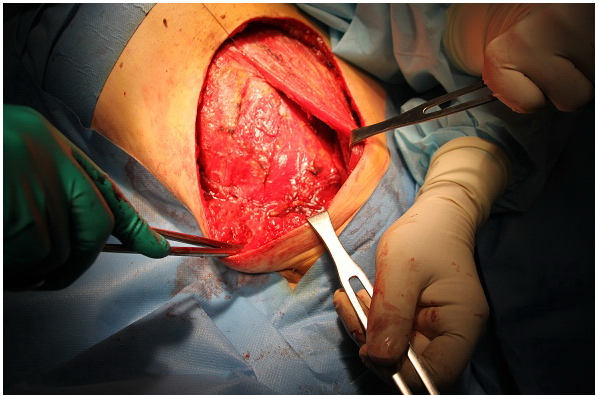
Рис. 4. Конечный вид миопластики подмышечной области
Выводы
1. Распыление фибринового клея в комбинации с миопластикой подмышечной области является эффективным способом профилактики лимфореи. Данный метод снижает продолжительность лимфореи и объем лимфы.
2. Внедрение новых хирургических методов снизило частоту послеоперационных осложнений таких как нагноение послеоперационной раны и краевые некрозы.
3. Единственным фактором, лимитирующим распространение распыления фибринового клея, является стоимость препарата и расходных материалов.
