Каждый год более 1 млн. женщин во всем мире заболевают раком молочной железы (РМЖ), который составляет почти четверть всех злокачественных опухолей у женщин. В России в структуре онкологической заболеваемости женщин РМЖ занимает 1-е место. Заболеваемость и смертность от этой болезни за 30 лет выросли в 4 раза: в 1970 г. стандартизованные показатели заболеваемости и смертности на 100 000 населения составляли 9,6 и 4,2; в 2000 − 38,3 и 17,2 соответственно [1]. За следующие 7 лет можно отметить дальнейший рост заболеваемости, и стабилизацию смертности. В 2007 г. в России РМЖ диагностирован у 51865 женщин, умерли от этой болезни 23064 больные [2].
При локальных формах РМЖ T1-2N0M0 у 10-20% больных развиваются метастазы в отдаленные органы и ткани в течение 2-3-х лет после радикальной операции. Более того, у больных с T2-3N1-2M0 у 30%-40% метастазы диагностируются в сроки 5-10 и более лет [3,4,5]. Средняя продолжительность жизни с момента выявления метастазов варьирует от 2 до 3,5 года, 25–30 % пациенток живут более 5 лет, 10 % – свыше 10 лет [6].
Основной задачей лечения диссеминированных форм РМЖ является продление жизни с удовлетворительным уровнем ее качества, что осуществляется путем проведения лекарственной терапии. За последнее десятилетие внедрены в практику новые эффективные цитостатики и разработаны новые режимы терапии. Все это дало возможность прогнозирования течения болезни и выбора обоснованной, индивидуализированной терапии РМЖ. Достигнутые успехи позволяют на сегодняшний день рассматривать метастатический РМЖ как хроническую болезнь, протекающую с периодическими обострениями, требующими того или иного вида лечения, и медленным постепенным ухудшением от обострения к обострению [7,8].
При выборе системного лечения метастатического РМЖ следует придерживаться индивидуального подхода с учетом биологических особенностей опухоли, целью которого является достижение максимальной эффективности при минимальной токсичности терапии. В последние годы в онкологии активно изучается проблема индивидуальной переносимости химиотерапии [9]. Кроме эффективности, интерес клиницистов привлекает переносимость химиотерапии, поскольку качество жизни является основным критерием оценки результатов лечения [10-12].
Лечение больных метастатическим РМЖ должно быть индивидуализировано с учетом основополагающих факторов прогноза. К ним относятся возраст больных, наличие или отсутствие гормональных рецепторов в опухоли, распространенность и локализация метастазов, экспрессия Her 2-Neu, Ki 86 и т.д. [13].
Метастатическое поражение печени при РМЖ по данным разных авторов, составляет 15-30%, тогда как, при аутопсии метастазы в печень выявляют у 30-50% больных. Высокая частота метастазирования в печень объясняется высоким печеночным кровотоком, двойным кровоснабжением (через печеночную артерию и воротную вену) и наличием фагоцитирующих купферовских клеток. Кроме того, оседанию в печени опухолевых клеток способствует ряд местных гуморальных факторов и свойства мембран эндотелиальных клеток.
У пациентов с метастазами РМЖ в печень, основным методом лечения является системная лекарственная терапия. РМЖ – опухоль, чувствительная к большинству современных противоопухолевых препаратов, среди них антрациклины, препараты таксанового ряда, винорельбин, капецитабин, препараты платины, гемцитабин, а так же некоторые таргетные препараты.
Цель данного исследования: сравнить различные варианты лекарственной терапии у больных РМЖ с метастазами в печень.
Материалы и методы. В работе обобщены результаты лечения 96 больных раком молочной железы стадий Т1-4N0-3М0-1, наблюдавшихся Российском научном центре рентгенорадиологии в 2000-2011 г. Всем пациенткам проводились различные варианты лекарственного лечения по поводу метастатического поражения печени, в сумме - 449 курсов химиотерапии.
Возраст больных варьировал от 34 до 75 лет, в среднем составив 50,9±4,7 лет. 19,8% (19) больных относились к IV стадии, то есть имели изначально метастатическое поражение печени, остальные больные до включения в исследование получили различные варианты лечения: неоадъювантную и адъювантную химиотерапию, хирургическое лечение, лучевую терапию, гормонотерапию.
Больные распределены по трем группам, в зависимости от варианта химиотерапии:
I группа (35 больных) - Навельбин 60 мг/м кв перорально 1,8 дни + Капецитабин 2000 мг/м кв перорально 1-14 дни, интервал между курсами химиотерапии - 21 день. Всего проведено 171 курс, в среднем 4,9 курсов.
II группа (31 больная) – Доцетаксел 75 мг/м кв или Паклитаксел 175 мг/м кв в/в кап + Доксорубицин 50 мг/м кв или Фарморубицин 70 мг/м кв в/в, с интервалом 21 день. Суммарно в данной группе проведено 149 курсов, в среднем – 4,8.
III группа (30 больных) - Гемцитабин 1000 мг/м кв 1,8 дни в/в + Карбоплатин AUC (Area Under the Curve) 5 или Цисплатин 60 мг/м кв, с интервалом 21 день. Общее количество курсов составило- 129, в среднем 4,3.
Особенностью работы является применение новой формы винорельбина - пероральной. Винорельбин - полусинтетический винкаалкалоид с модифицированным катарантиновым кольцом, вызывающий распад митотического веретена путем блокирования объединения микротрубочек, тем самым останавливая клеточное деление в метафазу. Механизм действия:
- блокада клеточного цикла в G2/M фазу,
- накопление в митозе,
- диссоциация митотического веретена,
- индукция апоптоза.
Навельбин выпускается в форме мягких капсул по 20 и 30 мг. Рядом клинических исследований показано, что данный препарат обладает противоопухолевой активностью, аналогичной внутривенной форме. Пероральная доза 60 мг/м кв соответствует внутривенной дозе – 30 мг/м кв.
Каждый из представленных режимов химиотерапии применялся в первой, второй и третьей линии химиотерапии. В группах I и II больные преимущественно получали первую линию химиотерапии (50,4% и 74,2% соответственно), тогда как в группе III – у большинства больных это была уже третья линия (40%).
У всех больных подтверждено метастатическое поражение печени по данным ультразвукового сканирования, морфологического исследования пунктата. У 29,2% (28) больных отмечалось изолированное метастатическое поражение печени, у 63,6% (61) - в сочетании с другими висцеральными метастазами (в легкие, плевру, кости скелета, головной мозг) и невисцеральными метастазами (мягкие ткани, лимфатические узлы) – 6,25% (6). У 76% (73) больных выявлено множественное метастатическое поражение печени, у 24% (23) – единичный метастатический очаг. У 12,5% (12) размер метастатических очагов в печени соответствовал 1-3 см, у 75% (72) - 3-5 см, у 12,5% (12) размер превышал 5 см.
Результаты исследования. Оценка эффективности лечения выполнялась в соответствии с критериями RESICT (Response Evaluation Criteria in Solid Tumors) после каждого второго курса химиотерапии. Базовый размер опухоли определялся как сумма наибольших диаметров всех измеряемых очагов. Под общей эффективностью лечения понимается сумма полного и частичного ответа, уровень контроля над заболеванием представляет собой сумму показателей полного, частичного ответа и стабилизации, при условии сохранения данного состояния не менее 3 месяцев.
В таблице 1 отражены непосредственные результаты лечения. В группе I полный ответ зафиксирован у 2,9% (1), во II – у 6,5% (2); частичный ответ в группе I – 28,6% (10), в группе II - 29,1% (9), в группе III - 23,3% (7); стабилизация 37,1% (13), 38,7% (12) и 43,3%(13); прогрессирование – 31,4% (11), 25,8% (8), 33,3% (10) соответственно.
Таблица 1. Непосредственные результаты лечения по группам.
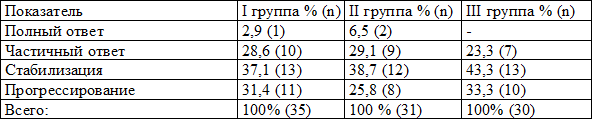
Общая эффективность лечения составила по группам 31,5%, 35,6% и 23,3%, а уровень контроля над заболеванием 68,6%, 71,3% и 66,6% соответственно.
Медиана выживаемости без прогрессирования составила в группе I – 6,8 мес., в группе II – 7,1 мес., в группе III – 4,3 мес. (различия статистически достоверны только для группы III).
При анализе зависимости результатов лечения от характера метастатического поражения печени получены следующие результаты.
Общая эффективность лечения в группе I при единичных метастазах составила 66,7% (6), группе II – 50% (3), в группе III – 37,5% (3), тогда как при множественном метастатическом поражении данный показатель составил по группам 19,2% (5), 32% (8) и 18,2% (4) соответственно (p< 0,05).
При размере метастатических очагов 1-3 см общая эффективность лечения в группе I составила – 100% (5), в группе II – 75% (3), в группе III – 66,7% (2); при размерах метастатических очагов 3-5 см – 23,1%(6), 30,4% (7), 21,8% (5) соответственно; при метастазах более 5 см в группах I и II случаев полного и частичного ответа не зафиксировано, а в группе III общая эффективность лечения составила 25% (1).
Широкий выбор цитостатиков и режимов химиотерапии позволяет эффективно проводить не только I, но и II, III и т.д. линии лечения, что значительно увеличило период до появления симптомов заболевания, приводящих к ухудшению качества жизни. Практический интерес представляют результаты лечения больных, которым раннее уже проводилась химиотерапия.
В группе I уровень контроля над заболеванием при проведении 1-й линии составил 79%, при 2-й - 56,3%, а медиана выживаемости без прогрессирования 8,5 мес. и 4,3 мес. В группе II уровень контроля над заболеванием при 1-й линии - 82,6%, 2-й линии – 50%, 3-й линии – 50%, медиана выживаемости без прогрессирования 9,2 мес., 4,6 мес. и 2,7 мес. соответственно. В группе III уровень контроля над заболеванием при проведении 1-й линии составил 77,8%, 2-й линии – 66,8%, а 3-й линии 58,3%, медиана выживаемости без прогрессирования 7,8мес., 5,1 мес. и 2,8 мес. соответственно.
Для выявления прогностических факторов ответа опухоли на цитотоксическую терапию проанализирована зависимость ответа опухоли от уровня рецепторов эстрогена и прогестерона. Общая эффективность лечения при наличии экспрессии рецепторов эстрогена и/или прогестерона в I группе составила- 31,8%(7), в группе II – 35,7% (7), в группе III – 23,8% (5). При отсутствии экспрессии рецепторов эстрогена и/или прогестерона общая эффективность лечения составила соответственно – 30,8% (4), 36,4% (4), 22,2% (2).
Значимой биологической характеристикой опухоли является уровень экспрессии Her2-neu, который определялся иммуногистохимически или FISH методикой (флюоресцентная гибридизация in situ). В исследуемой группе присутствовала гиперэкспрессия Her2-neu у 25% (24), у 20,8% (20) больных статус Her2-neu не известен. При наличии гиперэкспресии Her2-neu общая эффективность лечения в группе I составила – 30% (3), в группе II -41,6% (5), в группе III – 30% (3). Тогда как, при отсутствии гиперэкспрессии Her2-neu общая эффективность лечения составила 41,2%(7), 33,3% (4), 20% (3) соответственно. Различия статистически достоверны (p<0,05) в группе II.
В исследуемых группах до включения в исследование неоадъювантная химиотерапия проведена у 60 больных, из них у 46 присутствуют данные о степени лекарственного патоморфоза, который оценен в соответствии с классификацией Н.Н. Шиукашвили (1974 г.) [14].
Общая эффективность лечения в группе больных, у которых наблюдалась I степень лекарственного патоморфоза после проведения неоадъювантной терапии составила 23,6%, II степень - 35%, III степень - 62,5%, IV степень – 100%. Различия статистически достоверны, что позволяет предполагать о сохранении высокой чувствительности к химиопрепаратам после проведения неоадъювантной терапии.
Применение цитостатиков часто сопровождается развитием нежелательных реакций. Среди них преобладают реакции обусловленные повреждением быстро пролиферирующих тканей (костный мозг, слизистая оболочка желудочно-кишечного тракта, волосяных фолликулов и т.д.). Токсическое действие на кроветворение является наиболее частым побочным явлением химиотерапии, в основном поражается гранулоцитарный, реже тромбоцитарный и эритроцитарный росток. Для некоторых групп цитостатиков характерны специфические побочные явления, как, например кардиотоксичность антрациклинов. Кроме того, при проведении химиотерапии у больных РМЖ с метастазами в печень следует учитывать тот факт, что многие больные уже изначально имеют те или иные признаки печеночной недостаточности, что требует коррекции дозы цитостатиков и назначения дополнительной гепатотропной терапии.
Побочные явления, связанные с назначением химиотерапии разделены нами на две группы:
1. гематологические;
2. негематологическая токсичность: гастроинтестинальная (тошнота, рвота, повышение печеночных трансаминаз), кардиальная, кожная, нефротоксичность.
Гематологические осложнения представлены в таблице 2. В группе I гематологическая токсичность наблюдалась у 54,3% (19), во II группе у – 83,9% (26), в группе III – 63,3% (21) (p<0,05).
Частота развития нейтропении составила в I группе – 54,3% (19), в группе II - 83,9% (26), в группе III - 63,3% (19). Фебрильная нейтропения зафиксирована только в группе II и составила 6,5% (2). Стоит отметить тот факт, что нейтропения в целом и особенно нейтропения 3-4 степени достоверно чаще встречалась в II группе больных. У 74,2% (23) больных в группе II и только у 28,6% (10) в группе I нейтропения являлась фактором, влияющим на сроки проведения химиотерапии, и в ряде случаев требовала редукции дозы на следующих курсах.
Анемия наиболее выражена была в группе III – у 60 % (18), что является характерным токсическим явлением для цитостатиков, основанных на препаратах платины. Тромбоцитопения отмечена у 2,9% (1) больных в I группе, у 12,9% (4) в группе II и у 16,6% (5) в группе III. Для коррекции гематологической токсичности применялись гранулоцитарные колонестимулирующие факторы, эритропоэтины.
Таблица 2. Частота гематологической токсичности по группам
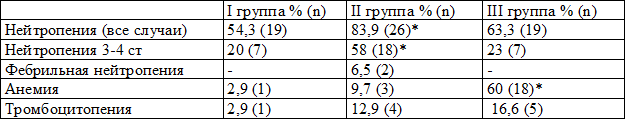
Примечание: *- p< 0,05
Гастроэнетеростинальная токсичность включала себя диарею, тошноту, рвоту, стоматит, повышение печеночных трансаминаз. В I группе данные побочные явления отмечены у 45,7% (16), в группе II – 54,9% (17), в группе III 76,7% (23).
Диарея в I группе составила 11,4 % (4), во II- 22,6% (7), в группе III отмечен только I случай диареи. Тошнота и рвота достоверно чаще встречалась в группе III и составила 76,7% (23), тогда как в группе I – 45,7% (16) и в группе II – 48,4 (15)%. Развитию стоматита были наиболее часто подвержены больные из группы II - 32,3,% (10), в группе I стоматит встречался у 8,6% (3), в группе III – у 13,3 % (4). Клинически значимое повышение уровня печеночных трансаминаз (более 2,5 верхней границы норма) отмечено у 8,6% (3) больных в группе I, у 16,1% (5) в группе II и у 10% (3) больных в группе III.
Из других побочных явлений следует отметить следующие, характерные для определенных групп цитостатиков:
- Ладонно-подошвенный синдром, проявляющийся гиперемией, десквамацией кожи ладоней, является характерным побочным явлением для навельбина и встречался у 17,1% (6) больных в группе I. В большинстве случаев, данный синдром не превышал 1-2 степени и не влиял на сроки проведения химиотерапии и не требовал коррекции дозы.
- Аллопеция – побочное действие, характерное для большинства цитостатиков и существенно влияющее на качество жизни больных. Тотальная аллопеция отмечалась у 14,3% (5) больных в группе I, у 54,9% (17) больных в группе II и у 23% (7) в группе III.
- Кардиотоксичность – является наиболее часто выраженным побочным явлением для цитостатиков из группы антрациклинов. Частота кардиотоксических реакций в группе II составила 51,6% (16).
- Нефротоксичность отмечалась в группе III у 16,7% (5) больных, у всех больных применялся цисплатин.
- Гипертермия – повышение температуры тела до 37,5-38,0ºС, наблюдалась после введения гемцитабина у 20% (6) больных в группе III.
Анализируя токсические реакции, наблюдающиеся при проведении данного исследования, следует отметить, что наиболее благоприятный профиль токсичности имеет комбинация навельбина и кселоды. Тогда как для комбинации таксанов и антрациклинов характерны более выраженные гематологические реакции, кардиотоксичность, для комбинации препаратов платины и гемцитабина – нефротоксичность, что ограничивает применение данных схем у пожилых или соматически отягощенных больных.
Выводы
1. Общая эффективность лечения при комбинированном применении пероральной формы навельбина и кселоды составила 31,5%, при использовании препаратов таксанового ряда и антрациклинов - 35,6%, гемзара и препаратов платины - 23,3%, а медиана выживаемости без прогрессирования - 6,8 мес., 7,1 мес., и 4,3 мес. соответственно (р<0,05).
2. У больных РМЖ с метастазами в печень проводимая лекарственная терапия наиболее эффективна при единичном метастатическом поражении и очагах, размер которых не превышает 3 см.
3. Частота развития гематологических осложнений при применении пероральной формы навельбина и кселоды составила 54,3%, при использовании комбинациями препаратов таксанового ряда и антрациклинов – 83,9%, гемзара и препаратов платины - 63,3% (р<0,05), а гастроинтестинальные побочные явления встречались у 45,7%, 54,9% и 76,7% больных соответственно.
В настоящее время стратегия терапии метастатического РМЖ основана на применением лекарственных препаратов, характеризующихся максимальной эффективностью при минимальной токсичности и одним из таких примеров является комбинация пероральной формы навельбина и кселоды.
