Актуальность. Храп и синдром обструктивного апноэ сна (СОАС) являются актуальной медицинско-социальной проблемой. Храпом страдают около 20% людей в возрасте старше 30 лет. СОАС по данным различных источников, встречается от 6% в общей популяции взрослых от 30 лет, до 67-75% взрослых старше 75 лет [1,2]. Храп возникает за счет вибрации мягких тканей глотки при ее неполной обструкции во время сна и представляет собой неприятный звуковой феномен. СОАС происходит при полной обструкции верхних дыхательных путей на уровне глотки, приводящей к полному прекращению легочной вентиляции на протяжении 10 секунд и более, и как следствие, к микропробуждениям и фрагментации сна [2]. Основными симптомами СОАС являются храп, «неосвежающий» сон, повышенная дневная сонливость. Наличие тяжелой формы СОАС сопряжено с высоким риском развитием сердечно-сосудистых, метаболических, эндокринных и неврологических нарушений. Одной из главных причин храпа и СОАС являются особенности строения верхних дыхательных путей (ВДП), такие как гипертрофия мягкого нёба, увеличение нёбных, глоточной и язычной миндалин, назальная обструкция, размер и положение языка, особенности зубочелюстной системы. Другим значимым фактором в развитии СОАС служит избыточный вес и ожирение (индекс массы тела [ИМТ] >29,9 кг/м2). Негативное влияние оказывают употребление алкоголя, прием снотворных и наркотических препаратов, а также курение [1, 2,6]. Разделяют 3 степени тяжести СОАС: легкая (индекс апноэ/гипопноэ (ИАГ) 5-15), средняя (ИАГ 15-30) и тяжелая (ИАГ >30). Наличие храпа при ИАГ<5 эпизодов в час, принято считать простым (неосложненным) храпом. «Золотым стандартом» диагностики СОАС является полисомнография (ПСГ). ПСГ позволяет оценить ИАГ во сне, проанализировать структуру сна, а также провести дифференциальную диагностику между СОАС и другими формами нарушения сна. В настоящее время для диагностики СОАС широко применяются упрощенные полисомнографические системы, такие как респираторные и кардио-респираторные системы (РС и КРС) позволяющие установить диагноз, оценить количество и качество дыхательных расстройств во сне, без анализа структуры сна [3]. Обследование пациентов с храпом и СОАС включает в себя инструментальный осмотр ВДП, эндоскопическое исследование, при необходимости дополненное функциональными пробами или проведенное в условиях медикаментозно-индуцированного сна (слипэндоскопия) [4].
Методы лечения пациентов с храпом и СОАС можно разделить на консервативные и хирургические. Важную роль играют общепрофилактические мероприятия: снижение массы тела, положение тела на боку во время сна, тренировка мышц нёба, отказ от вредных привычек. В ряде исследований было показано, что уменьшение массы тела пациента на 10% от исходной, может улучшить параметры дыхания во сне на 50% [5]. При патологии зубочелюстной системы в сочетании c первичным храпом и СОАС легкой степени используются внутриротовые фиксирующие устройства (аппликаторы, капы), выдвигающие нижнюю челюсть и язык вперед [2,6]. Наиболее эффективным способом устранения ночного апноэ является СРАР-терапия (от англ. Continuous Positive Airway Pressure) - ночная неинвазивная вентиляция легких с постоянным положительным давлением. Этот вид лечения показан больным с тяжелой степенью СОАС. Во время сна СРАР-аппарат создает в ВДП избыточное положительное давление, которое препятствует их коллапсу и устраняет основной механизм заболевания. Несмотря на высокую эффективность, СРАР-терапия имеет ряд существенных недостатков: неопределенная длительность лечения (СОАС может возникнуть через короткий временной промежуток после отказа от СРАР), физический и психологический дискомфорт, а также существенные экономические затраты [7].
Цель хирургического метода лечение заключается в устранении всех причин обструкции ВДП. В 1952 г. в Японии была впервые проведена операция по уменьшению мягкого нёба для устранения храпа. В последующем это направление хирургии пользовалось большой популярность, однако было отмечено, что эффект от проведения подобных операций не был стойкий. Удаление больших объемов ткани из глотки приводило к развитию таких осложнений как рубцовый стеноз глотки, рото-носовой рефлюкс, парез мягкого нёба, при сохраняющемся СОАС [8]. В настоящее время разрабатываются новые малоинвазивные способы реконструктивных хирургических вмешательств на мягком нёбе. При выраженной гипертрофии глоточной, нёбных и язычной миндалин в сочетании со всеми формами СОАС показана их полная или частичная резекция. Восстановление носового дыхания (септопластика, коррекция носовых раковин) является важным этапом лечения пациентов с апноэ сна, однако чаще не позволяет добиться полного устранения СОАС [9]. При обструкции ВДП на уровне корня языка проводятся редукция язычной миндалины, глоссэктомия, подвязывание корня языка, операция на подбородочно-подъязычной мышце с выдвижением языка вперед. По жизненным показаниям при тяжелой форме СОАС и отсутствии альтернативных способов надежного восстановления дыхательной функции может быть выполнена трахеостомия [10].
Материалы и методы. В исследование были включены 77 пациентов с храпом и СОАС, прошедших хирургическое лечение в отделении оториноларингологии Университетской клиники «Кусково» Московского государственного медико-стоматологического университета им. А.И. Евдокимова с 2017 по 2019 годы. Среди них 57 (74%) мужчин и 20 (26%) женщин. Возраст пациентов варьировался в диапазоне от 18 до 66 лет (средний возраст составил 41,7±10,71 лет).
Критериями включения в исследование были наличие у пациентов храпа и/или апноэ во сне (подтвержденные результатом объективного исследования), в сочетании с выявленными причинами обструкции ВДП.
Критерии исключения:
1) беременность, лактация; 2) тяжелое сопутствующее соматическое заболевание (нарушение функции щитовидной железы, почечная и печеночная недостаточность, тяжелое заболевание сердечно-сосудистой системы, онкологическое заболевание); 3) психическое заболевание в анамнезе или обнаруженное при клиническом обследовании; 4) наркотическая и алкогольная зависимость; 5) отказ пациента от проведения предложенной схемы лечения; 6) пациенты с СОАС без значимых изменений ВДП.
Для сбора жалоб и анамнеза использовались стандартизированный опросник Berlin Questionnaire© Sleep Apnea и шкала дневной сонливости Эпворта. В опроснике Berlin Questionnaire© пациенты самостоятельно указывали данные о своем росте и массе тела и отвечали на 3 категории вопросов, касающихся основных симптомов СОАС: выраженности и частоты храпа, остановок дыхания во сне, усталости, а также наличия артериальной гипертензии. Риск СОАС считается высоким, если положительные 2 категории и более. При оценке выраженности дневной сонливости по шкале сонливости Эпворта применялась следующая интерпретация результатов: 0-8 баллов - норма, 9-12 баллов - легкая сонливость, 13-16 баллов - средняя, более 16 баллов – тяжелая [11].
Для оценки состояния ВДП проводился рутинный инструментальный оториноларингологический осмотр: передняя и задняя риноскопия, мезофарингоскопия, непрямая ларингоскопия. Дополнительно проводилось эндоскопическое исследование ВДП при помощи жесткого эндоскопа KARL STORZ с оптикой 0° и 30°, для уточнения уровня и формы обструкции эндоскопический осмотр проводился в состоянии медикаментозно-индуцированного сна (слипэндоскопия). Оценивались состояние слизистой полости и носа, искривление носовой перегородки (ИПН), размеры носовых раковин, состояние структур лимфоидно-глоточного кольца, высота стояния небной занавески, размеры нёбного язычка и нёбных дужек, положение языка по Фридману.
Расширенный респираторный мониторинг проводился при помощи системы ApneaLink (Австрия). Данная система позволяет непрерывно регистрировать во время сна динамику сатурации (SpO2), назального потока воздуха, движений грудной клетки, частоты сердечных сокращений и храпа (выделенного из воздушного потока в виде отдельных колебаний). Данная система соответствует мировым стандартам и требованиям Американской академии медицины сна (AASM). Респираторный мониторинг проводился всем пациентам амбулаторно до проведения хирургического вмешательства. По результатам РМ пациенты были разделены на группы в зависимости от исходной степени тяжести СОАС (неосложненный храп (ИАГ<5/час), СОАС легкой, средней, тяжелой степени).
Хирургическое лечение было направлено на устранение всех выявленных причин обструкции ВДП. По показаниям проводилась коррекция структур полости носа (коррекция носового клапана, септопластика, редукция носовых раковин, задняя конхотомия), аденотомия, тонзиллэктомия. Реконструктивные операции на мягком небе (увулотомия, увулопалатопластика в сочетании с субмукозной радиочастотной абляцией мягкого нёба) осуществлялись с использованием радиоволнового аппарата Surgitron (США). Использовались параметры работы: высокочастотная (3,8-4,0 МГц) радиоволна, режим разреза «CUT/COAG» (разрез/коагуляция), игольчатый электрод. Показаниями для проведения данного типа операций были наличие обструкции на уровне мягкого нёба и переднезадняя форма обструкции.
Результаты лечения оценивались повторным анкетированием и данными респираторного мониторинга через 1 месяц после операции.
В качестве критериев оценки эффективности хирургического лечения использовались следующие параметры:
- Уровень храпа (полное устранение, уменьшение интенсивности, сохраняется, усилился).
- Качество сна (ночные пробуждения в связи с апноэ, дневная сонливость).
- ИАГ по результатам контрольного респираторного мониторинга (положительным результатом считалось снижение ИАГ на 50% от исходного уровня).
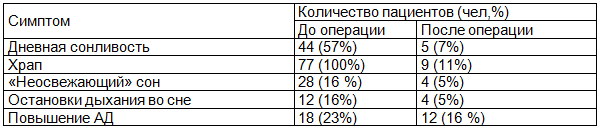
Результаты исследования. По результатам первичного анкетирования 77 (100%) больных отметили наличие храпа, 12 (16%) эпизоды апноэ. Повышенная дневная сонливость по Шкале Эпворта была выявлена у 44 (57%) пациентов. При изучении антропометрических данных было установлено, что у 31 (40%) больных имелась избыточная масса тела или ожирение, из них почти у половины больных тяжелая форма СОАС - 16 (21%). По данным объективного исследования сна неосложненный храп (ИАГ <5) был выявлен у 24 (31%) человек, СОАС легкой степени – 22 (29%), средней степени – у 12 (16%), СОАС тяжелой степени – у 19 (25%). Таким образом, из 77 пациентов с храпом у 53 (69%) больных выявлены эпизоды апноэ сна, что говорит о том, что субъективная оценка пациентом тяжести заболевания может быть занижена – 39 (53%) больных СОАС не знали о наличие у себя апноэ.
В зависимости от уровня локализации патологического процесса все пациенты были разделены на 3 группы: 1) полость носа, околоносовые пазухи, носоглотка; 2) ротоглотка, мягкое небо; 3) несколько уровней обструкции. Нозологические формы выявленных патологических изменений ВДП представлены в табл. 1. В большей части наблюдений имелось сочетание нескольких уровней обструкции – 38 (49%), из них искривление носовой перегородки и увеличение нижних носовых раковинам в сочетании с гипертрофией мягкого нёба встречалось чаще других - 20 (26%). Среди причин локализованных только на уровне ротоглотки преобладала гипертрофия мягкого неба - 18 (23%). Изолированно только на уровне полости носа – искривление носовой перегородки и гипертрофия нижних носовых раковин - 7 (9%) (p <0,05).
Таблица 1. Причины обструкции верхних дыхательных путей
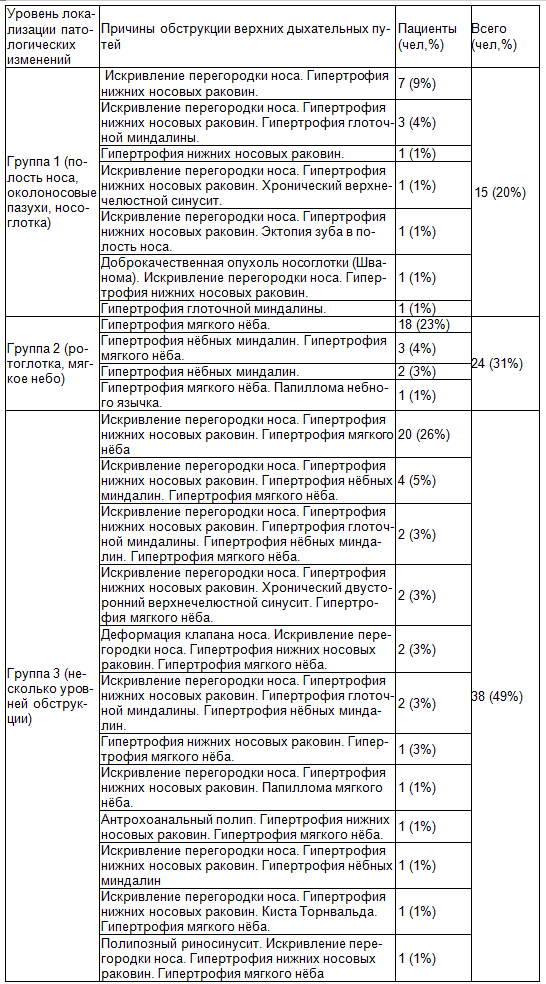
У пациентов с внутриносовой патологией чаще был диагностирован неосложненный храп или СОАС легкой степени. В группах с орофарингеальной и сочетанной патологией пациенты с разными степенями тяжести СОАС встречались более равномерно. Пациенты с тяжелой степенью СОАС в большинстве случаев имели несколько причин для обструкции, так из 19 пациентов имеющих тяжелую степень СОАС, у 11 (58%) требовалось комбинированное хирургическое вмешательство на нескольких уровнях (p <0,05) (таблица 2).
Таблица 2. Соотношение уровня локализации патологического процесса и тяжести СОАС
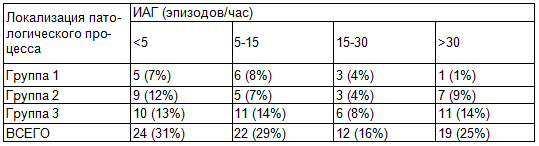
Под местной анестезией было проведено 25 (33%) операций, под общей анестезий (комбинированный эндотрахеальный наркоз) – 52 (67%). Увулопалатопластика была выполнена 52 (67 %) пациентам, из них в 18 (23%) наблюдений она проводилась как единственная операция, в 34 (44%) случаях – в комбинации с другими операциями. Объем увулопалатопластики чаще заключался в клиновидной резекции верхней медиальной порции задних нёбных дужек, иссечении нижней 1/3 сформировавшегося после удаления дужек небного язычка и субмукозной радиочастотной абляции свободного края мягкого нёба (рисунок 1). Наложение швов на послеоперационную рану при данной методике не требовалось. Послеоперационный болевой синдром продолжался в среднем 10 дней (от 7 до 14 дней), максимальная его интенсивность наступала на 5-6 день (7-9 баллов по ВАШ).
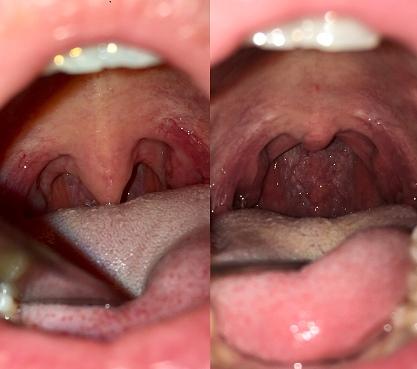
Рис. 1. Предоперационный осмотр глотки пациентки Т., 25 лет с неосложненным храпом (ИАГ-3/час) с гипертрофией мягкого нёба (фото слева). Через 1 месяц после операции (фото справа) отмечает полное устранение храпа, подтвержденное результатами респираторного мониторинга.
Как единственный способ лечения увулопалатопластика применялась в 7 (9%) наблюдениях при неосложненном храпе, а также при СОАС легкой степени у 5 (7%) пациентов. У этих больных операция проводилась под местным инфильтративным обезболиванием 2% раствором Лидокаина введенного в основание нёбного язычка и по ходу задних небных дужек. У пациентов с тяжелой степенью СОАС реконструкция мягкого нёба выполнялась как один из этапов операции: у 7 (9%) больных в сочетании с коррекцией внутриносовых структур, в 2 (3%) случаях - с двусторонней тонзиллэктомией (рисунок 2).
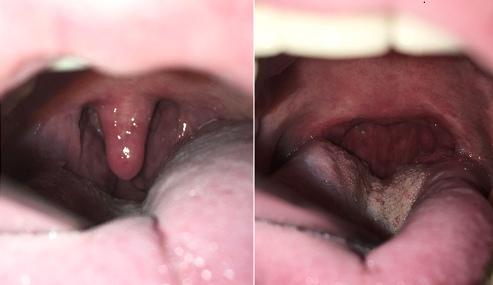
Рис. 2. Предоперационный осмотр глотки пациента К., 43 лет с СОАС тяжелой степени (ИАГ-60/час), имеющего гипертрофию небных миндалин и мягкого нёба (фото слева), в сочетании с назальной обструкцией. Через 1 месяц после хирургического лечения (фото справа) отмечает существенное уменьшение храпа и дневной сонливости, объективно отмечается снижение ИАГ до 12/час.
В послеоперационном периоде всем пациентам проводилась антибактериальная, комплексная противовоспалительная, местная терапия. В 1(1%) наблюдении после увулопалатопластики в раннем послеоперационном периоде наблюдалась нарушение разделительной функции мягкого нёба на фоне выраженного отёка тканей в области операции, полностью разрешившееся на 5 сутки после операции. В 1(1%) наблюдении после увулопалатопластики с тонзилэктомией развилось кровотечение из нижнего полюса тонзиллярной ниши, остановленное электрокоагуляцией кровоточащего сосуда. В отдаленном послеоперационном периоде во всех наблюдениях осложнений не выявлено.
Оценивая результаты лечения, полное устранение храпа или существенного уменьшение его интенсивности отметили 68 (88%) пациентов, храп остался на прежнем уровне у 7 (9%) пациентов. В 2 (3%) наблюдениях отмечено усиление храпа (в обоих случаях пациенты с неосложненным храпом, которым проводилась только внутриносовая хирургия) (p <0,05). Динамика изменения основных симптомов представлена в таблице 3.
Таблица 3. Оценка изменения основных симптомов через 1 месяц после хирургического лечения по результатам стандартизированных опросников
Результаты объективного исследования представлены в таблице 4. Через 1 месяц после операции нормальное значение ИАГ было выявлено у 51 (66%) человек, у 22 (29%) пациентов ИАГ снизился на 50% и более со средней и тяжелой степеней до более легких. У пациентов с неосложненным храпом увеличения ИАГ не отмечалось - 24 (31%). В группах с легкой и средней степенью СОАС у 27 (35%) пациентов ИАГ стал меньше 5. У пациентов с изначально тяжелой формой СОАС в 13(16%) наблюдениях отмечено снижение ИАГ на 50 %, еще в 4 (5%) случаях ИАГ существенно не снизился. Среди пациентов с неудовлетворительным результатом хирургического лечения у всех имелось ожирение, в дальнейшем им было рекомендовано проведение CPAP- терапии. Все полученные данные статистически достоверны (p <0,05).
Таблица 4. Изменение показателей дыхательных нарушений во сне после хирургического лечения (p <0,05)

Выводы:
- Обследование пациентов с жалобами на храп и апноэ сна обязательно должно включать исследование параметров дыхания во сне с целью установки правильного диагноза, адекватной оценки степени тяжести заболевания и выбора оптимального метода лечения.
- Хирургическое лечение является эффективным у пациентов с неосложненным храпом и СОАС легкой и средней степени тяжести, а для пациентов с тяжелой формой СОАС хирургическое вмешательство может быть одним из этапов лечения.
- Контрольное обследование после операции с применением предложенного алгоритма позволяет оценить результаты лечения и скорректировать дальнейшую тактику лечения.
