В последние годы особый интерес вызывает синдром абдоминальной компрессии (САК) или Abdominal Compartment Syndrome или синдром интраабдоминальной гипертензии (СИАГ), который представляет собой симптомокомплекс, развивающийся вследствие повышения давления в брюшной полости и характеризующийся развитием полиорганной недостаточности [1 – 3]. Наиболее важной причиной внутрибрюшной гипертензии являются перитонит [4, 5], деструктивный панкреатит [6].
При перитоните, панкреонекрозе и тяжелой сочетанной травме внутрибрюшная гипертензия развивается у 30 и более процентов больных, а СИАГ возникает приблизительно у 5,5-8,3% пациентов [12, 2, 7, 8]. Ввиду того, что внутрибрюшная гипертензия ведет к развитию полиорганной недостаточности и возникает на фоне уже имеющихся тяжелых повреждений, летальность от СИАГ достигает очень высоких цифр – 42-68% [2, 9, 10], без лечения этот показатель приближается к 100% [2, 11].
Большинство авторов в настоящее время определяют четыре степени синдрома абдоминальной компрессии: I степень 10 - 15 мм рт. ст.; II степень 15 - 25 мм рт. ст.; III степень 25 - 35 мм рт. ст.; IV степень > 35мм рт. ст. [1, 12 – 15].
Самым популярным и наиболее простым в исполнении остаётся способ оценки давления в брюшной полости по уровню давления в мочевом пузыре. Метод прост, не требует специальной, сложной аппаратуры, позволяет осуществлять мониторинг за данным показателем на протяжении длительного срока лечения больного [8, 16 - 19]. Измерение давления в мочевом пузыре считают «золотым стандартом» для мониторинга ВБД [8, 13, 17, 20], однако оно неприменимо у пациентов с переломом костей таза, паравезикальными гематомами и травмой мочевого пузыря, с наличием в брюшной полости злокачественной или доброкачественной опухоли, соприкасающейся со стенкой пузыря [12, 13, 21].
Цель работы – разработать комплекс регистрации биофизических параметров брюшной полости, обеспечивающий возможность синхронного контроля и коррекции внутрибрюшного давления и силы натяжения паравульнарных тканей в интра- и послеоперационном периоде; изучить в эксперименте на животных влияние различной степени интраабдоминальной гипертензии на микроциркуляцию в стенке тонкой кишки.
Материалы и методы. В эксперименте на 42 беспородных собаках массой 15,4 ± 0,8 кг изучено состояние микроциркуляции в стенке тонкой кишки и натяжение паравульнарных тканей в зависимости от уровня внутрибрюшного давления (ВБД) (7, 15, 25 и 35 мм рт. ст.). Для решения поставленных задач животные были разделены на 4 группы.
Измерение ВБД в эксперименте проводилось одновременно методом открытого уретрального катетера по Harrahill M. (1998) [18] и с помощью комплекса регистрации биофизических параметров брюшной полости, разработанного совместно с сотрудниками Нижегородского государственного технического университета. Комплекс состоит из новой конструкции спицевого абдоминального раневого контрактора (СпАРК) с встроенным в браншу тензометрическим датчиком и электронной системы синхронного контроля двух биофизических параметров (ВБД и натяжение паравульнарных тканей).
Усовершенствованная конструкция СпАРК состоит из зубчатой рейки и реечно-винтового механизма 1, которые соединены с неподвижной 2 и подвижной 3 браншами. На браншах контрактора закреплены две насадки 4, 5. Насадка 5 установлена на подвижной бранше и служит для крепления тензометрических датчиков, преобразующих механические деформации в электрические сигналы, которые передаются по проводу 6 в контроллер 7 и затем через порт 9 на ЭВМ (рис. 1).
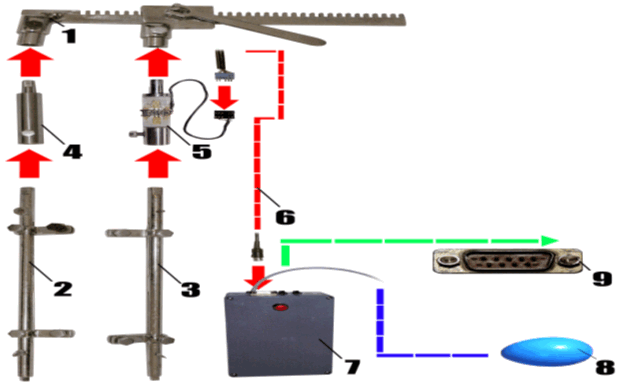
Рис. 1. Общая схема разработанного комплекса регистрации биофизических параметров брюшной полости.
Устройство, предназначенное для прямого измерения ВБД, состоит из терминального отдела 8 датчика давления, представляющего собой эластичный резиновый баллон объёмом 30 см3, заполненный воздухом, который через полихлорвиниловую трубку герметично соединён с контроллером 7 системы синхронной регистрации внутриполостного давления и усилия.
Животным выполняли нижнесрединную лапаротомию, троакарную цистостомию. Силиконовую трубку, помещённую в мочевой пузырь выводили наружу через отдельный прокол брюшной стенки в левой подвздошной области. Выведенный конец трубки крепили к вертикально установленной линейке. Нулевую отметку линейки устанавливали на уровне лобкового симфиза. В систему вводили 20 мл фурациллина, что моделировало измерение ВБД методом открытого катетера.
В брюшную полость помещали баллон из перчаточной резины и терминальный отдел 8 датчика давления. Накладывали СпАРК II, соединённый с электронной системой контроля. Сначала фиксировали биофизические параметры брюшной полости при полностью разведённых краях лапаротомной раны и определяли базальную перфузию. Потом края раны сводили и шприцем Жанэ нагнетали воздух в находившийся в брюшной полости баллон для повышения ВБД до 7; 15; 25 и 35 мм рт. ст. в различных экспериментальных группах и выдерживали экспозицию в течение 1 часа. Затем фиксировали показатели состояния паравульнарных тканей и органов брюшной полости: снимали показания с монитора электронной системы контроля ВБД и натяжения паравульнарных тканей. Лапаротомную рану после предварительного сближения краев раневого дефекта с помощью СпАРК II послойно ушивали капроновой нитью.
Состояние микроциркуляторного русла кишечной стенки оценивали с помощью неинвазивного метода исследования колебаний микрокровотока - лазерной доплеровской флоуметрии (ЛДФ). Перфузию стенки петли тонкой кишки, прилежащей к лапаротомной ране, определяли с помощью ЛАКК-01 (НПП «Лазма», Россия).
Для обработки данных использовали пакет программного обеспечения LDF 2.0.0.419, который позволил характеризовать состояние системы микроциркуляции по следующим показателям: показатель микроциркуляции (ПМ), среднее квадратичное отклонение (СКО), амплитуды медленных (ALF), быстрых (AHF) и пульсовых (АСF) колебаний. Перечисленные показатели измеряли в перфузионных единицах (пф. ед.). Также определяли нормативные показатели ритмических составляющих колебаний кровотока: коэффициент вариации (Kv), микрососудистый тонус (ALF/СКО), миогенную активность прекапиллярных вазомоторов (ALF/Mx100%), респираторные (AHF/CKOx100%) и пульсовые флуктуации кровотока (ACF/CKOx100%).
Результаты исследования. В результате экспериментального исследования установлено, что медиана базальной перфузии (при ВБД равном атмосферному) в микроциркуляторном русле тонкой кишки колебалась от 39,1 до 44,1 пф. ед. в различных экспериментальных группах.
Параметры кровотока по данным ЛДФ при повышении ВБД до 7 мм рт. ст. статистически значимо не отличались от значений при измерении показателей на базовом уровне ВБД, равном атмосферному.
Изучение показателей средних величин перфузии тканей кровью у животных 2-й экспериментальной группы (ВБД=15 мм рт. ст., n=10) показало, что значение ПМ, характеризующее средний поток эритроцитов в зондируемом участке ткани при первой степени интраабдоминальной гипертензии, статистически значимо снизилось (p=0,021) по сравнению с 1-й экспериментальной группой (ВБД=7 мм рт. ст., n=12) на 23,3 пф. ед. (табл. 1).
Таблица 1. Динамика показателей микроциркуляции в экспериментальных группах животных в зависимости от уровня ВБД (Ме [Q1; Q3])
![Таблица 1. Динамика показателей микроциркуляции в экспериментальных группах животных в зависимости от уровня ВБД (Ме [Q1; Q3])](/images/articles/2012/2.2/12153/t1.png)
Примечания: р – уровень статистической значимости различий между показателями 2-й и 1-й групп; р1 – уровень статистической значимости различий между показателями 3-й и 2-й групп; р2 – уровень статистической значимости различий между показателями 4-й и 3-й групп.
При повышении ВБД до 15 мм рт. ст. происходило снижение показателя СКО, характеризующего временную изменчивость кровотока, на 64,9% (p=0,05). При этом коэффициент вариации (Kv) в этой группе по сравнению с Kv при базальной перфузии увеличился в 1,5 раза (p=0,045).
Анализ амплитуд ритмических составляющих микрокровотока показал, что изменения показателей перфузии происходило на фоне увеличения миогенной активности прекапиллярных вазомоторов (ALF/ПM x 100%) на 67% и пассивных факторов модуляции кровотока (AHF/CKO x 100% и ACF/CKO x 100% на 83,5% и 77%, соответственно) по сравнению с 1-й группой животных. Однако изменения респираторно-пульсовых флуктуаций кровотока были значительно более выраженными.
Микрососудистый тонус (ALF/CKO x 100%) во 2-й группе животных увеличивался по сравнению со значениями, полученными в 1-й группе, на 66,5% (p=0,041). Также при первой степени интраабдоминальной гипертензии происходило увеличение миогенной активности прекапиллярных вазомоторов (ALF/ПM x 100%) в 2,9 раза (p=0,027). Пассивные механизмы модуляции кровотока в системе микроциркуляции при данных условиях изменялись сонаправленно, но в разной степени. Респираторные флуктуации кровотока увеличивались в большей степени в сравнении с пульсовыми (в 6,0 и 4,3 раза, соответственно) относительно показателей 1-й группы. Индекс эффективности микроциркуляции (ИЭМ) в стенке кишки в данных условиях значимо снизился с 1,4 при 7 мм рт. ст. до 0,8 при первой степени интраабдоминальной гипертензии (p=0,043).
Повышение ВБД до 25 мм рт. ст. в 3-й экспериментальной группе сопровождалось изменениями параметров кровотока, динамика которых была сонаправлена с динамикой изменений во второй группе. При этом значимых отличий между показателями ПМ, СКО и активности прекапиллярных вазомоторов во 2-й и 3-й группах животных отмечено не было (p=0,345, p=0,092 и p=0,251 соответственно), а микрососудистый тонус уменьшался статистически значимо (p=0,037). Показатели пассивных механизмов модуляции кровотока при второй степени ИАГ были ниже, чем при ВБД, равном 15 мм. рт. ст.
В 4-й группе животных на фоне абдоминальной компрессии 35 мм рт. ст. по сравнению с 3-й группой отмечено статистически значимое снижение показателя микроциркуляции ПМ с 12,5 до 5,1 пф. ед. (p=0,032). Коэффициент вариации (Kv) и индекс эффективности микроциркуляции (ИЭМ) значимо не изменились. Показатели пассивных факторов контроля микроциркуляции также снизились: AHF/CKO x 100% на 7% (p=0,110), а ACF/CKO x 100% на 48,2% (p=0,248). При этом миогенная активность прекапиллярных вазомоторов уменьшилась незначительно на 12,2% (p=0,632).
В эксперименте выявлена корреляционная связь между измерением ВБД методом открытого уретрального катетера и предложенным комплексом регистрации биофизических параметров брюшной полости. Значение коэффициента корреляции R Спирмена между ВБД и давлением в мочевом пузыре составило R=0,838, р=0,002, что свидетельствовало о равной информативности контроля ВБД как через мочевой пузырь, так и посредством разработанного комплекса регистрации ВБД (рис. 2).
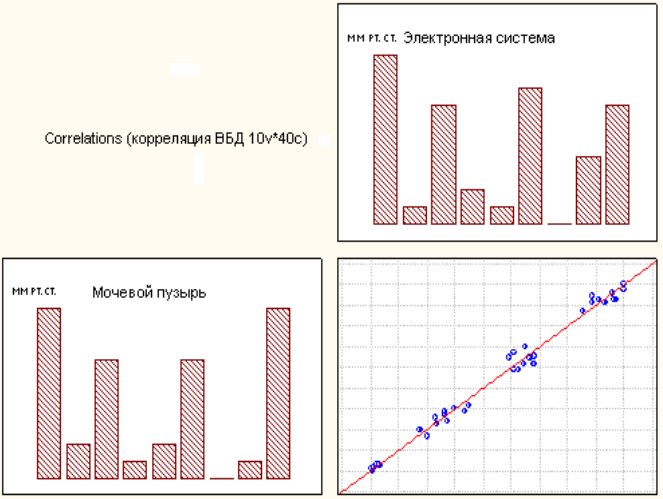
Рис. 2. График рассеяния переменных при определении ВБД методом открытого катетера и посредством электронной системы.
Проведенные исследования позволили сделать вывод, что при закрытой операционной ране и поэтапном повышении ВБД натяжение паравульнарных тканей возрастает в экспоненциальной зависимости. При этом существует корреляционная связь между изменением ВБД и натяжением краев раны (R=0,977, р < 0,001). При ВБД 15 мм рт. ст. сила натяжения паравульнарных тканей в среднем составила 12 ± 0,6 Н (рис. 3).
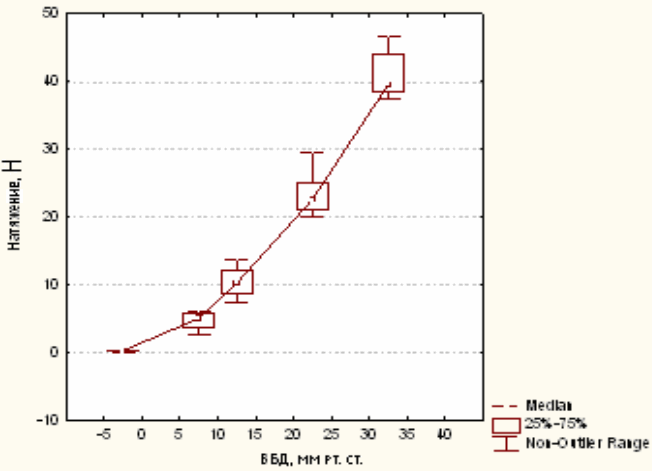
Рис. 3. Изменение натяжения паравульнарных тканей в зависимости от уровня ВБД в эксперименте.
Таким образом, проведенные экспериментальные исследования показали, что уже при уровне ВБД 15 мм рт. ст. наступает значимое ухудшение перфузии в тонкой кищке в виде снижения показателей микроциркуляции и индекса эффективности микроциркуляции, застоя в венулярном сегменте циркуляторного русла по сравнению с уровнем ВБД 7 мм рт. ст. Учитывая отсутствие значимых отличий показателей регионарной перфузии при дальнейшем повышении ВБД до 25 мм рт. ст. и развивающиеся в микроциркуляторном русле при 35 мм рт. ст. признаки прогрессирующей сердечно-сосудистой и дыхательной недостаточности можно считать, что первая степень ИАГ (15 мм рт. ст.) является критическим уровнем ВБД.
