Введение. Синдром раздражённого кишечника (СРК) относится к функциональным заболеваниям органов пищеварения. Распространенность СРК в большинстве стран мира в среднем составляет 20%, варьируя, по данным различных исследований от 9 до 48% [1]. По данным Всемирной Гастроэнтерологической Организации [11] распространённость СРК в Европе и Северной Америке достигает 10-15% от общей популяции. В некоторых странах посчитаны абсолютные цифры количества больных СРК, так, например, в Германии это число превышает 12,5 млн. и только лишь около 2 млн. человек получают лечение [7]. Подобные пациенты составляют до 12% всех больных врача общей практики и до 28% среди обращающихся за специализированной помощью к гастроэнтерологу, занимая 50% рабочего времени врачей данной специальности [1]. Ежегодные расходы, связанные с обследованием и лечением данной категории больных в США, достигают 25 млрд. долларов, а число обращений составляет приблизительно 3 млн., общее число дней нетрудоспособности вследствие СРК сопоставимо с таковыми при острой респираторной вирусной инфекции (ОРВИ) [7]. Так как пик заболеваемости приходится на молодой трудоспособный возраст – 30–40 лет [7,11,12], то широкое распространение СРК наносит большой экономический ущерб обществу как по прямым показателям затрат на медицинское обслуживание и лечение, так и по непрямым показателям, включающим компенсацию временной нетрудоспособности [6,9]. Следует заметить, что в России сведения о частоте СРК не до конца изучены. Считается, что за врачебной помощью обращается не более 10% больных и большинству из них ставят другие диагнозы [1,3].
Согласно современным представлениям СРК является биопсихосоциальным функциональным кишечным расстройством, в основе которого лежит взаимодействие трёх основных патогенетических механизмов: психосоциального воздействия, сенсомоторной дисфункции, проявляющейся нарушением висцеральной чувствительности и двигательной активности, и стойких нейроиммунных повреждений, которые развиваются после перенесённых инфекционных заболеваний кишечника [1,4,10,11].
Для отличия СРК от другой кишечной патологии эксперты Всемирной Гастроэнтерологической Организации в апреле 2009 г. предложили использовать диагностические Римские критерии III. Они включают в себя: 1) появление симптомов, по меньшей мере, за 6 месяцев до установления диагноза; 2) наличие рецидивирующей абдоминальной боли или дискомфорта >3 дней в месяц в течение прошлых 3 месяцев; 3) присутствие минимум 2-х из 3-х представленных симптомов: уменьшение болей после дефекации, связь симптоматики с изменением частоты стула и с изменением в характере стула [11]. Абдоминальная боль является обязательным компонентом клинической картины СРК. Она имеет широкий спектр интенсивности от легкого дискомфорта, терпимой ноющей боли до интенсивной, постоянной, схваткообразной [1]. Как правило, боль локализуется внизу живота, чаще в левой подвздошной области, но может отмечаться практически в любом отделе вплоть до эпигастрия. На фоне появления боли отмечаются вздутие живота, метеоризм, усиление перистальтики кишечника, диарея или урежение стула. Боли стихают, как правило, после дефекации и отхождения газов и не беспокоят по ночам. Согласно Римским критериям, принятым для включения больных в протоколы научных исследований, патологической считается частота стула более 3 раз в день (диарея) и менее 3 раз в неделю (запоры). Наряду с изменениями частоты стула у больных с СРК наблюдается изменение формы и консистенции кала [1,2,6,10]
Патогенетические модели развития СРК на протяжении многих лет претерпевали изменения. Ещё в 1998 году были опубликованы результаты двух крупных исследований, использующих идентичные методы оценки психологического статуса (Минесотская многофазная индивидуальная шкала – Minnesota Multiphasic Personality Inventory - MMPI), которые пришли к различным заключениям. В одном из этих исследований поведение пациентов с СРК не отличалось от такового у пациентов с органической патологией [14], тогда как число СРК-пациентов с нервно-психическими отклонениями по результатам MMPI в другом наблюдении было значительно выше, чем в контрольной группе [13].
На рабочем совещании по СРК, которое проходило в рамках Всемирного конгресса гастроэнтерологов (Вена, 1998), председатель Рабочего комитета по функциональным расстройствам желудочно-кишечного тракта профессор D.A. Drossman (США)- доктор психиатрии, определил СРК как психосоматическое заболевание, в основе которого лежит расстройство нервной регуляции моторики тонкой и толстой кишки [13]. В медицинской литературе можно встретить изречение известного гастроэнтеролога середины ХХ века О.Л. Гордона о пациентах с синдромом раздражённого кишечника: «У этих больных «голова всегда в кишках», то есть их мозг постоянно занят анализом неприятных ощущений, исходящих из кишечника, в ущерб интересам семьи, работы, другим видам общественной деятельности и увлечениям» [4]. G. Engel предложена биопсихосоциальная модель СРК (1998): социальные потрясения вносят вклад в клинические проявления заболевания, болезнь развивается в результате стрессорного вмешательства в биологические, психологические и социальные сферы, взаимодействующие на различных уровнях, причём не в результате нарушения кишечной моторики, а при расстройстве регуляции между ЦНС и автономной энтеральной нервной системой [16].
Маев И.В., Drossman D.A. в своих работах придают большое значение при СРК состоянию высшей нервной деятельности и типу личности больного [9,13]. По характеру выраженности нервно-психических реакций эти больные составляют пограничную группу между нормой и психопатологией, а стресс является триггерным звеном развития психосоматических заболеваний. Жизнь, наполненная стрессами, играет важную роль в развитии симптомов функциональных заболеваний органов пищеварения [9,13].
Другие исследователи (Баранская Е.К., Ивашкин В.Т.) рассматривают патогенез СРК как взаимодействие генетической предрасположенности и воздействие сенсибилизирующих факторов (перенесенная кишечная инфекция, стресс) у личности психологическими особенностями характера [1,7]. Эмоциональная напряженность, возникающая при стрессе, приводит к соматическим изменениям благодаря реализации гипоталамических влияний через нервные пути, систему рилизинг-факторов и тропных гормонов гипофиза, что обусловливает изменения вегетативно-гуморальной регулиряции. Физиологические сдвиги характеризуются возрастанием активности симпатоадреналовой и гипоталамо-гипофизарно-надпочечниковой системы, усилением продукции катехоламинов и глюкокортикоидов [9,13]. На этом фоне либо на стадии истощения развиваются психосоматические нарушения, зависящие от типа психофизиологического реагирования. Низкая резистентность к стрессам приводит к нарушениям регуляции желудочно-кишечного тракта, нарушению висцеральной чувствительности и моторики кишечника, при этом изменяются энтероцеребральные связи и формируется симптомокомплекс раздраженного кишечника [1,9]. Общеизвестно, что гиперактивация гипотоламо-гипофизарно-надпочечниковой системы, включающая гиперкортизолемию является также одним из звеньев патогенеза ишемической болезни сердца (ИБС). Депрессия является дополнительным фактором риска при ИБС и оказывает отрицательное влияние на качество жизни этих больных[6].
Учитывая вышесказанное, целью исследования явилось изучить степень выраженности психологических нарушений и изменение качества жизни у больных с СРК и провести сравнительный анализ полученных результатов с данными полученными у здоровых лиц и пациентов с ИБС, перенёсших операцию аортокоронарного шунтирования (АКШ) (серьёзная соматическая патология).
Материалы и методы. В одномоментное исследование были выборочным методом включены 3 группы пациентов:
1-я группа – 30 человек, обратившихся в терапевтическое отделение клиники Кировской ГМА, которым в результате обследования был выставлен диагноз СРК. Диагноз был установлен на основании Римских критериев II и III, после проведённого обследования (общий анализ крови, биохимические показатели крови на общий билирубин, аспартатаминотрансферазу (АСТ), аланинаминотрансферазу (АЛТ), щелочную фосфотазу, гамма-глутамилтранспептидазу (ГГТП), глюкозу, креатинин; копрограмма, анализы кала на дизбактериоз, яйца глистов и цисты лямблий, на скрытую кровь, фиброгастродуоденоскопия (ФГДС) (гастрофиброскоп Olympus CIF XQ 40. Япония) с биопсией на Helicobacter pylori (Нр) (уреазный Helpil-test и метод мазка-отпечатка на Helicobacter pylori), ректороманоскопия, колоноскопия (колоноскоп Pentax FC 38 LV.Япония), ультразвуковое исследование (УЗИ) органов брюшной полости и малого таза, щитовидной железы, предстательной железы у мужчин (Medison Accuvix V-10. Корея), толстокишечная манометрия (Гастроскан-Д, Россия))
Средний возраст пациентов составил 36,4±3,9 года. Пациенты с «симптомами тревоги», органическими заболеваниями кишечника и сахарным диабетом были исключены из исследования.
2-я группа - 30 человек, страдающих ИБС (стенокардия напряжения I ФК-68% и II ФК- 32%) с умеренно выраженной ХСН (до II ФК по классификации NYHA), перенесших операцию АКШ (количество шунтов 2-5). Средний период после операции 6,6±3,3лет. Средний возраст 56,7±1,6 года. Все пациенты находились на плановом обследовании и лечении в клинике Кировской ГМА.
3-я группа – 30 человек практически здоровых лиц, проходивших диспансеризацию и отнесённых к Д-1, Д-II группам здоровья. Средний возраст 38,2±3,7 года.
Таблица 1. Характеристика групп пациентов по возрасту

Примечания: здесь и далее р1 - дисперсионный анализ, р2 – достоверность различий между 1 и 2 группами (критерий Стъюдента); р3 – достоверность различий между 1 и 3 группами; р4 – достоверность различий между 2 и 3 группами.
От каждого пациента было получено письменное информированное согласие на добровольное участие в исследовании. Все пациенты заполняли: опросник качества жизни МОS-SF-36 (компания Эвиденс - Клинико-фармакологические исследования) переведённый на русский язык «Институтом клинико-фармакологических исследований» Санкт-Петербурга и опросник по шкале Бека (Beck Depression Inventory). Они являются общими и применимы для сравнения качества жизни у различных групп здоровых лиц, больных различными заболеваниями, а так же между ними.
Понятие «качество жизни» сегодня прочно вошло в медицинскую терминологию. Это субъективный показатель удовлетворения личных потребностей в жизни, отражающий степень комфортности человека как внутри себя, так и в рамках своего общества.
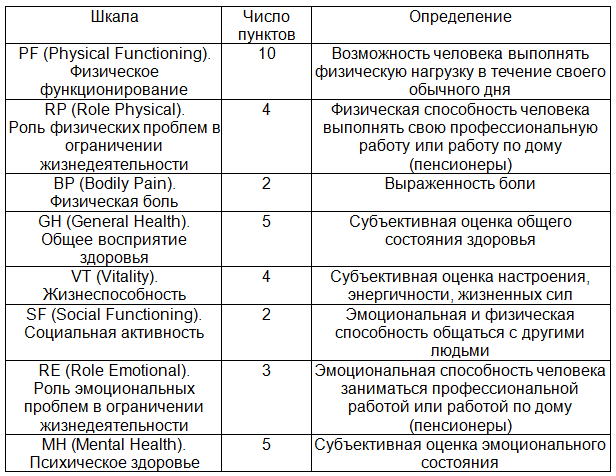
Анкета SF–36 включает 36 вопросов, которые отражают 8 шкал здоровья: физическую работоспособность, социальную активность, степень ограничения физической работоспособности и социальной активности, психическое здоровье, энергичность и утомляемость, боль, общую оценку здоровья (табл.2). Опросник обеспечивает количественное определение качества жизни по указанным шкалам. Показатели при этом варьируют от 0 до 100 баллов. Чем выше значение показателя, тем лучше оценка по избранной шкале [15].
Таблица 2. Определение концепций здоровья при использовании опросника SF-36
Шкалу депрессии Бека (Beck Depression Inventory), разработанную на основе клинических наблюдений [8], мы использовали для оценки наиболее значимых симптомов депрессии и наиболее часто предъявляемых пациентами жалоб. Опросник включает в себя 21 категорию симптомов и жалоб. Каждая категория состоит из 4-5 утверждений, соответствующих специфическим проявлениям депрессии. Показатель по каждой категории рассчитывается следующим образом: каждый пункт шкалы оценивается от 0 до 3 в соответствии с нарастанием тяжести симптома. Суммарный балл составляет от 0 до 62 и снижается в соответствии с улучшением состояния. При интерпретации данных учитывается суммарный балл по всем категориям:
0-9 – отсутствие депрессивных симптомов;
10-15 – легкая депрессия (субдепрессия);
16-19 – умеренная депрессия;
20-29 – выраженная депрессия (средней тяжести);
30-63 – тяжелая депрессия;
Градуально оценивается выраженность 21 симптома депрессии.
Пункты 1-13 – когнитивно-аффективная субшкала (C-A).
Пункты 14-21 – субшкала соматических проявлений депрессии (S-P).
Полученные данные обрабатывались с использованием общепринятых методов параметрической статистики. Использовались программы Microsoft Excel 2003 и BIOSTAT. Достоверность динамики показателей оценивали с помощью дисперсионного анализа, t-критерия Стъюдента. Статистически значимыми считали различия при р< 0,05.
Результаты и их обсуждение. В результате проведённого исследования было обнаружено достоверно значимое снижение качества жизни у пациентов с СРК по всем шкалам опросника SF-36 в сравнении со здоровыми (рис. 1, 2). Физическая активность (возможность выполнять физическую нагрузку в течение обычного дня) в группе СРК соответствовала 65,5±15,7 балла, что значимо ниже, чем в группе здоровых лиц - 89,3±3,5. Общее восприятие здоровья у больных СРК также значимо ниже, чем в контрольной группе 45,7±5,6 баллов, против 64,9±4,6 соответственно; социальная активность (эмоциональная и физическая способность общаться с другими людьми) соответствовала 51,7±8,2 балла при наличии СРК и 80,8±4,6 - у здоровых, что достоверно выше.
Почти в 3 раза чаще отмечали роль физических проблем в ограничении жизнедеятельности пациенты СРК в сравнении со здоровыми лицами. Таким образом, физическая способность у пациентов с СРК выполнять свою профессиональную работу или работу по дому была снижена до уровня 27,5±19,9 балла, в то время как у здоровых этот балл составил- 80,8±7,5.
Более чем в 2 раза выше оценивали выраженность боли пациенты при СРК, где суммарный балл составил 41,7±6,5, против аналогичного показателя у здоровых - 81,4±7,5 (чем ниже балл, тем более выражено восприятие боли). На этом фоне показатели энергичности, настроения, жизнеспособности, эмоционального состояния в группе СРК были ниже более чем в 1,5 раза: 36,3±5,9 против 67,3±4,6 у здоровых. Почти в 3 раза чаще эмоциональные проблемы ограничивали жизнедеятельность пациентов с СРК, снижая возможность заниматься профессиональной работой или работой по дому (суммарный балл 27,9±20 против 76,7±12,9 у здоровых). Субъективная оценка пациентами СРК психического здоровья была значимо ниже, чем у здоровых и составила 44,3±5,4 против 67,±6,2 баллов. Различия в группах по всем показателям опросника SF-36 были высоко достоверны р<0,001 (рис.2).
Задачей нашего исследования было также провести сравнение качества жизни и психологического статуса между пациентами с СРК (функциональным расстройством кишечника) и группой больных ИБС (стенокардия I-II ФК), перенесших операцию АКШ, причем последние по возрасту превышали основную группу (табл.1). Оказалось, что пациенты с функциональным заболеванием кишечника (СРК) гораздо ниже оценивали свою способность выполнять физическую нагрузку в течение обычного дня, чем больные ИБС, перенесшие операцию АКШ (суммарный балл- 65,5±15,7 против 76,3±9,7 соответственно), причем в 2 раза чаще пациенты основной группы придавали значение в ограничении своей жизнедеятельности физическим проблемам, на это указывают значения этого параметра в группах - 27,5±19,9 и 52,5±26,2 соответственно (чем ниже балл, тем выше роль проблем) (рис.1).
Субъективная оценка выраженности боли у пациентов с СРК, также как при сравнении с группой здоровых лиц, была выше, чем выраженность кардиалгий у пациентов с ИБС после операции АКШ (рис.1). Настроение, энергичность, эмоциональная способность общаться с другими людьми, психическое самочувствие были достоверно ниже при СРК, чем у больных с коронарной болезнью сердца: балл составил 36,3±5,9 против 65±6,1 соответственно. Значимо большее значение придавали эмоциональным проблемам в ограничении своей жизнедеятельности пациенты с СРК, в том числе способности заниматься своей профессиональной работой или работой по дому(27,9±20 против 63,3±16,4 при ИБС после АКШ) (чем ниже балл, тем выше роль проблем). Уровень психического здоровья пациенты с СРК оценили на 44,3±5,4 балла, а пациенты с ИБС достоверно выше в 1,5 раза (66,4±4,9). Социальная активность (эмоциональная и физическая способность общаться с другими людьми) существенно ниже у пациентов с СРК (51,7±8,2), чем у больных с ИБС после АКШ (74,2±3,3), несмотря на более высокую возрастную категорию последних.
Субъективная оценка настроения, энергичности, жизненных сил и эмоционального состояния больных перенёсших операцию АКШ достоверно не отличались от данных показателей здоровых лиц (65±6,1 и 67,3±4,6 баллов соответственно; р=0,105). Хотя физическая способность выполнять свою работу у пациентов с ИБС после АКШ достоверно ниже, чем у здоровых (52,5±26,2 и 80,8±11, р<0,001), а выраженность боли закономерно выше (р<0,001).
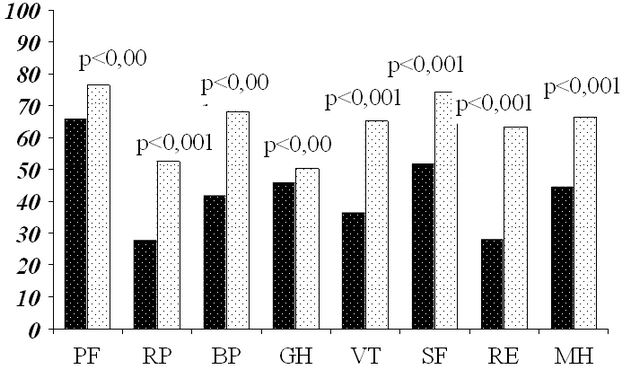
Рис. 1. Качество жизни у пациентов с СРК и больных ИБС, после АКШ: по оси абсцисс: здесь и далее показатели шкалы SF-36: PF - физическое функционирование, RP - роль физических проблем в ограничении жизнедеятельности, BP-физическая боль, GH - общее восприятие здоровья, VT - жизнеспособность, SF - социальная активность, RE - роль эмоциональных проблем в ограничении жизнедеятельности, MH - психическое здоровье. Тёмные столбики – пациенты с СРК, светлые столбики – пациенты с ИБС.
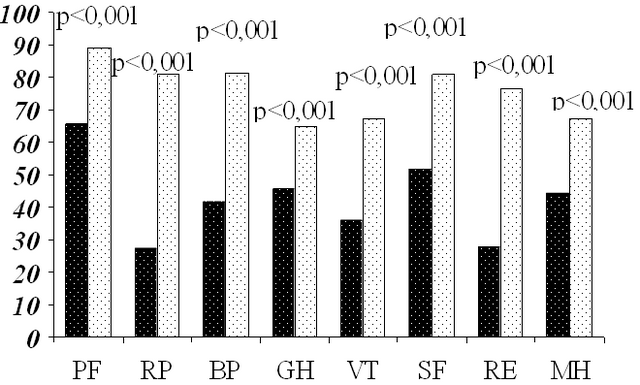
Рис. 2. Качество жизни у пациентов с СРК и здоровых людей: тёмные столбики – пациенты с СРК, светлые столбики – здоровые.
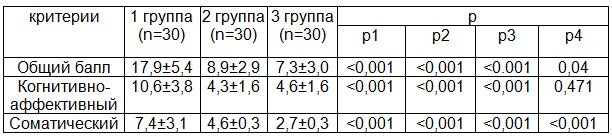
При оценке уровня депрессии по шкале Бека полученные результаты, указывают на значительно более выраженную депрессию у пациентов с СРК, чем в обеих группах сравнения (р<0,001) (табл. 3). Среди пациентов с СРК 10% находились в состоянии тяжёлой депрессии, 30% – выраженной депрессии, 17% - умеренной депрессии, а у 37% наблюдались лёгкие депрессивные расстройства. Таким образом, практически все пациенты с СРК нуждались в помощи психотерапевта с применением медикаментозных средств коррекции психоэмоционального состояния. У здоровых лиц и у пациентов с ИБС симптомы депрессии в основном отсутствовали (табл.3). Лёгкая депрессия (субдепрессия) наблюдалась только у 1 человека среди здоровых (3%) и у 3 пациентов с ИБС, что составило 10% (р=0,049).
Таблица 3. Уровень депрессии у пациентов с СРК, больных ИБС, перенесших АКШ и у здоровых людей
При проведении анкетирования, где пациентов просили указать на возможную, по их мнению, причину заболевания, 28 пациентов страдающих СРК из 30 опрошенных (93%) чётко указали на длительное стрессовое состояние (неприятности на работе и дома, тяжёлая болезнь или смерть близкого родственника, развод и т.д.). Причём 12 из них (43%) отмечали появление психоэмоциональных расстройств до начала абдоминальных симптомов, у остальных больных начало тревожно-депрессивных расстройств совпадало с дебютом кишечной симптоматики. Причиной вновь возникающих ухудшений самочувствия 26 из 30 (87%) также назвали стресс. Лишь 4 человека (13%) в качестве провоцирующего обострение фактора предположили нарушение в диете и физическую нагрузку. При беседе с пациентами, страдающими СРК, обращало на себя внимание их неспособность различать между собой физическую боль и эмоциональные переживания, высокий уровень тревоги и страха.
Выводы
- Уровень депрессии, снижение настроения, энергичности, жизнедеятельности, эмоционального состояния при СРК значительно более выражены, чем у здоровых людей и даже у больных ИБС, перенесших операцию АКШ.
- Психические нарушения, имеющиеся у большинства больных СРК, усугубляют тяжесть состояния пациентов, снижают их адаптационные возможности, мешают заниматься профессиональной работой и работой по дому, достоверно снижая качество их жизни.
- Полученные результаты исследования позволяют сделать вывод о необходимости дополнения терапии СРК средствами психофармакокоррекции и совместного ведения пациента врачами гастроэнтерологами и психотерапевтами. Это будет способствовать оптимальной регрессии клинических проявлений заболевания, одновременному повышению качества жизни больного и снижению экономических затрат на лечение данной категории пациентов.
