Введение. Одна из наиболее частых причин госпитализации пациентов в хирургический стационар, требующая оперативного лечения - паховые грыжи, на долю которых приходится до 70-80% в общей структуре наружных грыж живота [1, 4, 8, 11, 12].
Герниопластика паховой грыжи является одной из самых распространенных хирургических операций, по всему миру такая операция ежегодно проводится более чем у 20 миллионов людей [4, 11-13]. Несмотря на совершенствование хирургических вмешательств, актуальной остается проблема развития послеоперационной хирургической инфекции.
Развитие инфекций в области хирургического вмешательства - одна из причин увеличения длительности госпитализации, возникновения рецидива грыжи и повторной госпитализации, роста расходов на лечение [1, 2, 8, 10, 11].
Основу эффективного лечения послеоперационных инфекций составляет антибактериальная терапия. Траты на антибактериальные препараты, которые несет стационар весьма значительны и могут доходить до 40-50% затрат бюджета лечебных учреждений расходуемого на лекарства [6, 11, 13].
Если ранее единые цены на лекарственные средства устанавливались государством и осуществлялись централизованные закупки, распределение препаратов по регионам и учреждениям, то в рыночных условиях ценообразование является многофакторным, и цены могут варьировать в широком диапазоне.
В этой связи, определение помимо клинической еще и экономической эффективности различных схем антибактериальной терапии, несомненно важно.
Однако, часто, при выборе схемы лечения, с целью экономии средств, не всегда оправданным является включение в неё препаратов с исходно более низкой ценой, без учета особенностей режима введения, стоимости услуг, связанных с проведением инъекций, спектра действия антибиотиков, чувствительности флоры к препаратам, и возможных дополнительных трат при их применении, что в итоге может привести к удорожанию терапии.
В этой связи, актуальным будет выбор наиболее оптимальных схем антибиотикотерапии, не только с точки зрения эффективности, но и стоимости.
Исходя из изложенного, целью настоящей работы стало проведение экономического анализа разных схем антибактериальной терапии осложнений после грыжесечения.
Материал и методы. В работе изучены и проанализированы показатели пациентов, перенесших операцию грыжесечения по поводу паховой грыжи в хирургическом отделении БУ ХМАО-Югры «Сургутская городская клиническая больница» в 2014-2015 г.
Пациентам была выполнена паховая герниопластика по Bassini. Средний возраст прооперированных составил 61,45±0,95 лет. Оперативное лечение выполнялось в плановом порядке.
Основанием для назначения пациентам антибиотикотерапии послужило наличие послеоперационных осложнений, связанных с зоной операции (воспалительный инфильтрат, нагноение раны), которые наблюдались у 26 прооперированных.
Для эмпирической антимикробной терапии послеоперационных раневых осложнений в анализируемом стационаре применяли три схемы, в силу этого, актуальным был вопрос выбора помимо клинически и экономически более эффективного подхода.
Схема 1 - ингибиторзащищенный аминопенициллин ампициллин/сульбактам, выпускаемый в виде порошка по 1,5 г во флаконе с прилагаемым растворителем в коробке (вводили внутримышечно, в дозе 1,5 г каждые 8 часов).
Схема 2 - цефалоспорин I поколения цефазолин, выпускаемый в виде порошка по 1,0 г во флаконе без растворителя и аминогликозид III поколения амикацин, порошок по 0,5 г во флаконе без растворителя.
В данном случае, имела место необходимость дополнительного включения в стоимость и цены растворителя (цефазолин вводили внутримышечно, в дозе 2,0 г каждые 6 часов, амикацин внутримышечно, в дозе 1,0 г 1 раз в сутки).
Схема 3 - цефалоспорин III поколения цефтриаксон, в виде порошка во флаконе с приложением растворителя в коробке и производное нитроимидазола метронидазол, 0,5% раствор для инфузий во флаконе 100 мл (цефтриаксон вводили внутримышечно, в дозе 2,0 г 1 раз в сутки, метронидазол внутривенно, 0,5 г каждые 8 часов).
Клиническая картина показала, что нормализация состояния пациентов во всех случаях достигалась к пятым суткам терапии.
Проявлений нежелательных эффектов препаратов в процессе терапии выявлено не было. При наличии идентичной эффективности актуальным стал вопрос предпочтения той или иной схемы исходя из стоимости терапии.
Стоимость курса лечения каждой схемой рассчитывалась путем суммирования стоимости лечебных манипуляций и стоимости лекарственных препаратов [3, 5, 9].
Стоимость услуги рассчитывали по формуле: У=СхЧ, где У - затраты на предоставление услуги, С - стоимость услуги, Ч - частота предоставления услуги. Стоимость ориентировочной дневной дозы препарата рассчитывалась по формуле: ОДД=С/(N x n) x K, где ОДД - стоимость ориентировочной дневной дозы, С - стоимость упаковки препарата, N - количество флаконов в упаковке, n - количество миллиграмм во флаконе, К - количество миллиграмм в дневной дозе.
Стоимость эквивалентной курсовой дозы рассчитывали по формуле: ЭКД=С/(N x n) x K, где ЭКД - стоимость эквивалентной курсовой дозы, С - стоимость упаковки препарата, N - количество флаконов в упаковке, n - количество миллиграмм во флаконе, К - количество миллиграмм в эквивалентной курсовой дозе.
В силу того, что анализируемые режимы терапии обладали одинаковым лечебным эффектом, для экономической оценки альтернативных схем антибиотикотерапии был использован «анализ минимизации затрат» (cost minimization analysis (СМА)) [3, 5, 9].
Нами были проведены расчеты прямых затрат на одного пациента на основе данных о стоимости препаратов и лечебных манипуляций за курс терапии по каждой используемой схеме.
Расчет указанных затрат был основан на данных реестра медицинских услуг, затрат на приобретение лекарственных препаратов, трудозатрат БУ ХМАО-Югры «Сургутская городская клиническая больница».
В силу того, что мы проводили анализ в одном и том же стационаре, то косвенные затраты, не связанные напрямую с лечебным процессом (оплата услуг связи, транспортные услуги, административно-хозяйственные расходы и т.п.) не учитывались, так как они не влияют на эффективность лечения и равны при рассматриваемых методах лечения.
Для расчета разницы затрат, использовали формулу: СМА=Сhigh-Clow, где СМА - показатель разницы затрат; Сhigh и Clow - прямые затраты на использование соответственно более и менее затратной терапии. Упущенные возможности при применении более затратной терапии (Q) определяли по формуле: Q=СМА/Clow [5, 9].
Результаты и обсуждение. Результаты, отражающие стоимость используемых препаратов и услуг по их введению, представлены в таблице 1.
Сравнительная оценка различных режимов антибиотикотерапии осложнений после грыжесечения показала при наличии одинаковой эффективности используемых подходов, различия в экономических затратах (табл. 1).
Как видно из табл. 1, стоимость курса терапии ампициллин/сульбактамом составила 2102,9+2385,0=4487,9 руб. на одного человека, стоимость курса терапии комбинацией цефазолина с амикацином, с учетом стоимости растворителя (1333,6+48,0+3180,0)+(248,0+30,0+795,0)=5634,6 руб. на одного больного, а цефтриаксона с метронидазолом соответственно (304,6+795,0)+(574,7+3225,0)=4899,3 руб. на одного пациента.
Таким образом, расчет прямых затрат указывает на то, что лечебный эффект ингибиторзащищенного аминопенициллина достигнут меньшими суммарными тратами, чем при терапии иными, применяемыми в стационаре антимикробными схемами.
Проведенный анализ минимизации затрат показал, что экономия при использовании схемы 1, по сравнению со схемой 2 составила 1146,7 руб. (СМА=5634,6-4487,9=1146,7), а со схемой 3 - 411,4 руб. (СМА=4899,3-4487,9=411,4) (табл. 1). Разница между затратами при назначении схемы 3, по сравнению с более затратной схемой 2 была 735,3 руб. (СМА=5634,6-4899,3=735,3) (табл. 1).
Несмотря на исходно большую стоимость препарата ампициллин/сульбактам (140,19 руб. за флакон), по сравнению с антибактериальными препаратами, составивших основу других схем лечения (цефазолин - 33,34 руб., амикацин - 24,80 руб., цефтриаксон - 30,46 руб. и метронидазол 38,1 руб. за флакон), что часто служит фактором ограничивающим его применение, факт более высокой экономической эффективности препарата объясняется возможностью проведения монотерапии и, как следствие, в целом меньшей кратностью его назначения, а значит снижения затрат на услуги по введению, материалы для проведения инъекций/инфузий (это вносит существенный вклад в стоимость других схем терапии (табл. 1)), отсутствием необходимости дополнительных затрат на растворитель.
Таблица 1. Стоимость лекарственных препаратов и услуг для проведения антибиотикотерапии осложнений после грыжесечения (затраты на лечение 1 пациента)
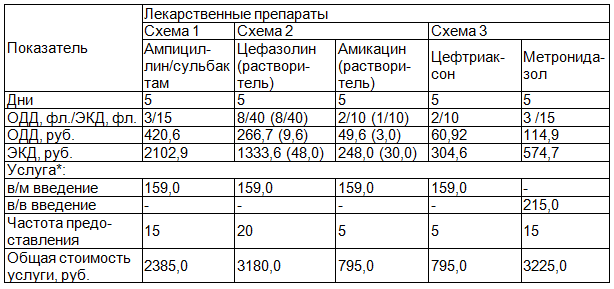
Примечание: * - стоимость с учетом цены вспомогательных материалов для проведения инъекций/инфузий.
Приоритетность назначения ампициллин/сульбактама необходимо рассматривать и с точки зрения микробиологических аспектов. Как известно, спектр антимикробной активности препарата, используемого для эмпирической антибиотикотерапии, должен включать наиболее вероятных возбудителей инфекции области хирургического вмешательства и, прежде всего флоры, обнаруживаемой в конкретном стационаре [2, 6, 7].
Проведенное бактериологическое исследование у пациентов с послеоперационными раневыми осложнениями показало, что наиболее часто (до 85% случаев) обнаруживаются Staphylococcus aureus, в отношении которых активность проявляли ингибиторзащищенный аминопенициллин, цефазолин, цефтриаксон и амикацин.
В 12% проб обнаружены представители семейства Enterobacteriaceae (E.coli), которые были чувствительны к ампициллин/сульбактаму, цефтриаксону и амикацину, умеренно чувствительны к цефазолину и устойчивы к метронидазолу.
Обращает на себя внимание, что в ряде случаев (3%) высевались Enterococcus faecalis, чувствительные лишь к ампициллин/сульбактаму и резистентные к другим используемым в обсуждаемых схемах антимикробным средствам.
Анаэробные микроорганизмы бактериологическим методом выявлены не были, но, согласно литературным данным [2, 7, 11], идентифицируются у большинства пациентов с инфекционными осложнениями после различных видов операций на органах брюшной полости.
В этой связи, наличие высокой антиэнтерококковой, антианаэробной и антиколибактериозной активности у ингибиторзащищенных аминопенициллинов, делает использование ампициллин/сульбактама более предпочтительным.
Можно предположить, что не учитывание указанного факта может стать одной из причин, которая создаст проблему недостаточной эффективности иных, применяемых в стационаре схем терапии в будущем.
Расчет упущенных возможностей, который показывает, сколько дополнительно пациентов на один курс терапии можно пролечить при переходе на менее затратный метод, дал следующий результат: при переходе со схемы 2 на схему 1 Q=(5634,6-4487,9)/4487,9=0,26; в случае перехода со схемы 3 на менее затратную схему 1 Q=(4899,3-4487,9)/4487,9=0,09; при переходе со схемы 2 на схему 3 Q=(5634,6-4899,3)/4899,3=0,15.
Величина полученного показателя свидетельствует о том, что переход на менее затратную схему позволит сэкономить средства и в рамках выделенного бюджета пролечить больше пациентов (соответственно, на 26%, 9% и 15%).
Заключение. Развитие инфекций в области хирургического вмешательства является одной из основных причин увеличения длительности пребывания хирургических пациентов в стационаре, повышения летальности среди данного контингента больных, а также затрат на лечение.
Помимо экономических (прямых медицинских и немедицинских) затрат, связанных с лечением осложнений в постоперационном периоде, необходимо учитывать и нематериальные затраты: тяжелые физические и моральные страдания, испытываемые пациентом и увеличение профессионального риска медицинских работников.
Снижение частоты развития этой патологии достигается путем использования целого комплекса мероприятий, причем основную роль при этом играет рациональная как с точки зрения клинической, так и экономической эффективности антибиотикотерапия.
Полученные нами данные свидетельствуют об экономическом преимуществе антибиотикотерапии амциллин/сульбактамом перед использованием других применяемых в анализируемом стационаре схем лечения осложнений после операции грыжесечения.
Более дорогой по себестоимости оказалась антибиотикотерапия комбинацией цефазолина с амикацином. Экономическая эффективность антибиотикотерапии с использованием ингибиторзащищенного аминопенициллина оказалась более высокой и была менее затратной (на 1146,7 руб. по сравнению с комбинацией цефазолина с амикацином и на 411,4 руб. по сравнению со схемой включавшей цефтриаксон и метронидазол).
Переход на использование менее затратной схемы с ингибиторзащищенным аминопенициллином позволит сэкономить средства и в рамках выделенного бюджета пролечить больше пациентов.
