Предменструальные нарушения составляют спектр эмоциональных и физических симптомов, в большинстве своем наблюдающихся в течение лютеиновой фазы менструального цикла. Характер и интенсивность проявлений имеет значительную вариабельность от небольшого дискомфорта, ежемесячно переживаемого женщинами, до тяжелых проявлений, существенно снижающих качество жизни [1].
К настоящему моменту накоплен обширный объем информации об эффективности ингибиторов обратного захвата серотонина в лечении тяжелых форм предменструального синдрома (ПМС). Однако быстро наступающий эффект при назначении этих препаратов диктует необходимость полномасштабного изучения режимов назначения и оптимальных дозировок.
Имеет широкую распространенность теория, согласно которой развитие симптоматики инициируется повышением выработки прогестерона в период после овуляции [2]. В связи с чем, супрессия овуляции хирургическим или медикаментозными методами в некоторых случаях может стать оправданным шагом в достижении терапевтического эффекта [3].
Существуют мнения, согласно которым развитие предменструальных нарушений является отражением срыва важных физиологических механизмов обмена таких микроэлементов как кальций, и адекватное восстановление нарушенного баланса может способствовать обратному развитию нейропсихических и физических проявлений предменструальных нарушений.
В целом можно сказать, что к сегодняшнему дню предложены различные методы лечения предменструальных нарушений, при этом основными методами считаются использование ингибиторов обратного захвата серотонина и оральных контрацептивов.
Вместе с тем, оценка эффективности комплексной терапии данного состояния в литературе освещена крайне недостаточно.
Целью данного исследования явилось проведение многофакторной оценки эффективности применения комплексной терапии тяжелой формы предменструальных нарушений с включением ингибиторов обратного захвата серотонина, оральных контрацептивов, содержащих дросперинон, кальция и омега-3 полиненасыщенных жирных кислот.
Пациенты и методы
Участницами стали 328 женщин в возрасте от 20 до 35 лет. При отборе пациенток для включения в исследование руководствовались следующими критериями: наличие регулярных менструальный циклов продолжительностью от 22 до 35 дней; наличие клинических проявлений предменструального синдрома в течение как минимум 6 месяцев; влияние симптомов на ежедневно выполняемую активность (рабочие обязанности, семейные отношения, социальная активность), отсутствие психических заболеваний, удовлетворительное состояние здоровья, в общем, наличие подтвержденных критериев ПМС, согласно проведенной двухмесячной проспективной оценке самочувствия с использованием «предменструального профиля».
Критериями исключения из исследования выбраны: психические заболевания, расстройство аппетита, злоупотребление алкоголем, применение психотропных средств, прием любых лекарственных средств для лечения симптомов ПМС до начала исследования, беременность, кормление грудью, гистерэктомия, клинические проявления эндометриоза в виде болевого синдрома, нерегулярные менструации, какое-либо серьезное соматическое заболевание, риск суицида.
Диагноз тяжелой формы ПМС и предменструального дисфорического расстройства (ПДР) предварительно выставлялся на основании анализа заполненных вопросников самооценки «Предменструальный профиль» [4], т.е в случаях, когда общая оценка симптомов, наблюдаемых в дни лютеиновой фазы, превышала оценки в дни фолликулиновой фазы на 50 % и более. Данный вопросник был выбран исследователями, так как отличался простотой и удобством заполнения.
Далее, при проведении структурированного интервью до распределения в группы терапии и дальнейшем наблюдении за пациентками использовался Ежедневный Вопросник Выраженности Симптомов (Daily Record of Severity of Problems (DRSP)) [5].
Подтверждение диагноза тяжелого ПМС/ПДР проводилось в день интервью при подсчете суммарных оценок самочувствия по вопроснику DRSP. Применение данного инструмента является широко распространенным и подтвержденным методом диагностики предменструальных нарушений. Вопросник состоит из всех 24 пунктов, отражающих наличие предменструального дисфорического расстройства, включенных в DSM –IV. Двадцать один вопрос помогает оценить степень выраженности психологических и физических симптомов ПДР, последние три нацелены на оценку трех доменов функциональности пациентки: 1) продуктивность (работоспособность) на работе, дома или в учебном заведении; 2) социальную активность; 3) степень сохранения межличностных отношений. Тяжесть каждого из вопросов оценивалась по 6-ти балльной шкале: 1 - отсутствие симптомов, 4 - умеренная симптоматика, 6 - наиболее тяжелые проявления. В период проведения терапии пациенток просили заполнять вопросники ежедневно. Для участия в исследовании по каждому из трех последних пунктов пациенткам требовалось набрать не менее 2 баллов.
Для подтверждения диагноза тяжелого ПМС/ПДР было необходимо, чтобы как минимум 5 симптомам вопросника DRSP пациенткой была присвоена рейтинговая оценка 4.
Для оценки состояния в дальнейшем использовались суммарные оценки, которые высчитывались путем сложения рейтинговых оценок для постменструальных (фолликулиновых) дней - с первого по пятый и предменструальных дней цикла - шесть дней до начала менструации. При необходимости пациентки направлялись к соответствующему специалисту для исключения психического заболевания.
После установления диагноза пациентки, включенные в исследование, приглашались на визит к специалисту в лютеиновую фазу цикла. В течение этого визита специалист оценивал общий статус здоровья, наличие и степень выраженности предменструальных симптомов, проводил необходимый физикальный и гинекологический осмотр, распределял пациенток в группы терапии. Лабораторные исследования включали биохимический анализ крови, профиль тиреоидных гормонов, ФСГ, общий анализ крови, общий анализ крови и мочи.
Терапия и динамическая оценка состояния проводилась в течение трех месяцев, контрольные визиты к специалисту планировались один раз ежемесячно. В общей сложности каждой женщине, участвовавшей в исследовании, предстояло сделать семь визитов в лечебное учреждение: первый скрининговый визит, два визита во время заполнения «предменструального профиля», три визита во время назначенной терапии и один визит в конце лечения. В рамках исследования было принято, что при пропуске назначенной терапии в течение 6 дней и незаполнении дневников самооценки пациентки считались выбывшими из исследования вследствие нарушения лечебного режима.
Все пациентки, принявшие участие в исследовании, были разделены на экспериментальную и группу традиционной терапии.
Традиционная терапия тяжелых форм предменструального синдрома/предменструального дисфорического расстройства начиналась с первого дня менструального цикла и состояла в назначении орального контрацептива, содержащего дросперинон (Джес), с первого дня менструации в режиме 24/4.
В группе предлагаемой терапии к назначению орального контрацептива в том же режиме добавлялось назначение ингибиторов обратного захвата серотонина (пароксетин) по 20 мг в день в лютеиновую фазу (с 13 дня цикла), добавки кальция и рыбьего жира по 1 гр в день в непрерывном режиме с первого дня менструации.
Дополнительно и в уместных случаях женщинам рекомендовалось использовать барьерные методы контрацепции в течение всего периода исследования.
Безопасность назначаемых доз препаратов контролировалась путем периодической оценки общего самочувствия, основных жизненных показателей, общепринятых рутинных лабораторных тестов, изменений характеристик менструальной функции. Общая схема дизайна исследования представлена на рис. 1.
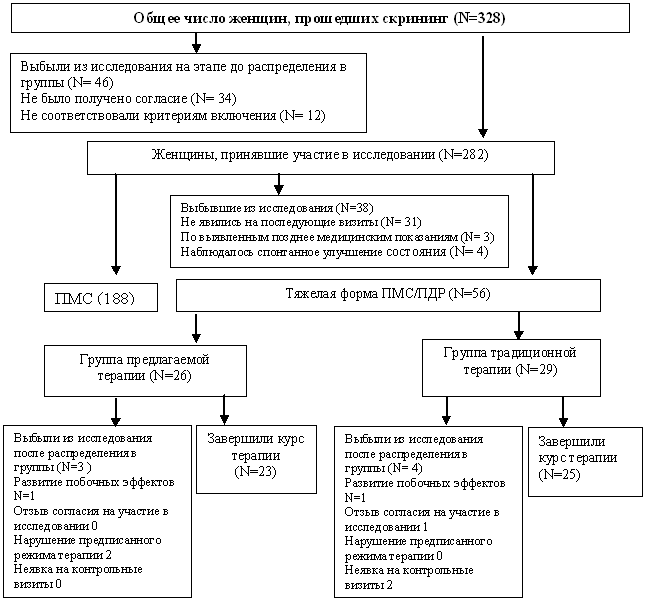
Рис. 1. Схема дизайна исследования.
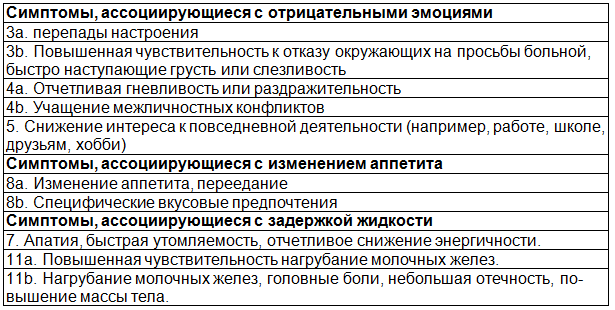
Основу оценки эффективности терапии составила динамика тяжести состояния в течение лютеиновых фаз циклов терапии. Для удобства проведения анализа симптомы были разделены на три группы: 1) Симптомы, ассоциирующиеся с отрицательными эмоциями, 2) Симптомы, ассоциирующиеся с изменением аппетита, 3) Симптомы, ассоциирующиеся с задержкой жидкости (табл. 1).
Таблица 1. Десять пунктов вопросника DRSP, отобранные в кластеры для анализа
Статистический анализ результатов был проведен с использованием программного обеспечения Epi Info Version 3.5.3 (http://wwwn.cdc.gov/epiinfo/).
Результаты и их обсуждение
Из 328 женщин, прошедших первоначальный скрининг, 46 выбыли на этапе до распределения в группы. Из них 34 не дали согласие на участие в исследовании, 12 не соответствовали критериям включения. Не явилась на последующие визиты 31 женщина. У 3 пациенток выявлены медицинские проблемы, препятствовавшие дальнейшему продолжению участия. Спонтанное улучшение состояния зарегистрировано у 4 женщин. У 244 женщин были выявлены различные формы предменструального синдрома. Фокусом данного исследования стали 56 пациенток, имевшие критерии предменструального дисфорического расстройства/тяжелой формы предменструального синдрома.
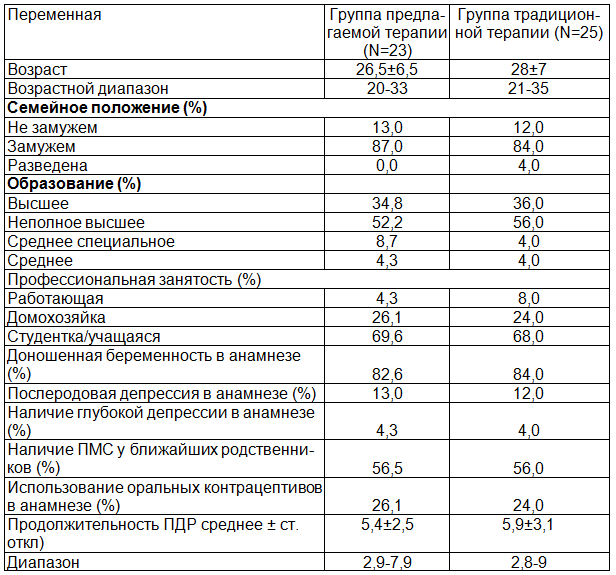
Типичная пациентка – участница исследования имела следующие демографические характеристики: образование высшее (35,4%) или незаконченное высшее (54,2%), домохозяйка (25,0%), либо посещающая учебное заведение (68,8%), замужем (85,4%) и имеющая одного-двух детей (83,3%) (табл. 2).
Таблица 2. Основные социально-демографические характеристики изучаемой выборки
При проведении скрининговой беседы выяснилось, что 37 (77%) участниц отмечали снижение работоспособности в дни перед менструацией как минимум в течение последнего месяца.
Довольно большое число женщин отмечали использование оральных контрацептивов в анамнезе (25%)
Снижение настроения в послеродовом периоде анамнестически отметили 12,5% участниц.
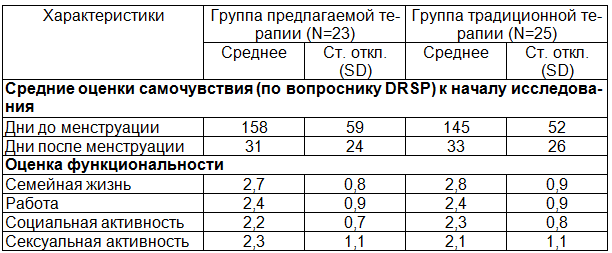
К моменту включения в исследования средние оценки самочувствия, согласно вопроснику Daily Record of Severity of Problems, составили 158 и 145 в группе предлагаемой и традиционной терапии соответственно (табл. 3).
Таблица 3. Базисные клинические характеристики пациенток к моменту включения в исследование
Проявление побочных действий препаратов наблюдалось у 7 пациенток. В общем, побочные действия были незначительными и спонтанно исчезали при продолжении терапии. Среди всего возможного спектра побочных эффектов назначаемых препаратов зарегистрированы тошнота, ощущение сухости во рту, бессонница. У трех женщин интенсивность нежелательных эффектов терапии была выражена настолько, что явилась препятствием для продолжения участия в исследовании. В группе традиционной терапии у одной из пациенток отмечалось развитие чрезмерной тошноты и выраженных мигренеподобных головных болей, что и явилось причиной для прекращения дальнейшего участия в исследовании. В экспериментальной группе у одной из женщин отмечалось развитие кожной сыпи и зуда, вследствие чего дальнейший прием препаратов был прекращен.
Из 56 пациенток, распределенных в группы, до финала исследования терапию продолжили только 48 (25 – в группе традиционной терапии и 23 – в группе предлагаемой). Причинами выбывания послужили: Отзыв согласия на участие в исследовании - 1, нарушение предписанного режима терапии - 2, неявка на контрольные визиты- 2
Динамическое наблюдение и оценка состояния пациенток в течение трех циклов терапии в обеих группах показало снижение оценок симптомов относительно базового уровня (табл. 4).
Таблица 4. Динамическое наблюдение и оценка состояния пациенток в течение трех циклов терапии
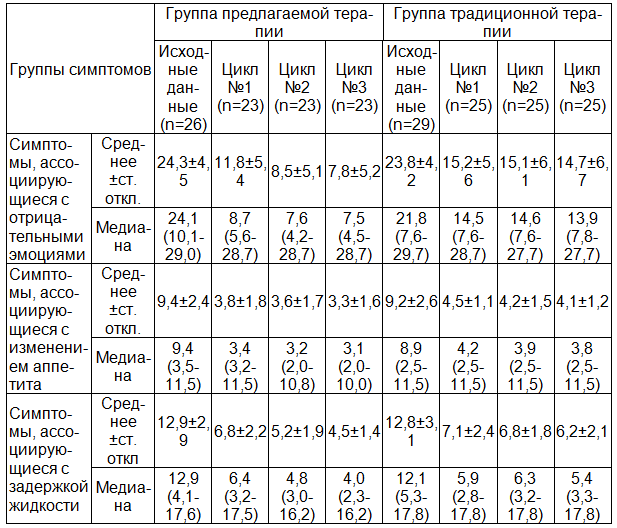
Средний процент снижения оценок для каждой группы симптомов оказался больше в группе предлагаемой терапии. При сравнении групп наибольший эффект в снижении оценок симптоматики наблюдался среди пациенток экспериментальной группы по истечении первого месяца лечения.
Тренд к улучшению самочувствия в обеих группах наблюдался и в дальнейшем, на протяжении 2 и 3 месяца терапии, однако эффективность предлагаемой терапии оказалась несколько выше. Результаты наглядно представлены на Рисунке 2. Анализ эффективности обоих видов лечения, проведенный с учетом групп симптомов, показал, что наиболее значимых результатов по снижению оценок самочувствия удалось добиться в экспериментальной группе в плане улучшения эмоционального состояния и снижения степени выраженности симптомов задержки жидкости. В группе предлагаемой терапии пациентки в большей мере отмечали улучшение взаимоотношений в семье, межличностных контактов, повышение уровня и качества социальной активности.
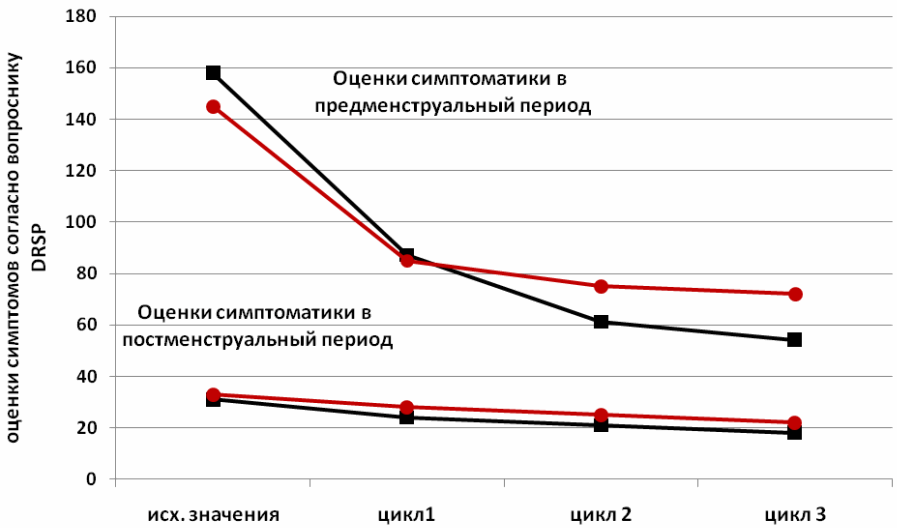
Рис. 2. Динамика пре- и постменструальных симптомов в течение трех циклов терапии.
Все пациентки, досрочно прекратившие предлагаемую терапию, принимали препараты как минимум в течение месяца, несмотря на это все женщины отметили улучшение самочувствия, проявившееся, в основном, в виде снижения эмоционального напряжения и повышения настроения.
Ответ на терапию в отношении исчезновения симптомов после менструации также был более значимым в группе предлагаемой терапии, однако, несмотря на то, что улучшение отметили как женщины с изначально выраженной симптоматикой, так и те, у которых проявления были незначительными, клинически значимой эффективности терапия достигла только среди последней категории пациентов. Женщины, имевшие более высокие оценки симптоматики в постменструальном периоде, отмечали улучшение, однако уровень симптомов все же оставался высоким.
Клинический ответ на терапию, согласно снижению процента оценок самочувствия, составил 69,6% (16 человек) в группе предлагаемой терапии и 52% (13 человек) в группе традиционного лечения. Снижение средней оценки предменструальной симптоматики на 75% наблюдался у 26% женщин в группе предлагаемой терапии.
Нарушений показателей общих лабораторных исследований в обеих группах пациенток отмечено не было.
По определению, ПДР является состоянием, способным серьезно снизить качество жизни, нарушить привычный ежедневный ритм страдающих этим недугом женщин, повлиять на взаимоотношения пациенток с членами семьи, коллегами по работе, сверстниками в учебном заведении.
Влияние ПДР на взаимоотношения в семье и выполнение родительских обязанностей сравнивается с нарушениями, обнаруживаемыми у больных с глубокой депрессией [6,7]. Обзоры, посвященные исследованию тяжелых форм ПМС/ПДР, показывают, что от 3 до 16% женщин не могут выполнять соответствующие обязанности на работе вследствие развивающихся клинических проявлений заболевания. [8].
В недавнем исследовании глобального масштаба, нацеленного на выяснение влияния симптомов ПМС/ПДР на каждодневную активность женщин, было доказано, что больше всего страдает сфера взаимоотношений между супругами, членами семей, снижается трудоспособность [9,10].
Результаты проведенной нами работы показывают, что участницы исследования также имели высокие базовые оценки интенсивности клинических проявлений, отмечали ощутимые перепады настроения, чувствовали резкое снижение возможности установления межличностных отношений.
Некоторая эффективность отдельных компонентов предлагаемой терапии доказана во многих серьезных научных изысканиях. Так, данные полученные в ходе проведения двойных слепых, плацебо-контролируемых рандомизированных исследований, а также мета-анализов, указывают на стабильное улучшение самочувствия женщин, принимающих ингибиторы обратного захвата серотонина в лютеиновую фазу цикла.
Результаты данной работы показывают, что включение этого класса лекарственных средств в комплекс предлагаемой терапии и ограничение приема ингибиторов обратного захвата серотонина лишь лютеиновой фазой цикла привело к снижению вероятности развития побочных действий при сохранении стойкой положительной динамики в ответ на проводимую терапию. Кроме того, наблюдаемые положительные эффекты при назначении пароксетина в относительно низких дозах могут служить доказательством вовлечения серотонина в патофизиологические механизмы развития предменструальных симптомов, а также указывают на существующую разницу в механизмах развития предменструального синдрома и предменструального дисфорического расстройства. Существующие теории объясняют эту разницу в наличии динамически возникающей уязвимости к флюктуациям гормонов, обусловленной генетическими и внешними факторами, а также взаимодействиями между флюктуациями гормонов и нейротрансмиттеров.
Возрастающий интерес к омега-3 полиненасыщенным жирным кислотам в лечении различных видов нарушения настроения, включая биполярное расстройство, появился послу опубликования результатов хорошо известного плацебо-контроллируемого исследования [11].
Получены доказательства о том, что омега-3 жирные кислоты могут модулировать метаболизм нейротрансмиттеров и предполагается их способность ингибировать трансдукцию нейрональных сигналов по типу препаратов лития и вальпроата [12]. Кроме того, хорошо известны доказательства эффективности пищевой поддержки омега-3 полиненасыщенными жирными кислотами в лечении таких серьезных видов патологии, как глубокая депрессия и шизофрения, пограничные расстройства личности [13-16].
С этих позиций видится оправданным включение в комплексную терапию рыбьего жира - основного естественного источника омега-3 полиненасыщенных жирных кислот.
В ряде исследований было показано существование ассоциации между циклическими изменениями кальциевого обмена и нестабильностью настроения в течение менструального цикла у женщин с предменструальными нарушениями [17]. Также некоторыми авторами было доказано наличие связи между снижением функции паращитовидных желез и гипокальцемией в развитии депрессивных состояний [18]. Полученные в ходе проведения данного исследования результаты поддерживают выдвигаемое в литературе предположение о важности и необходимости поддержки кальцием женщин с предменструальными нарушениями для снижения интенсивности клинической симптоматики [19].
Вместе с тем, для получения полноценных доказательств следует провести исследование изменений кальцемии в группах женщин, участвовавших в исследовании.
Данная работа, в совокупности с результатами исследований, опубликованных другими авторами [20-22], подтверждает наличие периодичности и цикличного характера патологии, при котором терапия может показать свою эффективность, если проводится в определенном периоде менструального цикла и обосновывается с позиций существующих и изученных патогенетических механизмов [23,24].
Результаты проведенного исследования демонстрируют, что подход к терапии тяжелых форм ПМС/ПДР с использованием комплекса этиопатогенетических средств, позволяет добиться значительного уменьшения клинических проявлений этого заболевания.
Важность проведенной работы с практической точки зрения состоит и в том, что динамическое наблюдение за участницами исследования позволило доказать, что комплексный подход к терапии тяжелых форм ПМС/ПДР индуцирует более благоприятные адаптационные ответы организма, приводящие к менее выраженному спектру клинических проявлений болезни, сопровождается снижением вероятности развития побочных действий препаратов.
