Частота бесплодных браков в разных регионах России составляет 15-19%. При увеличении этого показателя до 15% неблагоприятную демографическую ситуацию можно рассматривать как серьезную проблему для здравоохранения, общества и государства [1]. Вспомогательные репродуктивные технологии (ЭКО – экстракорпоральное оплодотворение, ИКСИ – интрацитоплазматическая инъекция сперматозоида) дают сегодня возможность преодолеть бесплодие в тех ситуациях, когда традиционные методы лечения неэффективны (отсутствие и непроходимость маточных труб, тяжелые нарушения сперматогенеза). Однако частота наступления беременности после ЭКО/ИКСИ по данным Российской ассоциации репродукции человека составляет не более 30-40% из расчета на перенос эмбрионов, а частота родов 19-21%, и эти показатели не имеют стойкой тенденции к изменению [2]. В связи с этим изучение факторов, влияющих на результативность программ ЭКО/ИКСИ, является одной из главных целей многочисленных отечественных и зарубежных исследований в области репродуктологии [3-6].
Хронический эндометрит (ХЭ) является одним из наиболее часто встречающихся заболеваний у пациенток, планирующих циклы ЭКО/ИКСИ, его частота по данным разных авторов составляет 30-86% [7-9]. Данные литературы о влиянии хронического эндометрита на эффективность ЭКО немногочисленны и противоречивы. Есть сообщение о возможности наступления и успешного вынашивания беременности при морфологически подтвержденном хроническом эндометрите без лечения [10]. Другие авторы сообщают о значительном снижении частоты имплантации в циклах ЭКО при этой патологии и повышении эффективности ЭКО после проведения курса эмпирической антибактериальной терапии [11]. Kasius, J.C. отрицает негативное влияние ХЭ на исходы ЭКО [12].
В доступной нам литературе мы не обнаружили данных об общей частоте родов и возможных предикторах наступления беременности и родов после ЭКО/ИКСИ у пациенток с ХЭ.
Цель исследования – оценить эффективность ЭКО/ИКСИ у инфертильных пациенток с хроническими эндометритами в зависимости от количества попыток переноса эмбрионов и выявить факторы, взаимосвязанные с ней.
Материалы и методы исследования. В проспективное когортное исследование включены двести шестьдесят семь инфертильных пациенток с морфологически верифицированным диагнозом хронического эндометрита (ХЭ), которым было показано проведение ВРТ.
Всем пациенткам проведено стандартное общеклиническое обследование и дополнительные методы исследования: бактериологическое, гормональное, ультразвуковое, эндоскопическое и гистологическое. При выявлении ИППП на амбулаторном этапе проводилось соответствующее лечение с последующим его контролем. Жидкостная гистероскопия проводилась на 6 - 8 день цикла с биопсией эндометрия. Гистологическое исследование эндометрия проводилось по стандартной методике формалиновой фиксации, спиртовой проводки и парафиновой заливки с изготовлением срезов толщиной 6-8 мкм и их окраской гематоксилином и эозином. Морфологический диагноз хронического эндометрита основывался на выявлении очаговой и/или диффузной лимфогистиоцитарной инфильтрации и фиброза стромы, склеротических изменений стенок спиральных артерий эндометрия [12]. В зависимости от выявленной патологии во время клинико-лабораторного и эндоскопического обследования проводилась соответствующая коррекция с последующей комплексной прегравидарной подготовкой. Антибактериальную терапию назначали по показаниям при выявлении этиологического фактора.
Количество переносов эмбрионов после ЭКО/ИКСИ у одной пациентки составило от одного до шести. Каждой пациентке проводили подсадку от одного до трех эмбрионов высокого и хорошего качества (Grade I-II по Gardner и Sсhoolkraft). Всего у 267 пациенток проведено 537 переносов эмбрионов, в том числе 64 криопереноса (11,9%).
С целью выявления факторов прогноза наступления беременности и родов среди обследованных пациенток выделены три группы: основная группа – 83 пациентки с наступившей после ЭКО/ИКСИ после первой или второй попытки переноса эмбрионов беременностью, которая закончилась рождением живого ребёнка. Первая группа сравнения - 41 пациентка с беременностью после ЭКО/ИКСИ, закончившиеся самопроизвольным абортом раннего срока один и более раз при отсутствии родов на момент проведения исследования. Вторая группа сравнения - 72 пациентки, имевших две и более неудачных попытки ЭКО/ИКСИ. Из исследования исключены пациентки, которым проводились донорские программы. Определение статистической значимости различий проводили при помощи критерия χ2, точного двустороннего критерия Фишера для качественных переменных и U-критерия Манна-Уитни для количественных переменных. Для сравнения долей трех групп применяли многопольные таблицы сопряженности [13].
Для наглядного представления общей частоты родов живым плодом в зависимости от количества переносов эмбрионов (включая криоперенос) использован метод Каплана-Майера. Метод Каплана-Майера первоначально предложен как метод анализа выживаемости, однако в широком смысле – это анализ времени до наступления какого-либо события (в данном случае – роды живыми детьми после ЭКО/ИКСИ), включающий в себя оценку вероятности того, что некоторое событие произойдет в тот или иной момент времени [14,15]. В контексте данного исследования таким моментом времени может считаться эмбриотрансфер, т.к. беременность и роды у пациенток в исследуемой группе могут наступить только после переноса эмбрионов. Кривая Каплана-Майера является ступенчатой функцией, которая показывает долю пациенток, родивших жизнеспособных детей в те моменты, которые соответствуют основным точкам деления временной оси (порядковый номер переноса эмбрионов). Во всех процедурах статистического анализа критический уровень значимости р принимался равным 0,05 [14]. Расчеты выполнены при помощи программного пакета IBM SPSS Statistics v.19.
Результаты исследования. Общее количество переносов эмбрионов у 267 пациенток составило 537, в результате которых наступило 148 беременностей (27,7%). Из 148 наступивших клинических беременностей только 95 закончились родами живыми детьми (64,2%). Таким образом, репродуктивные потери составили, 35,8%, преимущественно за счет невынашивания беременности в первом триместре (29,9%). Эктопическая беременность наступила в 7 случаях (4,6%).
Учитывая, что невынашивание беременности у пациенток с ХЭ значительно снижает конечную результативность программ ВРТ, важно выявить факторы, взаимосвязанные с этими осложнениями, и определить, совпадают ли эти факторы с причинами многократных неудач ЭКО/ИКСИ.
Для решения этой задачи проведен сравнительный анализ выделенных трех групп по 200 параметрам, отражающих клинические и параклинические характеристики пациенток.
При анализе социального статуса выявлено, что каждая пятая женщина в группе с невынашиванием являлась индивидуальным предпринимателем (19,5%), тогда как среди родивших детей и пациенток с неудачами ЭКО/ИКСИ только 7,2% и 4,2% соответственно (χ2=8,15; р=0,017, df=2).
Пациентки трех групп были идентичны по возрасту, характеристикам менструальной функции, возрасту начала половой жизни.
Длительность бесплодия в исследуемых группах была идентичной. Как показано на рис. 1, в структуре факторов бесплодия у пациенток с неудачами и невынашиванием после ЭКО/ИКСИ имелась тенденция к преобладанию мужского фактора, а женщины, родившие детей с первой или второй попытки, несколько чаще страдали трубным бесплодием. Различия статистически незначимы.
Первичный характер бесплодия отмечен более, чем у половины пациенток с неудачами ЭКО/ИКСИ - 59,7%, и лишь у каждой третьей женщины среди родивших или страдающих невынашиванием беременности - 34,9% и 34,1% соответственно (χ2=12,74; р=0,002, df=2).
При анализе соматической патологии выявлено, что пациентки с невынашиванием чаще страдали заболеваниями легких, желудочно-кишечного тракта и реже – ожирением и избыточной массой тела. У родивших женщин реже, чем у пациенток с невынашиванием и неудачами ЭКО/ИКСИ встречались заболевания легких, ЛОР-органов и мочевыделительной системы. Различия статистически значимы только в отношении заболеваний легких (рис. 2).
При этом такие экстрагенитальные воспалительные заболевания, как хронический пиелонефрит, тонзиллит, бронхит, вдвое чаще встречались у пациенток с неудачами ЭКО/ИКСИ и невынашиванием (38,9% и 46,3% соответственно), чем у родивших женщин (14,5%; χ2=17,4; р<0,001; df=2).
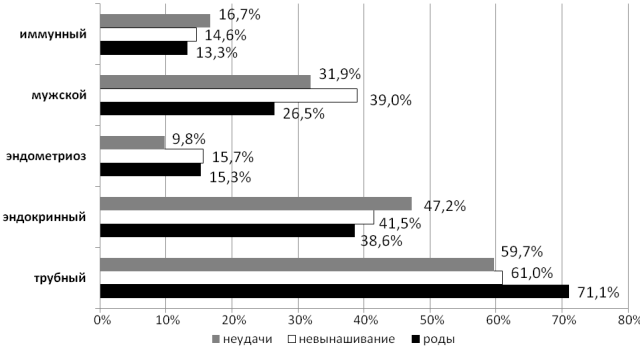
Рис. 1. Структура факторов бесплодия у пациенток с ХЭ в зависимости от исходов циклов ЭКО/ИКСИ
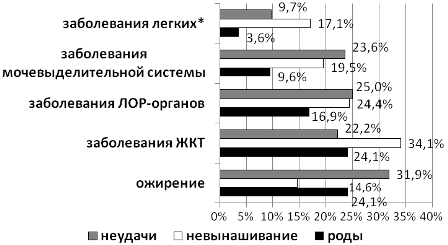
Рис. 2. Соматическая патология пациенток с ХЭ в зависимости от исходов циклов ЭКО/ИКСИ:* χ2=6,4; р=0,040; df=2
Различные варианты гормональных нарушений в целом в два раза чаще выявлялись у пациенток с невынашиванием после ЭКО/ИКСИ (36,6%), чем у женщин с неудачами и родами (15,3% и 14,5% соответственно, χ2=9,8; р=0,007; df=2).
Отмечена четкая тенденция к большей частоте аденомиоза, аномалий развития матки, синехиями среди пациенток с невынашиванием после ЭКО/ИКСИ (рис. 4).
В целом, такие варианты патологии матки, как гипоплазия и аномалии развития матки, аденомиоз, синехии, встречались у 8,4% родивших женщин, у 18,1% пациенток с неудачами ЭКО/ИКСИ и в 43,9% случаев в группе с невынашиванием беременности (χ2=22,2; р<0,001; df=2). Доля пациенток с миомой матки и полипами эндометрия в исследуемых группах была одинаковой, с тенденцией к более частому выявлению полипов эндометрия в группе женщин с неудачами ЭКО/ИКСИ.
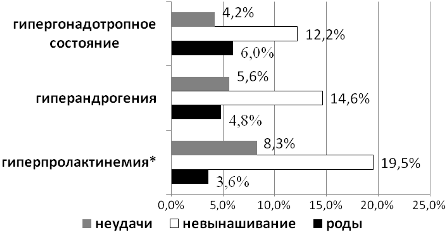
Рис. 3. Гормональные нарушения у пациенток с ХЭ в зависимости от исходов циклов ЭКО/ИКСИ:* χ2=8,7; р=0,012; df=2
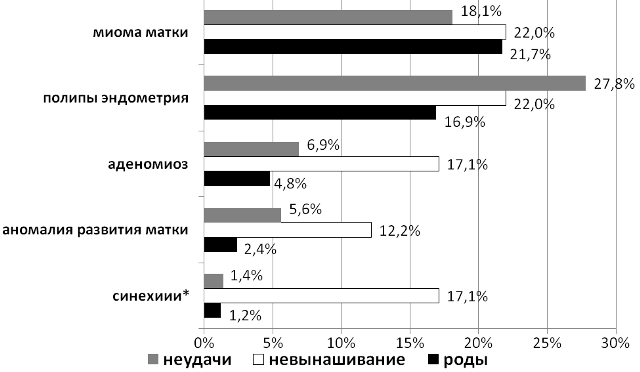
Рис. 4. Маточный фактор у пациенток с ХЭ в зависимости от исходов циклов ЭКО/ИКСИ:* χ2=18,4; р<0,001; df=2
При анализе частоты родов после ЭКО/ИКСИ важна не простая констатация фактов, но и выяснение факторов, которые, возможно, оказывают на это влияние. Для решения этой задачи, описанные выше состояния, взаимосвязанные с меньшей вероятностью родов после ЭКО/ИКСИ, оценены при помощи лог-рангового критерия Мантеля-Кокса (χ2). Количество пациенток с ХЭ и вероятность рождения живого ребенка в зависимости от порядкового номера переноса эмбрионов представлены в табл. 1.
Одной из характеристик кривых Каплана-Майера является медиана, что в данном случае обозначает количество переносов эмбрионов, в результате которого половина пациенток родит живых детей. Медиана количества переносов у женщин с вторичным бесплодием равна трем, тогда как определить данный показатель для пациенток с первичным бесплодием невозможно, поскольку общая частота родов в этой группе при имеющемся количестве переносов эмбрионов (шесть) не достигает 50% (рис. 5). Таким образом, суммарная частота родов после ЭКО/ИКСИ при вторичном бесплодии выше, чем при первичном, различие статистически значимо (χ2=5,66, р=0,017).
Таблица 1. Сводка оценок Каплана-Майера для выборки из 267 пациенток
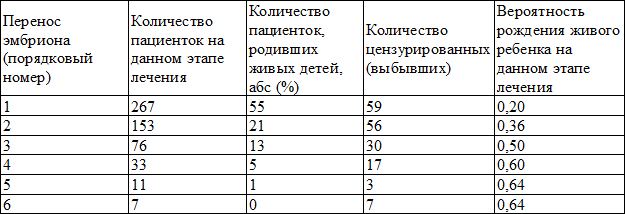
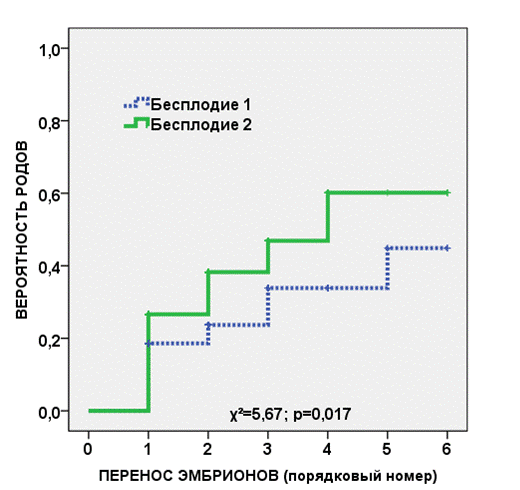
Рис. 5. Кривая Каплана-Майера, показывающая вероятность родов у пациенток с ХЭ и первичным бесплодием по сравнению с вторичным в зависимости от количества переносов
Аналогичные кривые для других факторов, значимо влияющих на общую частоту родов у пациенток с ХЭ, приведены на рис. 6-9.
При наличии мужского фактора бесплодия (рисунок 6) у пациенток исследуемой группы общая частота родов после ЭКО/ИКСИ не превышала 30%, даже с учетом повторных переносов эмбриона (χ2=4,34, р=0,038).
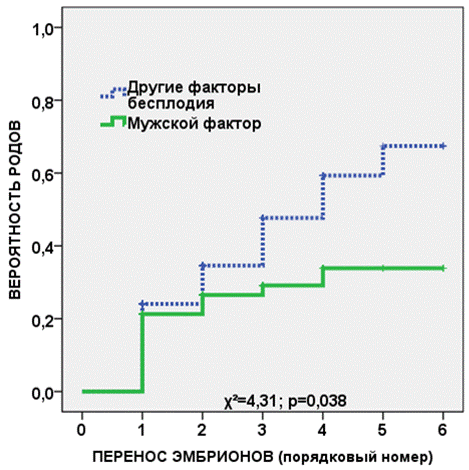
Рис. 6. Кривая Каплана-Майера, показывающая вероятность родов у пациенток с ХЭ и мужским фактором бесплодием по сравнению с другими в зависимости от количества переносов
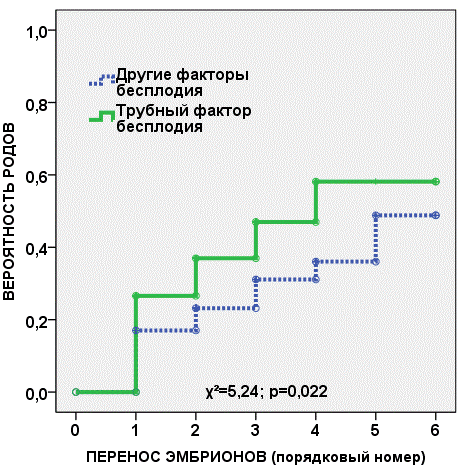
Рис. 7. Кривая Каплана-Майера, показывающая вероятность родов у пациенток с ХЭ и трубным фактором бесплодием по сравнению с другими в зависимости от количества переносов
Тогда как наличие трубного фактора бесплодия (рис. 7) было прогностически благоприятным по сравнению с другими этиологическими факторами бесплодия (χ2=5,24, р=0,022).
Статистически значимыми негативными предикторами родов являлись хронические воспалительные заболевания – хронический пиелонефрит, тонзиллит, бронхит (χ2=10,1, р=0,001) и такие варианты патологии матки как гипоплазия и аномалии развития матки, аденомиоз, синехии (χ2=8,0, р=0,005). Наличие очагов хронической инфекции или вышеуказанной патологии матки уже при первом переносе эмбрионов уменьшало частоту родов в два раза (рис. 8,9).
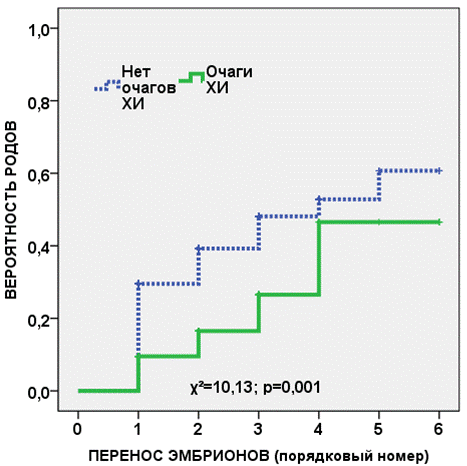
Рис. 8. Кривая Каплана-Майера, показывающая вероятность родов у пациенток с ХЭ и экстрагенитальными очагами хронической инфекции (ХИ) в сравнении с их отсутствием в зависимости от количества переносов
Обсуждение. Главной целью лечения бесплодия, в том числе методами ВРТ, является рождение ребенка. Доля родов живыми детьми после первой попытки переноса эмбрионов составляет в России не более 19-21% [2]. Однако неудача первой попытки не означает полной неэффективности программ ВРТ, беременность может наступить после криопереноса или при переносе вновь полученных эмбрионов в следующем цикле стимуляции. Так, у пациенток с ХЭ после первой попытки только в 20% случаев родились жизнеспособные дети, после второй – в 36%, после третьей – в 50%, после четвертой – в 60%, после пятой – в 64%. Таким образом, общая частота родов живыми у данной категории пациенток составила 64%.
Неэффективность ВРТ в буквальном смысле, т.е. отсутствие родов живым ребенком, обусловлены как неудачами имплантации, так и встречающемся при каждой третьей беременности после ЭКО/ИКСИ невынашиванием, предикторы которых не являются абсолютно идентичными. Негативно влияют и на имплантацию и на формирование плаценты, повышая риск невынашивания, экстрагенитальные очаги хронической инфекции (пиелонефрит, тонзиллит, воспалительные заболевания легких). В патогенезе этих заболеваний, а также и хронического эндометрита, имеет значение нарушение защитных механизмов на уровне иммунной системы слизистых оболочек, обеспечивающих быструю локализацию инфекционного процесса и снижающих повреждение тканей при развитии воспалительных реакций. Экстрагенитальные хронические воспалительные заболевания выявлялись почти у половины пациенток с невынашиванием беременности (46,3%), у каждой третьей при неудачах имплантации (38,9%) и лишь у 14,5% женщин, родивших детей после первого или второго переноса эмбрионов (χ2=17,4; р<0,001; df=2).
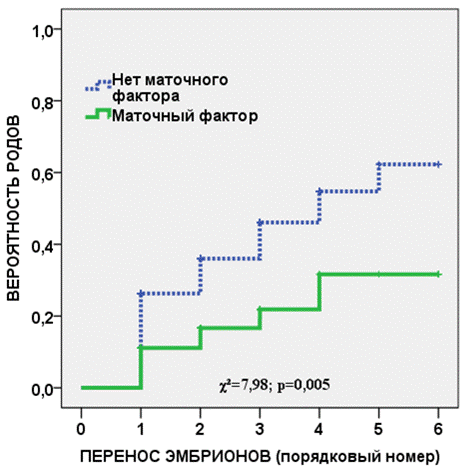
Рис. 9. Кривая Каплана-Майера, показывающая вероятность родов у пациенток с ХЭ и патологией матки в сравнении с её отсутствием в зависимости от количества переносов
Мужской фактор бесплодия также можно рассматривать как общий предиктор неудач имплантации и невынашивания, а первичное бесплодие ассоциировано преимущественно с неудачами имплантации. Можно предположить, что эти факторы скорее взаимосвязаны с генетическими, чем с эпигенетическими особенностями половых клеток, процессами оплодотворения и имплантации. Они полиэтиологичны по своей природе, менее изучены и в настоящее время наиболее сложно поддаются коррекции.
Такие варианты патологии матки, как аномалии развития матки, аденомиоз, синехии, являются негативными предикторами родов после ЭКО/ИКСИ вследствие их высокой частоты (43,9%) у пациенток с невынашиванием беременности и минимальной (8,4%) в группе женщин, родивших детей после первого и второго переноса эмбрионов. Терапевтические подходы в отношении данных заболеваний на современном этапе в разной степени разработаны, продолжаются исследования наиболее эффективных способов их коррекции у пациенток, планирующих программы ВРТ.
Примечателен также тот факт, что гормональные нарушения (гиперпролактинемия, гиперандрогения, гипергонадотропное состояние) встречались у каждой третьей пациентки (36,6%) с невынашиванием беременности, тогда как при неудачах имплантации и у родивших женщин лишь в 15,3% и 14,5% соответственно. Меньшая частота этих нарушений при неудачах имплантации, идентичная с таковой у женщин, беременность которых завершилась родами, чем при невынашивании, может говорить о том, что гормональные нарушения мало препятствуют получению зрелых ооцитов в результате медикаментозной стимуляции и даже эмбрионов, способных к имплантации. Однако, нарушение формирования желтого тела, инвазии трофобласта с формированием полноценной плаценты на последующих этапах приводят к отторжению плодного яйца. Влияние социального статуса и особенностей образа жизни на эффективность лечения бесплодия, в том числе методами ВРТ, является мало изученной проблемой. При анализе рода профессиональной деятельности в исследуемой группе выявлена более высокая частота индивидуальных предпринимателей среди пациенток с невынашиванием. Можно предположить, что данная социальная группа наиболее подвержена хроническому психоэмоциональному стрессу, механизм влияния которого на репродуктивную функцию также в значительной степени реализуется через эндокринные механизмы.
Таким образом, изучение предикторов родов и возможных механизмов их действия, является важным как для консультирования пациенток, вступающих в программы ВРТ, и для выработки наиболее оптимальной стратегии прегравидарной подготовки врачами репродуктологами.
Выводы:
1. Общая частота родов живыми детьми в результате шести попыток переноса эмбрионов в программах ЭКО/ИКСИ у пациенток с хроническим эндометритом составляет 64,2%.
2. Негативными предикторами родов после ЭКО/ИКСИ являются: первичный характер бесплодия, мужской фактор бесплодия, патология матки (гипоплазия и аномалии развития матки, аденомиоз, синехии), экстрагенитальные хронические воспалительные заболевания (хронический пиелонефрит, тонзиллит, бронхит).
3. Трубный фактор бесплодия является позитивным предиктором родов.
