На сегодняшний день значительной проблемой репродуктивного здоровья является миома матки, которая встречается у 20% женщин до 35 лет, при этом у 30% пациенток репродуктивного возраста миома матки ассоциирована с бесплодием, невынашиванием и другими неблагоприятными исходами беременности [1, 2, 5, 12-15]. Учитывая сложившуюся в России демографическую ситуацию, не потеряло своей актуальности высказывание великого русского ученого М.В. Ломоносова в письме И.И. Шувалову «О сохранении и размножении российского народа» (1761 г.): «Начало сего полагаю самым главным делом: сохранением и размножением российского народа, в чем состоит величество, могущество и богатство всего государства, а не в обширности, тщетной без обитателей» [3].
В настоящее время приоритетным направлением в лечения женщин репродуктивного возраста с миомой матки является органосохраняющая функциональная хирургия с применением классических хирургических доступов - лапароскопического и лапаротомического. Влагалищная консервативная миомэктомия – один из возможных способов лечения, однако, на сегодняшний день он не получил широкого распространения, чему есть объективные причины, такие как сложность овладения навыками техники влагалищной хирургии, отсутствие алгоритма дифференцированного выбора доступа при выполнении консервативной миомэктомии, недостаточное количество данных об отдалённых результатах данной операции. Кроме того, крайне мало изучено влияние влагалищной консервативной миомэктомии на показатели репродуктивного здоровья женщины, в том числе и в сравнении с классическими оперативными доступами. Всё это повышает интерес к дальнейшему изучению и разработке тактики хирургического лечения при выполнении консервативной миомэктомии у женщин репродуктивного возраста.
Материалы и методы. В настоящее время на кафедре акушерства и гинекологии имени С.Н. Давыдова, на базе гинекологического отделения СПб ГБУЗ «Городская больница №40», г. Санкт-Петербург, мы проводим ретро- и проспективное когортное исследование, целью которого является повышение эффективности лечения женщин репродуктивного возраста с миомой матки. На данном этапе были проанализированы клинические данные 61 пациентки в возрасте 34,16±5,17 лет (23 - 43 года) с субсерозной и интрамурально-субсерозной формой миомы матки, размерами доминантного узла 4-9 см., расположенного по задней стенке и в дне матки. Характеристика узлов представлена в таблице 1.
Таблица 1. Характеристика миоматозных узлов
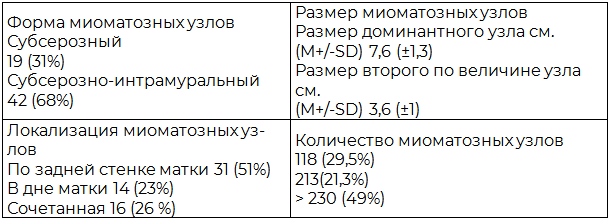
В зависимости от оперативного доступа пациентки были разделены на три группы. Первую (основную) группу составили 18, вторую и третью (группы сравнения) - 24 и 19 пациенток. Больным основной группы была выполнена влагалищная консервативная миомэктомия. Пациенткам из групп сравнения – лапароскопическая и лапаротомическая консервативная миомэктомия соответственно. Показанием к оперативному лечению служили быстрый рост узлов, менометроррагия, привычное невынашивание беременности и бесплодие (при исключении других причин), а также отсутствие эффекта от проводимой консервативной терапии. Группы были сопоставимы по возрасту, акушерско-гинекологическому и соматическому анамнезу женщин. Характеристика миоматозных узлов (форма, размер, локализация, количество) была идентичной в трёх группах. Все пациентки дали письменное информированное согласие на участие в исследовании, которое было одобрено локальным этическим комитетом. Единственной жалобой у 16 (26%) пациенток являлось отсутствие беременности на протяжении 1-10 лет регулярной половой жизни. Первичное бесплодие было выявлено у 17 (27,8%) женщин, вторичное - у 5 (8%), привычное невынашивание беременности - у 6 (9,8%) пациенток. Боли в нижних отделах живота отмечали 8 (13%) женщин. Нарушение менструального цикла по типу меноррагии и альгодисменореи установлено у 27 (44%) пациенток. Быстрый рост узла миомы наблюдался у 11 (18%) обследованных женщин. У большинства женщин (у 44 (72%)) было отмечено сочетание вышеперечисленных симптомов. Сопутствующая гинекологическая патология была диагностирована у 7 (11%) больных в исследуемых группах, экстрагенитальная патология - у 19 (31%) пациенток. Внутриполостные вмешательства имели место в анамнезе у 9 (14,7%) женщин, операции на органах малого таза у 4 (6,5%) пациенток. По поводу рецидива миомы матки обратились 3 (5%) женщины. Родоразрешение путём операции Кесарева сечения было в анамнезе у 3 (5%) женщин. С целью уменьшения размеров миоматозных узлов, в течение трёх месяцев до оперативного лечения 6 (9,8%) пациенток получали терапию агонистами гонадотропин-рилизинг гормона (аГнРГ) и 5 (8%) женщинам была выполнена предоперационная эмболизация маточных артерий рассасывающимися материалами. В ходе исследования проведена оценка анамнестических и клинических данных. Определены стандартные показатели оперативного вмешательства и течения послеоперационного периода (объём кровопотери, длительность оперативного вмешательства, интенсивность болевых ощущений в раннем послеоперационном периоде при помощи визуально-аналоговой шкалы (ВАШ), количество дней потребления анальгетиков, наличие интраоперационных и послеоперационных осложнений, величина и длительность температуры в послеоперационном периоде, продолжительность госпитализации). Оценка объёма интраоперационной кровопотери была осуществлена при помощи гравиметрической методики, подсчёта количества излившейся крови в аспираторе, оценки показателей гемоглобина и гематокрита до и после оперативного лечения. Помимо общепринятого клинического обследования, было выполнено ультразвуковое исследование (УЗИ) органов малого таза на 5-е сутки послеоперационного периода на аппарате НITACHI c цветным допплеровским картированием. Статистическая обработка полученных результатов проведена с использованием электронных таблиц "Microsoft Excel", пакета статистических программ SAS 9,3. Количественные переменные представлены в виде среднего арифметического и его стандартного отклонения (M +/- SD). Для сравнения показателей применялся t критерий Стьюдента.
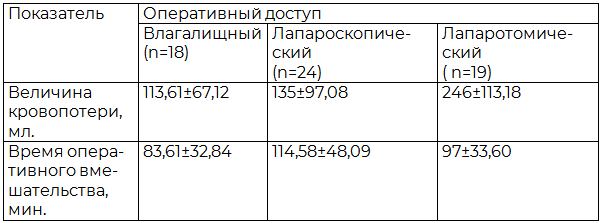
Результаты. Течение операционного периода. Как видно из табл. 2, наименьшая величина кровопотери наблюдалась в основной группе и составила 113,61±67,12 мл. В группе пациенток, которым органосохраняющая операция была выполнена лапароскопическим доступом, объём кровопотери составил 135±97,08 мл. Однако статистически достоверных различий между двумя группами по вышеуказанному показателю выявлено не было (p>0,05). Кровопотеря в группе женщин, получивших оперативное лечение лапаротомическим доступом, составила 246±113,18 мл и была достоверно выше в сравнении с обеими группами (p=0,0001). Гемотрансфузия у пациенток из основной группы не проводилась. В контрольных группах, где консервативная миомэктомия была выполнена лапароскопическим и лапаротомическим доступом, гемотрансфузия была выполнена в 3 (12,5%) и 4 (21%) случаях соответственно. Было зарегистрировано статистически достоверное снижение гемоглобина и гематокрита в послеоперационном периоде у пациенток, которые были прооперированы лапаротомическим доступом (p<0,05) при сравнении показателей клинического анализа крови в пред и послеоперационном периоде. При анализе времени оперативного вмешательства не было выявлено статистически достоверных различий между основной группой и группой пациенток, которым консервативная миомэктомия была выполнена лапаротомическим доступом, она составила 83,61±32,84 мин. и 97±33,60 мин. соответственно (p>0,05). Тогда как этот показатель был 114,58±48,09 мин. при выполнении операции лапароскопическим доступом, что достоверно выше в сравнении с основной группой (p=0,01).
Таблица 2. Сравнительная оценка показателей интраоперационного периода
Течение послеоперационного периода. Повышение температуры тела в послеоперационном периоде было отмечено у 5 (28%) больных, которым консервативная миомэктомия была выполнена влагалищным доступом. В контрольных группах, где оперативное лечение проведено лапароскопическим и лапаротомическим доступом, повышение температуры было отмечено у 4(16%) и 7 (36%) пациенток соответственно; длительность лихорадки составила 3,2±1,16 дня в основной группе, 3,8±1,5 дня и 2,12±1,3 дня в контрольных группах соответственно. Таким образом, в группе пациенток, которым оперативное лечение было проведено лапароскопическим доступом, данный показатель был самым низким. Ни в одной из исследуемых групп температура не превышала 37,8°C. Вышеуказанные данные приведены на рис. 1.
Рис. 1. Повышение температуры тела после консервативной миомэктомии.
Как представлено на рис. 2, применение анальгетиков в первые сутки послеоперационного периода было необходимо всем больным. Потребность в применении анальгетиков сохранялась в течение четырёх суток в группах пациенток, которым консервативная миомэктомия была выполнена влагалищным и лапароскопическим доступом. В группе женщин, получивших оперативное лечение лапаротомическим доступом, необходимость в применении анальгетиков сохранялась в течение семи суток. При оценке интенсивности болевых ощущений в послеоперационном периоде по визуально-аналоговой шкале (ВАШ), не было выявлено статистически достоверных различий между группой женщин, которым консервативная миомэктомия была выполнена влагалищным и лапароскопическим доступом, она составила 3,5±0,9 в основной и 3,3±1,3 в контрольной группе (p>0,05). В группе пациенток, которым была выполнена лапаротомическая консервативная миомэктомия, этот показатель был достоверно выше по сравнению с обеими группами и составил 4,7±1,3 (p<0,05). Длительность госпитализации составила 4,6±1,14 дня в основной группе, 4,8±0,79 дня и 6,35±1,2 дня в группе женщин оперированных лапароскопическим и лапаротомическим доступом соответственно, но достоверных различий по количеству дней госпитализации между тремя исследуемыми группами выявлено не было (p>0,05).
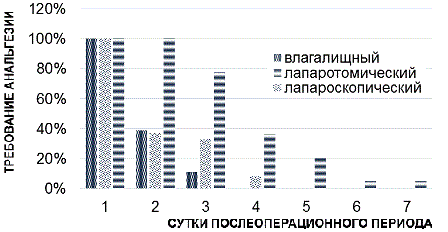
Рис. 2. Потребность в применении анальгетиков после консервативной миомэктомии.
Осложнения. На пятые сутки послеоперационного периода пациенткам было выполнено УЗИ органов малого таза на аппарате HITACHI, по результатам которого не было зафиксировано случаев возникновения абсцесса или гематомы Дугласова пространства. Так же ни в одном случае не было выявлено изменений в структуре послеоперационного рубца, в частности, деформации, ниш, участков втяжения, и жидкостных включений. В основной группе пациенток имело место одно осложнение - интраоперационное ранение петель тонкого кишечника, которое произошло у нерожавшей пациентки в возрасте 30 лет во время удаления миоматозного узла через передний кольпотомический доступ. Из особенностей анамнеза следует отметить, что это был рецидив миомы матки (ранее выполнена консервативная миомэктомия лапароскопическим доступом 6 лет назад). Показанием к операции служили быстрый рост миоматозных узлов, менометроррагия, первичное бесплодие. До операции, с целью уточнения локализации узлов, пациентке была проведена магнитно-резонансная томография (МРТ) малого таза. Во время оперативного вмешательства было обнаружено четыре интрамурально-субсерозных узла с максимальным диаметром доминантного узла 9 см. и размерами второго по величине узла – 4 см. Доминантный узел был расположен в дне матки, другие узлы были локализованы по передней стенке матки. Также следует отметить выраженный спаечный процесс органов малого таза. В ходе операции было выполнено ушивание стенки кишечника двойным эндошвом. Послеоперационный период протекал удовлетворительно.
Обсуждение. Исходя из предварительных данных нашего исследования, влагалищная консервативная миомэктомия обладает теми же преимуществами с точки зрения низкой величины кровопотери и малой травматичности метода, что и лапароскопическая консервативная миомэктомия. Тогда как существенным недостатком лапаротомической консервативной миомэктомии стала высокая величина кровопотери. В литературных источниках есть два сообщения о сравнительной оценке объёма кровопотери при влагалищной и лапаратомической консервативной миомэктомии, в которых авторы также указали на меньшую величину кровопотери в группе женщин, которым оперативное лечение было выполнено влагалищным доступом. Однако, в исследовании Wei FH et al. (2006) статистически достоверных различий по величине кровопотери выявлено не было (p>0,05) [4,16]. Предварительная оценка времени оперативного вмешательства показала, что длительность операции была меньше при выполнении консервативной миомэктомии влагалищным и лапаротомическим доступом. Сравнительная оценка длительности оперативного вмешательства была представлена в исследовании Zhang J et al. (2006). Данный показатель составил 76±21 мин. в группе женщин, оперированных влагалищным доступом, и 72±26 мин. в группе пациенток, которым консервативная миомэктомия была проведена лапаротомическим доступом. Статистически достоверных различий выявлено не было (p>0,05) [17]. В проспективном исследовании Birsan A et al. (2003) показано преимущество влагалищной консервативной миомэктомии по длительности оперативного вмешательства - 96±38 мин. при влагалищном доступе и 166±78 мин. при лапароскопическом доступе соответственно [9]. По предварительным данным нашего исследования, период восстановления после консервативной миомэктомии был короче у пациенток, которым оперативное лечение было выполнено лапароскопическим и влагалищным доступом. В этих группах было показано преимущество по таким показателям, как короткий период потребление анальгетиков, невыраженная болевая симптоматика в послеоперационном периоде и небольшая длительность госпитализации в сравнении с группой женщин, которым была проведена лапаротомическая консервативная миомэктомия. Следует отметить, что лапароскопический доступ показал преимущество и по малой длительности послеоперационной лихорадки в сравнении с влагалищным и лапаротомическим доступом. В зарубежной литературе есть единичные исследования, посвящённые оценке течения раннего послеоперационного периода у пациенток, которым консервативная миомэктомия была выполнена влагалищным доступом, в сравнении с лапаротомическим и/или лапароскопическим доступами. В исследовании Plotti G и et al. (2008) авторы указывают на более короткий период потребления наркотических анальгетиков (морфина) в группе женщин, которым консервативная миомэктомия была выполнена влагалищным доступом, в сравнении с группой пациенток, в которой консервативная миомэктомия была проведена лапароскопическим доступом. Однако, как и в нашем исследовании, авторы также не получили статистически достоверных различий по длительности госпитализации между двумя группами: 4.0±1.0 дней – при влагалищном доступе и 4,1±1,5 дней при лапароскопическом доступе [12]. В проспективном исследовании Zhang J (2006) проведено сравнение показателей консервативной миомэктомии, выполненной влагалищным доступом (основная группа) и лапаротомическим доступом (контрольная группа). Длительность госпитализации составила 4,8±0,6 дней в основной и 7,8±0,4 дней в контрольной группе [17]. Исходя из предварительных данных, можно предположить, что влагалищный доступ, как и лапароскопический, является малоинвазивным, имеет короткий период восстановления и не требует длительного применения анальгетиков. Напротив, лапаротомический доступ в сравнении с влагалищным доступом, исходя из результатов нашего исследования и единичных сообщений в мировой литературе, более травматичен и хуже переносится больными. С целью оценки безопасности влагалищной консервативной миомэктомии, нами были проанализированы сообщения об осложнениях, возникших в ходе операции, а также диагностированные в послеоперационном периоде. В нашем исследовании мы указали на случай интраоперационного ранения тонкого кишечника, который потребовал конверсии на лапароскопию у пациентки с выраженным спаечным процессом малого таза и размерами матки 13/14 недель беременности. Сообщения о ранении кишечника при выполнении консервативной миомэктомии есть и в зарубежной литературе [7, 8], но, вследствие малого количества опубликованных данных, не представляется возможным оценить частоту, а, следовательно, и риск возникновения данного осложнения. Наиболее частые осложнения, описанные в мировой литературе, которые можно считать специфичными для влагалищной консервативной миомэктомии, - послеоперационная гематома и абсцесс Дугласова пространства [4, 7, 10]. В нашем исследовании таких осложнений не было, что подтверждено данными трансвагинального ультразвукового исследования, выполненного на пятые сутки послеоперационного периода всем пациенткам. Обобщая мировой и собственный опыт, можно предположить, что влагалищная консервативная миомэктомия со временем может занять собственную нишу в органосохраняющем лечении женщин с миомой матки. Исследование и набор материала продолжаются, требует уточнения состояние репродуктивной, менструальной функции, отдалённые результаты влагалищной консервативной миомэктомии. Следует отметить, что данный вопрос крайне мало освещён как в отечественной, так и в зарубежной литературе, имеющиеся сведения носят отрывочный и противоречивый характер, что делает актуальным его дальнейшее углублённое изучение.
