На сегодняшний день актуальным является создание высокоэффективных отечественных методов ранней диагностики альтерации функций организма, тяжести патологических состояний и контроля эффективности проводимого лечения. Пути решения этой проблемы идут в направлении изучения патофизиологических реакций клеточных систем, которые являются исходным звеном развития патологического процесса. Одной из таких клеточных систем может быть кровь и электрофоретическая подвижность ее форменных элементов, в частности, эритроцитов.
Электрофоретическая подвижность эритроцитов (ЭФПЭ) относится к числу интегральных показателей мембранных функций эритроцитов и активности их метаболизма, что отражает состояние не только отдельных клеток, но и организма в целом.
Снижение ЭФПЭ определяет повышение агрегабельности эритроцитов, их прокоагулянтной активности, приводит к нарушению реологических свойств крови, изменяет вязкость и структуру крови, что приводит к развитию тканевой гипоксии [1, 2].
Установлены корреляции изменения ЭФПЭ крови у больных при различных видах патологии органов и систем организма: отмечено ее снижении при самых разных заболеваниях [3-5].
Ранее нами показана однонаправленность изменения ЭФПЭ не только при патологии, но и при различных экстремальных воздействиях на организм [6, 7].
Доказано, что изменение ЭФПЭ является отражением общей неспецифической реакции организма на раздражитель, и связана с развитием стресс-реакции и вовлечением стресс-реализующих систем на действие чрезвычайных раздражителей.
Учитывая, что в основе многих патологических процессов и чрезвычайных раздражителей лежит развитие разной степени выраженности стресса можно предположить, что анализ ЭФПЭ крови может служить достаточно убедительным маркером идущего в организме патологического процесса.
Однако целесообразность использования ЭФПЭ по сравнению со стандартными клиническими анализами крови при различных патологических процессах на сегодняшний день не изучалась.
Целью работы являлось изучение взаимосвязи электрофоретической подвижности эритроцитов со стандартными клиническими показателями крови больных с различными видами заболеваний в ходе проведения терапевтических мероприятий и обоснования возможности использования ЭФПЭ в качестве прогностического показателя эффективности терапии.
Материалы и методы. В работе был проведен анализ крови пациентов с сердечно-сосудистыми (острый инфаркт миокарда, артериальная гипертония, стенокардия, миокардит, сердечная недостаточность), бронхо-легочными (хроническая обструктивная болезнь лёгких, острый бронхит, острая внебольничная пневмония), гинекологическими (угроза выкидыша, обострение хронического эндомерита, диструктиментальное маточное кровотечение), гастроэнтерологическими заболеваниями (язвенная болезнь желудка, холецестит, острый гастрит, острый панкреатит) (по 20 пациентов в каждой группе).
Диагноз формулировался врачом в соответствии с общепринятыми клиническими критериями, на основании собранного анамнеза, и подтверждался лабораторными и клиническими исследованиями. Лечение больных включало проведение стандартных терапевтических мероприятий.
Исследование ЭФПЭ и клинический анализ крови проводили при поступлении пациентов в стационар до начала и после проведения терапевтических мероприятий. Измерение ЭФПЭ производили методом микроэлектрофореза [8].
В день определения ЭФПЭ готовили взвесь эритроцитов и использовали ее для измерения ЭФП отмытых эритроцитов. Отмытые эритроциты получали трехкратным центрифугированием при 1500 об/мин в течение 10 минут с 0,9% раствором хлористого натрия. Суспензию клеток разводили в 10 мМ трис НСl буфере (рН 7,4) и измеряли ЭФПЭ метод микроэлектрофореза в горизонтальной микрокамере при силе тока 12-15 мА.
Исследование лабораторно-клинических показателей крови (исследование количества гемоглобина, общего количества эритроцитов, лейкоцитов, СОЭ) проводили стандартными клиническими методами [9].
Результаты исследований статистически обрабатывались с использованием описательной статистики и t-критерия Стьюдента. Обработка данных осуществлялась с помощью программы «Biostat». За величину уровня статистической значимости различий принимали p≤0,05.
Результаты и обсуждение. Исследование клинико-лабораторных показателей крови и ЭФПЭ больных выявило их значимое изменение в ходе проводимой терапии при всех исследуемых видах патологий (табл. 1-4). Так, у пациентов с сердечно - сосудистыми заболеваниями статистически значимо изменялось общее количество лейкоцитов в крови на 10% относительно уровня показателя до лечения. Скорость оседания эритроцитов (СОЭ) уменьшалась на 19% после проведения терапии, при этом регистрировалось увеличение ЭФПЭ крови на 40% (табл. 1).
Таблица 1. Изменение клинико-лабораторных показателей крови и электрофоретической подвижности эритроцитов у больных сердечно-сосудистыми заболеваниями

Примечание: здесь и далее * - p≤0,05 по отношению к уровню данных показателей до лечения.
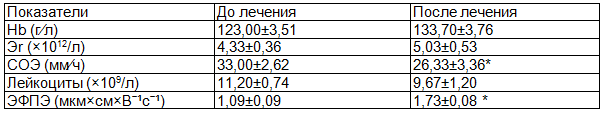
Результаты исследования крови пациентов с пульмонологическими заболеваниями выявили снижение СОЭ на 21% (р≤0,05), уменьшение количества лейкоцитов на 14% и увеличение ЭФПЭ на 58% относительно исходного уровня данных показателей (табл. 2).
Таблица 2. Изменение клинико-лабораторных показателей крови и электрофоретической подвижности эритроцитов больных пульмонологическими заболеваниями
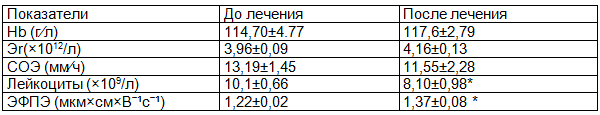
В результате исследований пациентов с гинекологическими заболеваниями было выявлено увеличение содержания гемоглобина на 13% (p≤0,05), общего количества эритроцитов на 8% и снижение количества лейкоцитов на 11% относительно показателей до лечения.
СОЭ после проведенной терапии при данной патологии изменялось на 13% (p≤0,05), ЭФПЭ на 34% относительно значений до лечения (табл. 3).
Таблица 3. Изменение клинико-лабораторных показателей крови и электрофоретической подвижности эритроцитов больных гинекологическими заболеваниями

В результате исследования крови больных гастроэнтерологическими заболеваниями было выявлено, что после проведённого лечения отмечалось уменьшение количества лейкоцитов, что составило 80% (p≤0,05) относительно исходного уровня показателя до лечения.
СОЭ имела тенденцию к снижению, тогда как ЭФПЭ статистически значимо увеличивалась на 12% после терапевтических мероприятий (табл. 4).
Таблица 4. Изменение клинико-лабораторных показателей крови и электрофоретической подвижности эритроцитов больных гастроэнтерологическими заболеваниями
Результаты анализа изменения ЭФПЭ при исследуемых видах патологии относительно нормы (1,30-1,75 мкм×см×Вˉ¹сˉ¹) свидетельствуют об однонаправленном ее снижении независимо от этиологиии патологического процесса и ее увеличении в ходе проводимой терапии.
Как следует из приведенных результатов, изменение данного параметра эритроцитов сочетается с направленностью изменений общего количества лейкоцитов и СОЭ. Однако выраженность ЭФПЭ в количественном отношении существенно превышает изменения содержания лейкоцитов и СОЭ, вариация признака которых не всегда носит статистически значимый характер.
Кроме того, СОЭ, являясь торпидным показателем, в ходе воспаления и проводимой терапии изменяется в ряде случаев длительно и не всегда позволяет оценить интенсивность патологического процесса и эффективность проводимой терапии.
Так, в наших исследованиях не выявлено статистически значимых изменений индекса при сердечно-сосудистых и гастроэнтерологических заболеваниях. При этом отмеченные значимые изменения количества лейкоцитов при данных заболеваниях свидетельствуют о снижении патологического процесса.
Механизм изменения ЭФПЭ не зависимо от этиологии заболевания, носит, по всей видимости, типовой характер, что обусловлено, вероятно, стереотипными изменениями, происходящими в мембране и метаболизме клеток при любой альтерации функций организма.
В частности, показано, что при стрессе и различных патологиях в эритроцитарной мембране изменяется фосфолипидный состав: уменьшается содержание фосфатидилхолина, фософатидилэтаноламина, увеличивается доля лизоформ, при этом повышается уровень холестерина и изменяется их трансмембранная асимметрия, мембрана эритроцита теряет эластичность [10, 11].
Липидные молекулы, являясь важными структурными и функциональными компонентами мембран эритроцитов, регулируют подвижность и активность липидзависимых ферментов и внутримембранных белков, тем самым обеспечивая в клетке селективную проницаемость и нормальное функционирование мембранассоциированных ферментов, а также рецепторного аппарата [12].
В частности, изменяется активность Na,К-АТФазы, ингибируются ферменты, участвующие в метаболизме клеток, что нарушает процесс обмена веществ [11, 13].
Угнетение активности Na-K-АТФазы приводит к увеличению концентрации внутриклеточного Са2+ [14, 15]. Поступление избыточного количества Са2+ сопровождается изменением функций клетки и их формы [16].
Увеличение внутриклеточного кальция вызывает образование эхиноцитов, анактоцитов, стоматоцитов [17]. Изменение формы приводит к модификации поверхностного заряда.
При этом следует полагать, что перечисленные изменения носят обратимый характер. В частности показано, что изменения формы обратимы и связаны с уменьшением концентрации Са2+. При этом защита эритроцита от Са2+перегрузки определяется активацией Са-АТФазой [18].
Таким образом, эритроциты не ограничиваются функцией переноса кислорода и углекислого газа, а посредством чрезвычайно активной мембраны принимают участие в сохранении гомеостаза [19]. В свою очередь, ЭФПЭ, являясь функцией клеточных мембран и отражая состояние их метаболизма, может рассматриваться как маркерная характеристика состояния гомеостаза организма.
Подтверждением сказанному являются полученные ранее нами данные о типовых изменениях ЭФПЭ реализующихся через повышение содержания в крови стресс-реализующих гормонов [7, 13, 20].
Заключение. Значения параметров количества лейкоцитов, СОЭ и ЭФПЭ варьирует согласовано. При этом целесообразно проводить комплексный анализ СОЭ и общего количества лейкоцитов, тогда как изменение ЭФПЭ может быть интегральным показателем развития патологического процесса и эффективности проводимой терапии.
Кроме того, методика измерения ЭФПЭ позволяет анализировать показатель гораздо быстрее (в течение нескольких минут), по сравнению с измерением СОЭ (не менее часа), что обуславливает возможность экспресс-диагностики состояния организма.
