Введение. По данным литературы, пациенты с сосудистыми заболеваниями головного мозга составляют до 20% неврологических больных [8]. В России цереброваскулярные заболевания вышли на второе место (после кардиоваскулярных заболеваний) среди всех причин смерти населения.
Ишемические сосудистые поражения головного мозга возникают вследствие атеросклероза, гипертонической болезни и их сочетания. У большого числа людей в возрасте старше 50 лет процессы так называемого «нормального старения» быстро сменяются патологическими изменениями, связанными с недостаточностью церебрального кровотока вследствие поражения сосудов, кровоснабжающих головной мозг, и изменений реологических свойств крови, что в комплексе приводит к дизрегуляциям и снижению нейротрансмиттерной церебральной активности.
Установлено, что важную роль в процессе развития атеросклероза играют нарушения в системе гемостаза [6,7], причем в процесс вовлекаются все компоненты свертывающей системы. Вследствие этого формируется постоянное гиперкоагуляционное состояние, предрасполагающее к развитию на фоне атеросклероза тромботических осложнений. При этом главной опасностью для жизни человека является не сам атеросклероз, обычно протекающий со слабой клинической симптоматикой, а наслаивающийся на него тромбоз артерий, приводящий к острой ишемии жизненно важных органов и часто заканчивающийся летально. Поскольку в патогенезе эректильных нарушений у больных с цереброваскулярными заболеваниями присутствуют те же факторы, что и в патогенезе самих заболеваний, то правильно подобранная терапия ишемического инсульта, с учетом их патогенеза, может оказывать положительное влияние и на состояние эректильной функции.
Цель исследования: оптимизировать комплекс лечебных мероприятий, направленный на снижение риска развития тромботических осложнений у больных, перенесших малый ишемический инсульт.
Материалы и методы исследования. Под нашим наблюдением находились 80 мужчин с сексуальными расстройствами в раннем восстановительном периоде после малых ишемических инсультов, у которых была диагностирована эректильная дисфункция. Средний возраст больных составил 53,4±1,1 года. Этиологическими факторами ишемических нарушений мозгового кровообращения явились сочетание атеросклероза и артериальной гипертонии – у 30 человек (37,5%), гипертоническая болезнь – у 24 человек (30%), атеросклероз без гемодинамически значимых изменений сосудистого русла – у 26 человек (32,5%).
У всех наблюдаемых больных исследовали систему гемостаза: концентрацию фибриногена; протромбиновый индекс; общую свертываемость крови оценивали на тромбоэластографе – определяли величину r+k, отражающую ферментативную фазу свертывания крови, величину mа, характеризующую эластичность сгустка, ИТП (индекс тромбопластического потенциала). Агрегация тромбоцитов оценивали фотометрическим методом с использованием в качестве стимуляторов агрегации растворов аденозиндифосфата (АДФ) в концентрации 1х10-3 и в реакции коллаген-агрегации. В качестве маркеров внутрисосудистого тромбообразования проводили исследование содержания продуктов деградации фибрина и фибриногена (ПДФ) с помощью теста ингибиции гамагглютинации и полуколичественным методом (латекс-тест). Проводили определение ингибиторов свёртывания крови и маркеров фибринолитического звена системы гемостаза: активности антитромбина – III (АТ-III); концентрации АТ-III методом радиальной иммунодиффузии; концентрации комплекса тромбин-антитромбин III (Т-АТ-III); концентрации фибронектина методом радиальной диффузии; концентрации кислого альфа-гликопротеида - белка «активной фазы» и ингибитора агрегации тромбоцитов; концентрации плазминогена – основного субстрата фибринолитической системы.
Комплексное лечение применялось в двух терапевтических группах: 1-я группа (40 больных) получала йодобромные ванны температурой 36-37ºС, продолжительностью 15 минут, на курс – 10 процедур, через день и психотерапевтическую коррекцию сексуальной дезадаптации; 2-я (40 больных) получала йодобромные ванны по вышеописанной методике, вращающееся (вихревое) импульсное магнитное поле от аппарата «Магнитотурботрон», ежедневно, 15 сеансов, время экспозиции от 10 до 20 минут и психотерапевтическую коррекцию сексуальной дезадаптации.
Статистическая обработка данных проводилась с применением программных пакетов «Statistica» 6,0 версии. Уровень значимости различий между связанными выборками при соблюдении условий нормальности распределения и равенства дисперсий определялся с помощью критерия Стьюдента. Качественные показатели анализировались по критерию углового преобразования Фишера. Критический уровень значимости при проверке статистических гипотез принимался равным 0,05.
Результаты и обсуждение. У больных содержание фибриногена было повышенным в 1,4 раза по сравнению с нормой. Как известно, его содержание увеличивается при усилении внутрисосудистого свёртывания крови, которое сопровождает экссудативную фазу воспалительной реакции. Показатель время реакции + время начала образования сгустка (r+К тромбоэластограммы) у больных был снижен (р<0,05) в 1,33 раза по сравнению с нормой, что свидетельствовало о наличии хронометрической гиперкоагуляции, показатель максимальной амплитуды тромбоэластограммы (ma тромбоэластограммы) был повышен в 1,1 раза, ИТП – в 1,6 раза по сравнению с нормой, что свидетельствовало о высокой степени хронометрической структурной гиперкоагуляции.
Таким образом, у больных выявлена скрытая гиперкоагуляция. Повышение вязкости крови обусловлено интенсификацией агрегации и нарушением процесса дезагрегации эритроцитов. Наличие крупных прочных агрегатов выключает из кровотока большое число эритроцитов и приводит к нарушению полноценного газообмена, снижению степени кислородного обеспечения тканей и, в конечном счёте, к прогрессированию дисциркуляторной энцефалопатии. Увеличение вязкости крови способствует замедлению кровотока, что, в свою очередь, является одной из причин ишемии головного мозга [2,5,6].
Концентрация АТ-III у больных была повышена в 1,3 раза (р<0,05), а активность АТ-III – снижена (р<0,05) в 1,21 раза по сравнению с нормой, что свидетельствует о гиперкоагуляции и снижении антикоагулянтного потенциала крови.
В анамнезе у всех обследованных больных была урогенитальная инфекция, по поводу которой они получали антибиотики. Для стимуляции синтеза протромбина в гепатоцитах необходим витамин К, который вырабатывается кишечной флорой. Антибиотики, подавляя жизнедеятельность кишечной флоры, способствуют тем самым уменьшению уровня витамина К и, как следствие, дефициту протромбина. Однако, нельзя исключить, что увеличение протромбинового времени происходит в результате повышенного потребления тромбина в процессе внутрисосудистого свёртывания крови [4].
Концентрация плазмина и активность плазминогена у больных были снижены в 2,27 и 1,29 раза соответственно по сравнению с нормой. Известно, что плазминоген является предшественником плазмина, обладающего способностью воздействовать на фибриноген, фибрин, антигемофильный фактор, проакцелерин и фактор Кристмаса, является основным субстратом фибринолитической системы.
Концентрация фибринонектина (играет роль в адгезии тромбоцитов к коллагену, формировании и угнетении тромбов), альфа-1-антитрипсина, альфа-1-гликопротеина (белков активной фазы, являющихся ингибиторами фибринолиза) были повышены в 1,47, 1,7 и 1,6 раза соответственно по сравнению с нормой, что свидетельствует об угнетении фибринолиза в организме. Фибринонектин синтезируется эндотелием сосудистой стенки, является мультифакториальным фактором системы гемостаза. Кроме того, фибринонектин откладывается в местах острого и хронического воспаления, что приводит к быстрому развитию фиброзирующих и склеротических процессов в пораженных тканях [1,3]. На фоне обнаруженных изменений в системе гемостаза в организме больных активизируются аутоиммунные процессы.
У больных концентрация Т-АТ-III (наиболее информативный и ранний тест для диагностики внутрисосудистого свертывания крови) и ПДФ были повышены в 2,97 и 6,7 раза соответственно по сравнению с нормой, что свидетельствует о хронической тромбинемиии и хронической компенсированной форме синдрома диссеминированного внутрисосудистого свёртывания. В связи с активацией тромбиногенеза АТ-III связывается с тромбином и превращается в неактивный комплекс Т-АТ-III. Такое соотношение показателей системы гемостаза может характеризоваться как разнонаправленные сдвиги гемокоагуляции и фибринолиза, что свидетельствует о тромбогенном риске у данной группы пациентов [3,4].
Таблица 1. Показатели ингибиторов крови и фибринолитического звена системы гемостаза у больных и у здоровых мужчин
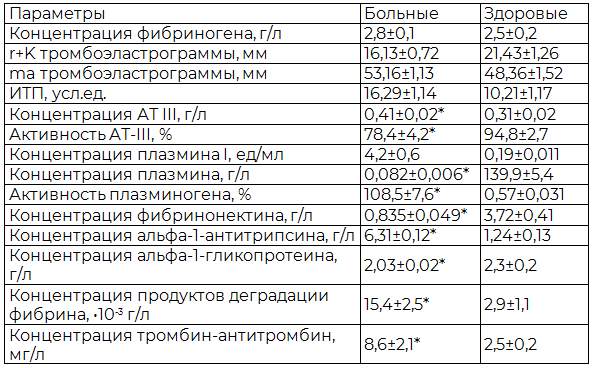
Примечание: * - р<0,05 по сравнению со здоровыми.
АТ-III, основной плазменный кофактор гепарина, относится к числу важнейших первичных антикоагулянтов, на долю которого приходится более 75% антикоагулянтной активности плазмы крови [4]. Как белок альфа-2-глобулиновой фракции крови, синтезируемый печенью, АТ-III является ингибитором тромбина. Дефицит АТ-III формирует гепаринорезистентность [4].
Количественный анализ показал, что гемостазиологические свойства крови были нарушены у 59 (73,8%) больных ЭД, перенесших малый ишемический инсульт.
После проведенного лечения концентрация фибрина снизилась на 7,1% в обеих группах, r+K тромбоэластограммы повысилась на 13,8% в контрольной и на 32,2% в основной группе, ma тромбоэластограммы снизилась на 3% и 5,6% соответственно, ИТП - на 23,3% и 36,2%, концентрация АТ-III – на 15,4% и 18%, альфа-1-антитрипсина – на 33% и 38,7%, альфа-1-гликопротеина – на 28,4% и 34,8%, фибринонектина – на 24,6% и 31,3%, продуктов деградации фибрина – на 79,1% и 83,3%, Т-АТ-III – на 54,7% и 59,5% соответственно, активность АТ-III повысилась на 7,9% и 15,2%, концентрация плазмина – на 63% и 79,8%, активность плазминогена – на 18,4% и 21,2% соответственно по сравнению с изначальными данными. В результате комплексного лечения гемостазиологические свойства крови нормализовались у 18 (64,3%) из 28 больных контрольной и у 23 (74,2%) из 31 больного основной группы (табл. 2).
Таблица 2. Влияние йодобромных ванн и йодобромных ванн в сочетании с магнитотерапией на показатели ингибиторов крови и фибринолитического звена системы гемостаза у больных с эректильной дисфункцией
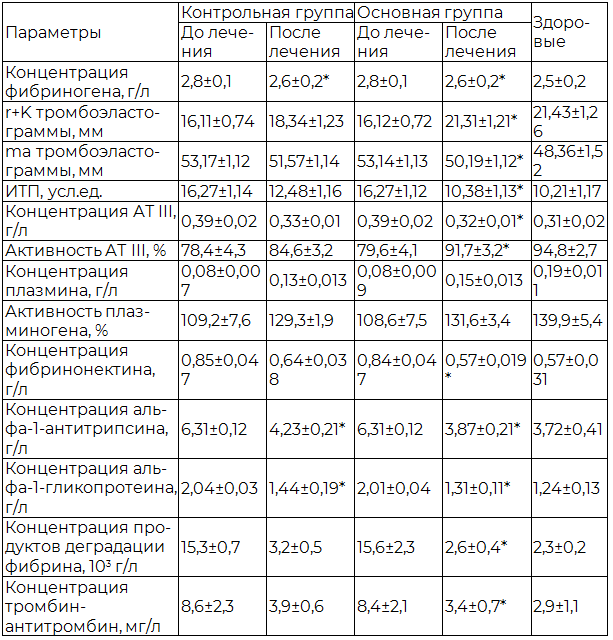
Примечание: * - р<0,05 по сравнению с показателями до лечения.
Таким образом, комплекс гемореологических параметров может рассматриваться в качестве маркеров тяжести течения ишемического инсульта и факторов риска развития повторных инсультов. Мониторинг показателей гемореологии является, на наш взгляд, обязательным условием для выбора успешной тактики ведения больных, перенесших ишемический инсульт.
Разработанный метод восстановительного лечения на этапе санаторно-курортной реабилитации позволит предупредить дальнейшее прогрессирование процесса, что значительно улучшит качество жизни этого распространенного контингента больных. Поэтому сочетанное использование йодобромных ванн и магнитотерапии может быть рекомендовано для внедрения в клинической практике.
