За последние годы в практике дерматологов заметно возросло количество детей, страдающих папилломавирусной инфекцией. Следует отметить, что лечение таких пациентов вызывает определенные трудности, а косметический дефект, к которому приводят бородавчатые разрастания на коже, особенно в области лица и кистей создают социальные проблемы, приводя к снижению качества жизни ребенка. Основным и единственным методом лечения бородавок является их механическое удаление, но такой метод имеет ряд недостатков, а именно: плохо переносится детьми, не всегда положительно воспринимается родителями, часто приводит к рецидивированию и прогрессированию заболевания [3]. На сегодняшний день предприняты значительные усилия для выяснения роли иммунной системы человека при папилломавирусной инфекции. Развитие папилломавирусной инфекции тесно связано с иммунным статусом инфицированного организма. Инфекция вызывает иммунодефицит и снижает противовирусную защиту, что способствует персистенции вируса папилломы человека [2]. Рядом исследователей дается разноречивая оценка роли различных звеньев иммунитета, как гуморального, так и клеточно-опосредованного, в развитии данного заболевания [5,9]. Выраженная связь иммунологических реакций с атипичной пролиферацией эпителия указывает на влияние клеточного и гуморального иммунитета на процессы, поддерживающие существование фоновых и предраковых заболеваний, а также провоцирующие их рецидивы.
К сожалению, проблема вируса папилломы человека в России в течение многих лет оставалась вне поля зрения специалистов. Отношение, сложившееся у многих специалистов к папилломавирусной инфекции кожи как редко встречающейся кожной патологии, является одним из факторов значительного увеличения числа больных детей в последнее десятилетие. Это было связано с недостаточными возможностями лабораторной диагностики и слабым пониманием патогенетических механизмов заболевания. Кроме того, участились случаи появления на коже папиллом, обусловленных вирусом папилломы человека высокого онкогенного риска. До сих пор не существует четко определенной системы медицинской помощи детям со специфическими инфекциями [6].
Также остается открытым для исследований вопрос тактики лечения папилломавирусной инфекции у детей. В современной научной литературе предлагается множество способов лечения клинических проявлений ПВИ (криодеструкция, электродеструкция, лазерная вапоризация, радиохирургическое удаление), но ни одна из методик не является приоритетной при выборе тактики лечения ребенка в силу высокого риска побочных эффектов и осложнений, технической сложности выполняемых манипуляций [1]. Проведенный нами анализ современной литературы показывает, что наиболее эффективным методом лечения бородавок можно считать комбинированный метод, включающий деструкцию видимых поражений и иммунотерапию [7,10]. Несмотря на множество предложенных локальных методов лечения остается высокой частота рецидивирования патологического процесса, что диктует необходимость поиска лекарственных средств, повышающих эффективность лечения.
Таким образом, высокая частота встречаемости папилломавирусной инфекции среди маленьких пациентов, отсутствие надежных методов лечения и частое рецидивирование инфекции делают данную проблему в дерматологии одной из наиболее актуальных.
Литературные данные свидетельствуют о тесной зависимости состояния здоровья детей от региональных экологических условий. До настоящего времени малоизученным остается вопрос о воздействии аномальных геомагнитных полей, возникающих в регионах с крупными подземными залежами железосодержащих руд, такими как Курская магнитная аномалия, где значения магнитного поля превышают фоновые в других регионах в 4-5 раз [4]. Наиболее восприимчивым к действию аномальных абиотических факторов в силу физиологической незрелости адаптационных систем является растущий организм. Магнитное поле оказывает негативное влияние на функциональное состояние многих систем детского организма и изменяет характер и интенсивность его ответной реакции.
Характер течения папилломавирусной инфекции в условиях воздействия аномальных магнитных полей и особенности реакции иммунной системы при этом практически не изучены. Представляет интерес также разработка методов фармакологической коррекции, позволяющих скомпенсировать влияние этих факторов на организм.
Цель исследования: оценить клинико-иммунологическую эффективность комплексной терапии папилломавирусной инфекции кожи у детей, проживающих в регионах с различным уровнем геомагнитного поля.
Материалы и методы исследования. В исследовании принимали участие 120 больных, которые соответствовали следующим критериям: дети в возрасте от 3 до 9 лет были поделены на две категории: от 3 до 5 лет и от 7 до 9 лет, в связи с возрастными различиями иммунологических показателей. В каждую категорию входило по 60 детей с установленным диагнозом папилломавирусная инфекция кожи D 23, не получавших терапию препаратами цитокинов (интерлейкинами 1 и 2, эритропоэтином, интерфероном и его индукторами) в течение одного предшествующего месяца, с отсутствием потребности в системном назначении глюкокортикостероидов и отсутствием терапии глюкокортикостероидами в течение 1 предшествующего месяца.
В группу контроля вошли 30 клинически здоровых детей в возрасте от 3 до 5 лет и 7-9 лет, проживающих в городе Курске при фоновых значениях геомагнитного поля (группа ГМП- контроль).
Родители всех детей заполняли информированное согласие на участие ребенка в исследовании. На первом этапе были изучены индивидуальные карты развития детей, амбулаторные карты, собран анамнез, проведен анализ данных клинико-параклинического обследования, целенаправленное анкетирование детей и родителей.
Средний возраст детей составил 6,5 лет. Из них девочек было 48 (40%), мальчиков – 72 (60%), что указывает на более частую заболеваемость среди мальчиков кожными формами папилломавирусной инфекции, в то время как проявления папилломавирусной инфекции на слизистых оболочках чаще наблюдаются среди девочек. Длительность заболевания на момент взятия под наблюдение составляла от 2 месяцев до 1 года.
Тяжесть заболевания оценивалась по распространенности патологического процесса, то есть по количеству морфологических элементов на коже. Наличие 1 элемента расценивалось как легкое течение, 2-5 - как средней тяжести, более 5 - как тяжелое течение. Больные распределились следующим образом: у 15% детей отмечалось легкое течение заболевания, у 50% – средняя тяжесть и у 35% детей – тяжелое течение.
По данным анамнеза, у 35 (29%) детей, из которых у 23 (19%) - только по материнской линии и у 12 (10%) - только по линии отца, определилась наследственная отягощенность по папилломавирусной инфекции.
При выявлении предполагаемого провоцирующего фактора предшествующего первичной манифестации папилломавирусной инфекции удалось установить, что она наиболее часто возникала у пациентов на фоне обострения хронических инфекций носоглотки, перенесенных ОРВИ у 82 (68%). У остальных 38 человек (32%) не удалось установить связи заболевания с какими-либо внешними или внутренними провоцирующими факторами.
Клиническая картина проявлений ПВИ на коже была разнообразна и представлена в виде пятнистых, гиперпигментированных очагов. Высыпания с умеренной или незначительной инфильтрацией (плоские бородавки), наблюдались в 15%, опухолевидные образования с ворсинчатой поверхностью (вульгарные бородавки) в 55%, образования в виде натоптышей с локализацией на подошвах (подошвенные) в 25% и опухолевидные образования на ножке (папилломы) в 5%.
Наиболее часто патологический процесс локализовался на коже ладоней и подошв 72,5%, на туловище 15%, на лице и шеи 7,5%, на конечностях 5% (рис. 2).
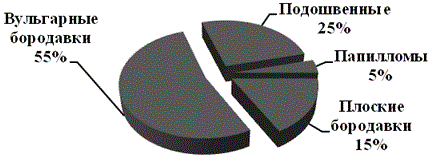
Рис. 1. Клиническое проявление ПВИ на коже
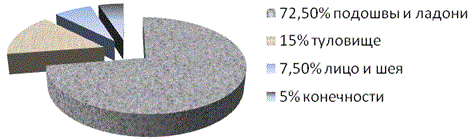
Рис. 2. Локализация очагов папилломавирусной инфекции
Анализ проведенного лечения показал, что у детей после удаления бородавок методом криодеструкции, который предполагает только механическое удаление, наблюдается высокая частота рецидивов (47%) в течение полугода, причем бородавки в большинстве случаев возникают на тех же участках кожи, что и раньше. Это, вероятно, объясняется нарушением не только общего, но и местного иммунитета. Эти данные указывают на низкую эффективность лечения ПВИ кожи традиционными методами.
С помощью рандомизации (вероятностный метод выборки) больные были разделены следующим образом: дети 1-й, 2-й, 3-й и 4-й групп имели установленный диагноз папилломавирусная инфекция кожи. При этом дети 1-й и 3-й группы в возрасте от 3 до 5 лет и 7-9 лет проживали в городе Железногорске, в регионе с аномальным магнитным полем (АМП), дети 2-й и 4-й групп в возрасте от 3 до 5 лет и 7-9 лет проживали в городе Курске. В опытных группах 1 (группа АМП –коррекция) и 2 (группа ГМП – коррекция) помимо криодеструктивного метода проводили по схеме иммунокоррекцию папилломавирусной инфекции кожи препаратом интерферона «Генферон Лайт». В 3-й (группа АМП сравнения) и 4-й (группа ГМП сравнения) группах дети не получали иммуномодулятор: для лечения использовался метод криодеструкции.
Детям с папилломавирусной инфекцией кожи, проживающим в г.х Курске и Железногорске, с целью иммунокоррекции ректально вводили препарат интерферона «Генфероном Лайт» по следующей схеме: по 1 суппозиторию 2 раза в день с 12-часовым интервалом в течение 10 дней до деструкции и в течении 10 дней по 1 суппозиторию 2 раза в день после деструкции. Затем в течение 1-3 месяцев – по 1 суппозиторию ректально на ночь через день. Разовая доза для детей старше 7 лет «Генферон Лайт» составляла 250 000 МЕ, до 7 лет 125 000 МЕ.
Исследование состояния клеточного и гуморального звена иммунитета в группах проводили до начала лечения и по его окончанию через 3 месяца. Уровнь иммуноглобулинов IgM, IgG, IgA в сыворотке крови определяли, по протоколу фирмы-изготовителя, методом твердофазного иммуноферментного анализа с помощью наборов реагентов «IgM общий – ИФА - БЕСТ», «IgG общий - ИФА - БЕСТ», «IgА общий - ИФА - БЕСТ» («Вектор-Бест», Россия). Уровень в сыворотке крови α- и γ-ИФН, ФНО-α, ИЛ-2, ИЛ-8 определяли методом твердофазного иммуноферментного анализа с использованием соответствующих наборов «BD Bioscience» согласно протоколу фирмы-изготовителя, методом ИФА-диагностики («BioSource International», США). Достоверность различий исследованных показателей определяли с использованием парного и непарного t-критерия Стьюдента [8].
Результаты исследования и их обсуждение. Исследование показателей иммунной системы показало, что у больных детей в возрастной группе от 3 до 5 лет, проживающих в городе Железногорске (АМП до лечения), уровень ИЛ 8, ФНО – α, γ-ИФН, Ig A, Ig M, Ig G достоверно превышал данные группы контроля (ГМП контроль) (табл. 1). У больных детей той же возрастной группы, проживающих в городе Курске (ГМП до лечения) от контрольных значений отличались (были выше) только концентрация Ig A (табл. 2). Сопоставление же иммунологических показателей у детей этой возрастной группы с папилломавирусной инфекцией кожи, проживающих в регионах с различным уровнем напряженности геомагнитного поля, выявило более высокие значения γ-ИФН, ИЛ 8, ФНО –α, Ig A, Ig M и Ig G у детей в городе Железногорске.
Таблица 1. Иммунологические показатели у детей 3-5 лет с папилломавирусной инфекцией кожи, проживающих в Железногорске до и после лечения
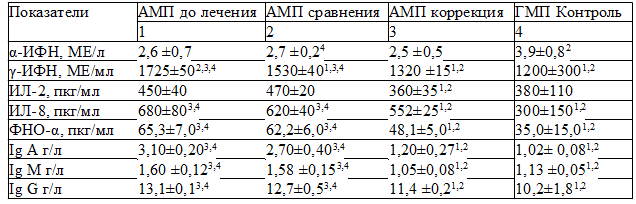
Примечание: здесь и далее цифрами надстрочного индекса указан номер группы, по отношению к которой разница достоверна (р<0,05)
Таблица 2. Иммунологические показатели у детей 3-5 лет с папилломавирусной инфекцией кожи, проживающих в Курске до и после лечения
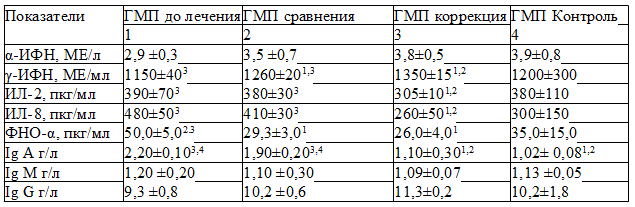
Исследование показателей иммунной системы у больных детей в возрастной группе от 7 до 9 лет, проживающих в городе Железногорске (АМП до лечения), показало, что уровень ИЛ 8, ФНО – α, Ig A и Ig M достоверно превышал данные группы контроля (ГМП контроль), а α-ИФН – был ниже их (табл. 3). У больных детей в той же возрастной группе, проживающих в городе Курске (ГМП до лечения), только концентрация ИЛ 8 и Ig A были выше контрольных значений, а α-ИФН - ниже их (табл. 4). Сопоставление же иммунологических показателей у детей этой возрастной группы с папилломавирусной инфекцией кожи, проживающих в регионах с различным уровнем напряженности геомагнитного поля, выявило более высокие значения γ-ИФН, ИЛ 8, ФНО –α, Ig A, Ig M и Ig G у детей в городе Железногорске.
После проведения терапии с использованием криодеструкции у детей г. Курска в возрастной группе от 3 до 5 лет (ГМП сравнения) регистрировалось увеличение концентрации γ-ИФН и снижение ФНО-α, тогда как у детей г. Железногорска (АМП сравнения) снижался только уровень γ-ИФН. В возрастной группе от 7 до 9 лет после проведения терапии с использованием криодеструкции изменения исследованных иммунологических показателей у детей г. Курска (ГМП сравнения) не отмечалось, тогда как у детей г. Железногорска (АМП сравнения) регистрировалось увеличение концентрации γ-ИФН.
Таблица 3. Иммунологические показатели у детей 7-9 лет с папилломавирусной инфекцией кожи, проживающих в Железногорске до и после лечения
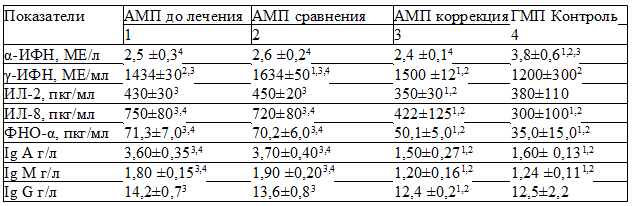
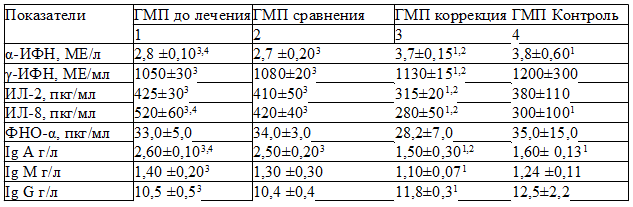
Таблица 4. Иммунологические показатели у детей 7-9 лет с папилломавирусной инфекцией кожи, проживающих в Курске до и после лечения
Включение в состав комплексной терапии препарата «Генферон Лайт» у детей в возрасте от 3 до 5 лет в группе ГМП – коррекция позволило нормализовать содержание Ig А. В той же возрастной категории в группе АМП – коррекция уровня контроля достигли концентрация ФНО–α, γ-ИФН, ИЛ-8, Ig A, Ig M и Ig G. Сопоставление значений исследованных иммунологических показателей у детей этой возрастной группы г. Курска и г. Железногорска после терапии с использованием «Генферон Лайт» выявило у пациентов г. Железногорска более высокие значения ИЛ 8, ФНО–α, и более низкие - α-ИФН.
Включение в состав комплексной терапии препарата «Генферон Лайт» у детей в возрасте от 7 до 9 лет в группе ГМП – коррекция позволило нормализовать содержание α-ИФН , ИЛ 8, Ig A и Ig M. В той же возрастной категории в группе АМП – коррекция уровня контроля достигли концентрация ИЛ 8, ФНО–α, Ig A и Ig M. Однако, сопоставление значений исследованных иммунологических показателей у детей этой возрастной группы г. Курска и г. Железногорска после терапии с использованием «Генферон Лайт» выявило у пациентов г. Железногорска более высокие значения γ-ИФН, ФНО–α и более низкие - α-ИФН.
Переносимость «Генферон Лайт» в использованных дозах была хорошей у всех детей. Побочных реакций выявлено не было. Положительная динамика иммунологических показателей сопровождалась благоприятными изменениями клинических симптомов.
Таким образом, клинические особенности течения папилломавирусной инфекции у детей, проживающих в Курске и Железногорске, характеризуют большей манифестацией заболевания в младшем школьном возрасте. Наиболее часто заболевание проявляется в виде вульгарных бородавок (55%) с локализацией в области ладоней и подошв (72,5%), а также характеризуется наследственной отягощенностью по папилломавирусной инфекции, чаще по линии матери (19%). Установлено, что развитие папилломавирусной инфекции у детей, проживающих в регионе Курской магнитной аномалии в условиях постоянного воздействия геомагнитного поля повышенной напряженности, приводит к возникновению более выраженных нарушений иммунной защиты по сравнению с пациентами региона с фоновым значением геомагнитного поля.
Традиционный метод лечения (криодеструкция в качестве монотерапии) не является эффективным в виду высокой частоты рецидивов в течение полугода (47%). Традиционная терапия позволяет с корригировать исходно измененные иммунологические показатели у детей г. Курска, но практически не оказывает никакого воздействия на показатели жителей г. Железногорска. Включение в терапию дополнительно иммуномодулятора «Генферон Лайт» позволило добиться коррекции вторичного иммунодефицита. Это может быть следствием того, что в состав препарата «Генферон Лайт» входит рекомбинантный человеческий интерферон альфа-2b, который оказывает противовирусное, иммуномодулирующее, антипролиферативное и антибактериальное действие. В то же время необходимо отметить, что значение ряда показателей детей г. Железногорска даже после достигнутой их коррекции в результате комплексной терапии по-прежнему отличались от значений детей аналогичной группы г. Курска
