Актуальность. Сахарный диабет (СД) является наиболее распространенным эндокринным заболеванием, которое в последнее десятилетие стали называть всемирной неинфекционной эпидемией: к 2025 году предполагается, что число больных СД превысит 300 млн. человек. А это значит, что будут расти и поздние осложнения, возникающие в результате метаболических нарушений, вызванных гипергликемией. Хорошо известно, что длительность и качество жизни больных СД определяются развитием и прогрессированием осложнений диабета [2, 6].
Нарушения обмена веществ, имеющие место при диабете, негативным образом сказываются на состоянии внутренних органов, именно поэтому на фоне сахарного диабета часто развивается такое состояние как диабетическая нефропатия. Одним из последствий диабетической нефропатии является анемия, возникающая у большей части больных с этой патологией [2, 3].
По данным эпидемиологического исследования NHANES II (National Health and Nutritional Examination Survey II), проводившегося в США, анемия наиболее распространена у детей до 7 лет (5,7%) и девочек подросткового возраста (5,9%). В противоположность этому при одномоментном исследовании пациентов в одной из диабетологических клиник Австралии было обнаружено, что у 23% из них диагностировалась анемия по критериям Всемирной организации здравоохранения (ВОЗ) [11]. Основными предикторами анемии в данном случае были насыщение трансферрина, скорость клубочковой фильтрации (СКФ) и скорость экскреции альбумина. На каждой стадии заболевания почек наиболее часто встречается анемия, а ее тяжесть, безусловно, выше у пациентов с диабетом по сравнению с пациентами без диабета [8], причем по мере ухудшения функции почек частота анемии экспоненциально увеличивается.
Анемия также довольно распространенное осложнение у пациентов с СД 2 типа на ранних стадиях диабетической нефропатии. Существуют убедительные данные последних исследований, свидетельствующие, что анемия имеет неблагоприятное влияние на прогрессирование диабетических осложнений, повышает риск сердечно–сосудистых заболеваний и увеличивает смертность.
Анемия приводит к ложному снижению уровня гликозилированного гемоглобина (HbA1c), что делает невозможной адекватную оценку углеводного обмена, а сохраняющаяся гипергликемия способствует прогрессированию микро– и макрососудистых осложнений [7, 9].
Этиология анемии при СД многофакторна и требует тщательного детального изучения для возможности эффективного управления этим грозным осложнением. Таким образом, наличие анемии относит пациентов с диабетом к группе риска прогрессирования ретинопатии, нефропатии, учащения госпитализаций и фатальных исходов [10,11].
Известно также, что анемия стимулирует пролиферативные и фиброзирующие процессы в таких органах, как сердце и почки. Эти процессы реализуются через усиление экспрессии генов факторов роста, гормонов и факторов, опосредующих вазоконстрикцию [5, 10].
В научно-исследовательской литературе мы нашли много работ посвященных взаимосвязи анемии и сахарному диабету у взрослых, тогда как у детей эта проблема решена недостаточно, а имеющиеся работы противоречивы [4, 6]. Так же мы не нашли работы посвященные качеству жизни у детей с сахарным диабетом осложненным анемией.
В связи с этим, считаем целесообразным провести изучение влияния анемии на течение и качество жизни детей с сахарным диабетом.
Материалы и методы исследования. В исследование были положены результаты обследования 72 детей, больных сахарным диабетом 1-го типа, в возрасте от 5 до 18 лет с длительностью болезни и продолжительностью заместительной инсулинотерапии от одного года до 10 лет.
Для оценки влияние анемии на качество жизни детей с сахарным диабетом пациенты были разделены на две группы: первую группу (n = 43) составили дети с СД и анемией, вторую группу (n = 29) — дети с СД без анемии.
Оценка КЖ больных детей была проведена с использованием международного стандартизированного опросника PedsQL™: его общего и диабетического модулей. PedsQL™ (Детский опросник КЖ) является одним из наиболее популярных опросников в мире [1, 4].
Данный опросник предназначен для изучения КЖ пациентов в возрасте от 2 до 18 лет включительно, страдающих СД. Указанный инструмент состоит из 28 вопросов, объединенных в следующие шкалы:
«Диабет» (клинические проявления гипогликемии, кетоацидоза) — 11 вопросов;
«Лечение» (проблемные ситуации, возникающие из-за необходимости проведения ежедневного самоконтроля гликемии, инсулинотерапии, жалобы на болезненные ощущения) — 11 вопросов;
«Беспокойство» (опасение развития острых и хронических диабетических осложнений, обеспокоенность эффективностью проводимой терапии) — 3 вопроса;
«Общение» (сложности в общении пациента с медицинским персоналом и окружающими) — 3 вопроса.
Ответы на вопросы в обоих модулях представлены в виде 5-балльных шкал Ликерта (горизонтально расположенных вариантов ответов на вопрос, каждому из которых соответствует цифра). Количество баллов при ответе колеблется от 0 до 4 (0 = никогда, 1 = почти никогда, 2 = иногда, 3 = часто, 4 = почти всегда). Для каждого вопроса предложено от трех до пяти вариантов ответов (в зависимости от возраста детей). Респондент в качестве ответа может выбрать только один из предложенных вариантов. Каждый вопрос оценивается по частоте возникновения предложенных ситуаций за «последний месяц». Окончательные результаты по каждой из шкал опросника представлены в баллах от 0 до 100: чем больше итоговая величина, тем лучше показатель качества жизни.
Результаты исследования. В период манифестации СД у всех обследованных превалировала типичная симптоматика заболевания в виде жажды, полиурии, прогрессирующего снижения массы тела.
В структуре осложнений СД 1 типа у детей первое место занимает диабетическая нейропатия (79,2%), меньший процент - нефропатия (5,6%), ретинопатия (4,2%) и диабетическая катаракта (1,4%).
Удельный вес встречаемости железодефицитной анемии (ЖДА) у детей больных СД составил 59,7%.
При анализе развитии анемии при сахарном диабете у детей были выявлены несколько причин, среди которых регистрировались воспаление, недостаточное питание, сопутствующие аутоиммунные заболевания, почечные заболевания, лекарства, а также гормональные изменения.
Согласно полученным данным нами было установлено, что наличие анемии у детей с СД повышает риск неблагоприятного течения диабетической ретинопатии, нефропатии, нейропатии и сердечно-сосудистых осложнений.
Так у данной группы детей наиболее чаще регистрировались сердечно-сосудистые заболевания по сравнению с больными СД без анемии (52,9% против 34,5% соответственно), скорее всего, это связано с тем, что анемия является независимым фактором, способствующим нарушению работы сердца и кровеносных сосудов.
У детей с СД сопряженный анемией средний показатель НвА1с составил 9,2±0,12%: у 23,2% пациентов показатели метаболического контроля соответствовали уровню субкомпенсации, у 76,7% — уровню декомпенсации.
У детей с СД без анемии средний показатель НвА1с составил 7,1±0,14%: 12 человек (41,4%) находились в состоянии субкомпенсации, 17 человек (58,6%) — в состоянии компенсации углеводного обмена.
При изучении уровня гемоглобина у детей больных СД и анемией было установлено, что концентрация гемоглобина у пациентов данной группы была значительно ниже, чем у больных группы сравнения (Р < 0,01) (рис. 1).
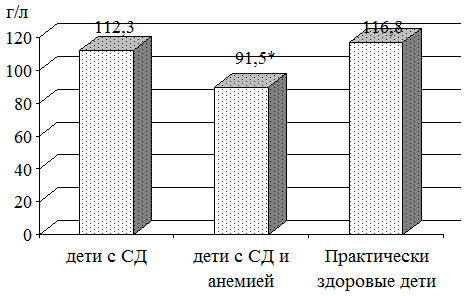
Рис. 1. Концентрация гемоглобина в периферической крови у детей больных СД: * - достоверность данных по сравнению с практически здоровыми детьми и детьми с СД (Р<0,01).
У данного контингента детей на фоне анемии отмечается снижение аппетита, физических способностей, интеллектуальной и умственные функций пациентов.
В соответствии с методологическими стандартами анализ показателей качества жизни был проведен в трех возрастных подгруппах [1, 4]: от 5 до 7 лет включительно, от 8 до 12 лет включительно, от 13 до 18 лет включительно (рис. 2).
Как видно из полученных данных в группе детей с СД сопряженный с анемией превалировали пациенты в возрасте 5-7 лет (44,2%), тогда как при заболевании СД без анемии превалирующая возрастная группа это дети 8-12 лет (34,5%) и 13-18 лет (37,9%).
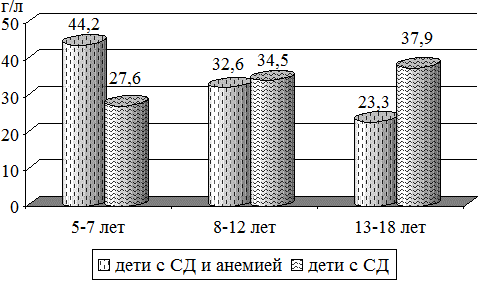
Рис. 2. Возрастная градация обследованных детей.
При анализе показателей качества жизни детей и подростков с СД как сопряженного с анемией было выявлено достоверное снижение уровня физического, эмоционального, социального и психосоциального функционирования, а также функционирование в детском саду и школе (табл. 1) во всех возрастных группах.
Согласно данным диабетического модуля, среди пациентов 1-й и 2-й группы дети дошкольного и младшего школьного возраста наиболее низко оценили шкалу «Диабет», а наиболее высокие показатели в данной возрастной подгруппе были получены по шкалам «Лечение» (блок 1) и «Беспокойство».
Изначально в дебюте заболевания все манипуляции (проведение самоконтроля, интерпретация показателей гликемии, подсчет количества хлебных единиц, введение инсулина) у пациентов данной возрастной группы в силу их малого возраста проводят родители. Однако, как было выяснено в процессе индивидуального интервьюирования, такая же ситуация сохраняется в большинстве семей и в последующем. Дети выступают скорее в роли стороннего наблюдателя, а не активного участника процесса. Поэтому большинство ситуаций, связанных непосредственно с процессом лечения сахарного диабета, ими не рассматриваются как проблематичные. Исключения составляют периодически возникающие болезненные ощущения, связанные с введением инсулина и/или проведением забора крови для самоконтроля гликемии.
В силу малого возраста эти пациенты не тревожатся по поводу диабетических осложнений и не боятся их, что отражает оценка, полученная по шкале «Беспокойство».
Таблица 1. Сравнительные показатели качества жизни детей и подростков
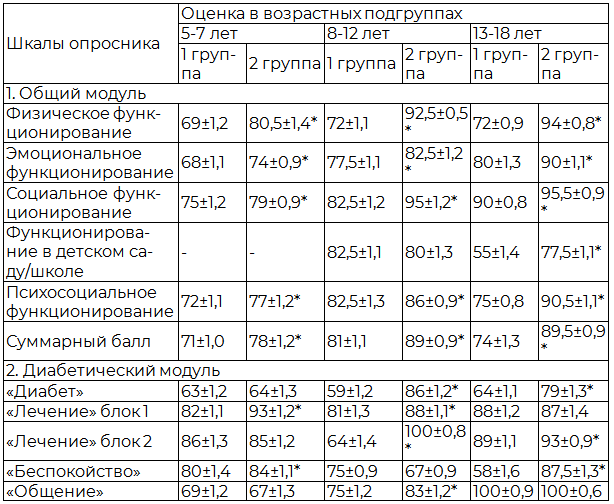
Примечание: * - достоверность данных между группами (Р<0,05-0,01).
Респондентами средней возрастной группы ситуации, сопряженные с проведением самоконтроля гликемии и введением инсулина, были восприняты менее проблематично и менее болезненно, чем дошкольниками, что может быть обусловлено адаптацией к своему заболеванию, повышением порога болевой чувствительности при увеличении длительности СД. В отличие от детей младшего возраста, значительная часть респондентов в возрасте 11–15 лет стесняются своего заболевания. По этой же причине многие из них уклоняются от расспросов о диабете как о своей болезни при общении с окружающими. Желание быть похожими на своих сверстников, что является отличительной чертой детей на данном этапе развития личности [1], часто становится причиной несоблюдения ими плана лечения, что в свою очередь приводит к возникновению ряда конфликтных и спорных ситуаций в отношениях с родителями. Данное положение подтверждает оценка шкалы «Лечение» (блок 2).
При анализе полученных данных обращает на себя внимание, что во всех трех возрастных группах шкала «Диабет», отражающая симптомы декомпенсации заболевания, была оценена низко, что свидетельствует о лабильном течении СД у подавляющего большинства опрошенных респондентов. Однако если подростков и детей старшего школьного возраста чаще других беспокоят симптомы, характерные для гипогликемических состояний (дрожь, головная боль, чувство голода), то дошкольники, напротив, чаще субъективно ощущают проявления гипергликемии (жажда, учащенные мочеиспускания, повышенный аппетит).
Респондентов старшей возрастной группы (в большей степени девушек) от пациентов других возрастных групп отличает высокая степень обеспокоенности развитием и прогрессированием хронических диабетических осложнений, что отражает крайне низкая оценка, полученная по шкале «Беспокойство». Свойственная всем подросткам обеспокоенность будущим [6] у пациентов с СД 1-го типа дополнительно усугубляется осознанием своей болезни как новой категории своего существования, реальности инвалидизации, возможного ограничения работоспособности.
Хочется отметить, что при оценке диабетического модуля достоверно низкие показатели были получены у детей 1 группы (Р<0,05-0,01).
Таким образом, анемия отрицательно влияете не только на клиническое течение СД, ускоряет развитие самой болезни и ее осложнений, но и на качество жизни детей и подростков.
Выводы
1. Влияние анемии на течение сахарного диабета у детей и подростков характеризуется повышением проявлений симптомов декомпенсации заболевания, снижением физических способностей, интеллектуальной и умственные функций пациентов.
2. Установлено отрицательное влияние сахарного диабета сопряженного анемий на качество жизни детей и подростков, которое связано со снижением уровня физического, эмоционального, социального и психосоциального функционирования.
