Введение. Бронхолегочная дисплазия (БЛД) является хроническим заболеванием бронхолегочной системы, характерным для недоношенных детей и нередко может стать причиной инвалидности и летальности [1, 6, 9, 11, 12]. Согласно данным литературы БЛД является полиэтиологическим заболеванием [3-5, 8, 11]. Факторами, способствующими развитию БЛД, являются незрелость легкого недоношенного ребенка, токсическое действие кислорода, баротравма легких, инфекция, отек легких, легочная гипертензия, наследственная предрасположенность, хронический гастроэзофагальный рефлюкс, гиповитаминозы А и Е [9, 11]. В основе лежит первичное (респираторные расстройства) и ятрогенное (ИВЛ, высокие концентрации кислорода) повреждение легких в сочетании с аутоповреждением легочной ткани, вследствие генерализованной воспалительной реакции [2, 8, 10]. Однако, недостаточно изучены факторы риска в формировании болезни, влияющие на степень тяжести данного заболевания.
Цель работы – изучить значимые антенатальные и постнатальные факторы риска формирования бронхолегочной дисплазии у недоношенных детей, определяющие тяжесть заболевания.
Материалы и методы. Исследование проводилось на базе ГУЗ Краевая детская клиническая больница отделение раннего возраста г. Читы в период 2009–2013 г. Группу исследования представили 121 недоношенный ребенок с клиническим диагнозом бронхолегочная дисплазия, согласно критериям степени тяжести данного заболевания новорожденные разделены на 3 подгруппы. В результате дети распределилась следующим образом: легкую степень тяжести БЛД имели 14 (11%) детей, среднюю степень 77 детей (64%) и тяжелую - 30 (25%) детей.
Проведен анализ данных материнского анамнеза, особенностей течения беременности и родов, состояние детей после рождения, клинические проявления в неонатальном периоде, результаты инструментальных и лабораторных показателей. Статистическая обработка полученных данных проводилась с использованием компьютерных программ «Statistica-6.0», Microsoft Exсel 2010 в соответствии с принципами доказательной медицины [7]. Проверку на нормальность распределения статистических показателей проводили путем построения гистограмм в программе «Statistiсa-6.0», а также с использованием критерия Колмогорова-Смирнова. При соответствии данных нормальному распределению значения количественных признаков представляли в виде M±SD, где М – среднее значение количественного признака, SD – стандартное отклонение среднего. Различия между группами выявлялись при помощи критерия Х2, критерия Стьюдента. При ненормальном распределении количественных признаков данные представляли в виде Me (25-75 перцентили), где Ме – медиана. Использовались методы непараметрической статистики с применением U-критерия Манна–Уитни (сравнение двух независимых переменных). Различия считались статистически значимыми при р<0,05.
Результаты и их обсуждение
В результате анализа отмечена известная закономерность, что тяжесть данного хронического заболевания легких наблюдается у детей с малым сроком гестации (р=0,02), низкой массой тела при рождении (р=0,02) и с длительным стационарным лечением (р=0,0004) виду тяжести состояния и глубокой незрелости (табл. 1).
Таблица 1. Распределение больных по сроку гестации, массе при рождении (М±SD)
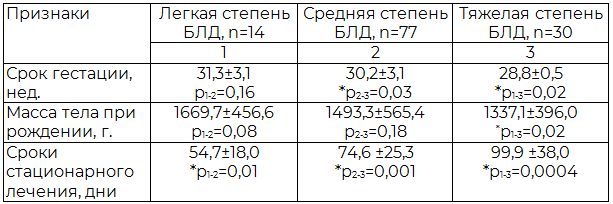
Примечание: *р – статистически значимая разница между группами по критерию Стьюдента (p<0,05).
Нами изучена зависимость степени тяжести БЛД у детей от экстрагенитальной и генитальной патологии матерей (таблица 2). Было отмечено, что факторами риска тяжелой степени БЛД в антенатальном периоде является кольпит (ОР=1,86), гестоз (ОР=1,21), латентное течение ВПГ 1 типа (ОР=1,66), анемия (ОР=1,24), пиелонефрит (ОР=2,02), ЗВУР (ОР=2,33). Данные патологические состояния усугубляют страдание плода, приводят к хронической внутриутробной гипоксии и рождению недоношенного ребенка с низкой и экстремально низкой массой тела при рождении.
Таблица 2. Экстрагенитальная и генитальная патология женщин, абс. (%)
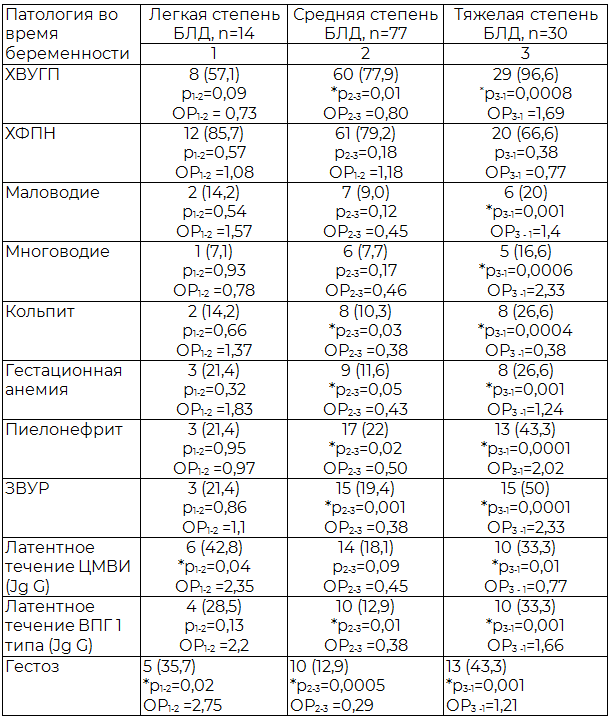
Примечание: здесь и далее ОР - отношение между группами, * р – статистически значимая разница между группами при использовании критерия χ2, p<0,05.
При изучении степени тяжести БЛД установлено, что его степень определяется степенью тяжести перенесенного РДС (ОР= 4,35) (табл. 3).
Таблица 3. Респираторный дистресс синдром у недоношенных, в зависимости от степени тяжести БЛД, абс. (%)
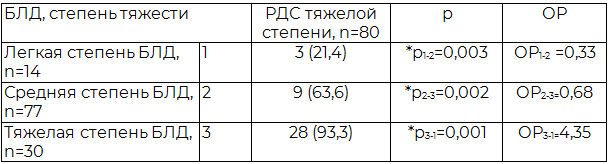
Глубоко незрелому ребенку с клиникой тяжелой дыхательной недостаточности проводилась пролонгированная ИВЛ (р=0,0002) и длительная оксигенотерапия (р=0,01), что способствовало повреждению легочной ткани, с формированием у пациентов в дальнейшем тяжелой БЛД (табл. 4).
Таблица 4. Респираторная терапия недоношенных детей, в зависимости от степени тяжести БЛД Ме (25-75 перцентили)
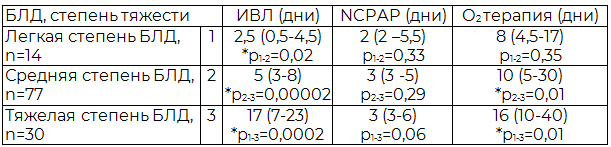
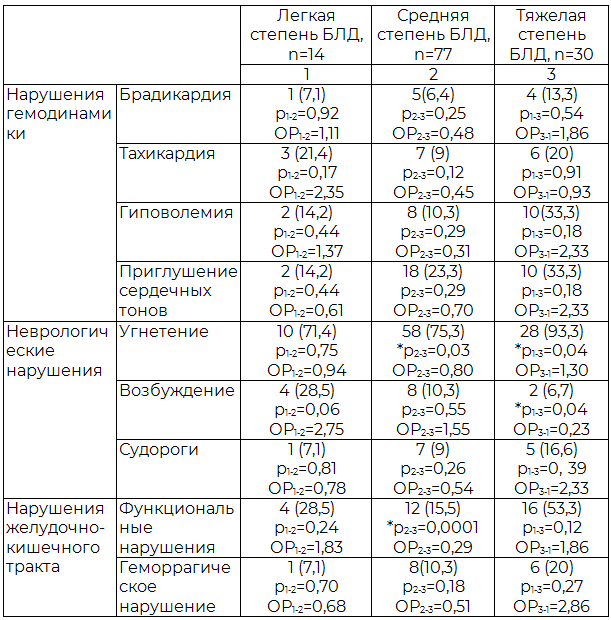
В периоде ранней адаптации дыхательная недостаточность у недоношенных сочеталась с поражением ЦНС, нарушениями гемодинамики и желудочно-кишечного тракта (табл. 5). В результате отмечено, что в раннем неонатальном периоде факторами риска формирования БЛД явились изменения гемодинамики (брадикардия (ОР=1,86), гиповолемия (ОР=2,33), приглушение сердечных тонов (ОР=2,33)), синдромы поражения ЦНС (угнетение (ОР=1,36), судороги (ОР=2,33)), дисфункция ЖКТ (функциональные нарушения (ОР=1,86), геморрагические проявления (ОР=2,80)).
Таблица 5. Состояние недоношенных детей в раннем неонатальном периоде, абс. (%)
Лечение всех исследуемых детей проводилось в отделении реанимации или патологии новорожденных, для дальнейшего лечения младенцы переводились в отделение раннего возраста КДКБ. Состояние при переводе в 2/3 случаев оценено как тяжелое. Тяжесть состояния определялась, в основном, степенью дыхательных нарушений, неврологической симптоматикой на фоне морфо-функциональной незрелости. В клинике у детей наблюдались бледность кожи с «мраморным» рисунком, периоральный, периорбитальный цианоз, выраженное участие вспомогательной мускулатуры в акте дыхания, тахипноэ до 54-64 в минуту, аускультативное дыхание резко ослаблено, у части пациентов выслушивались сухие и крепитирующие хрипы по всем легочным полям, кислородозависимость (Sa О2 без подачи кислорода составляла 70-80%). У 1/3 детей при переводе состояние оценено, как средней степени тяжести, Sat О2 без подачи кислорода составляла 90-98%, кожа бледно-розовая, цианоз носогубного треугольника, умеренное участие вспомогательной мускулатуры, аускультативно дыхание проводится по всем легочным полям ослабленное, у ряда детей выслушивались единичные хрипы.
Новорожденным проводился комплекс лабораторных и инструментальных исследований (табл. 6-9).
Таблица 6. Биохимические показатели крови недоношенных детей в зависимости от степени тяжести БЛД (Ме (25-75 перцентили))
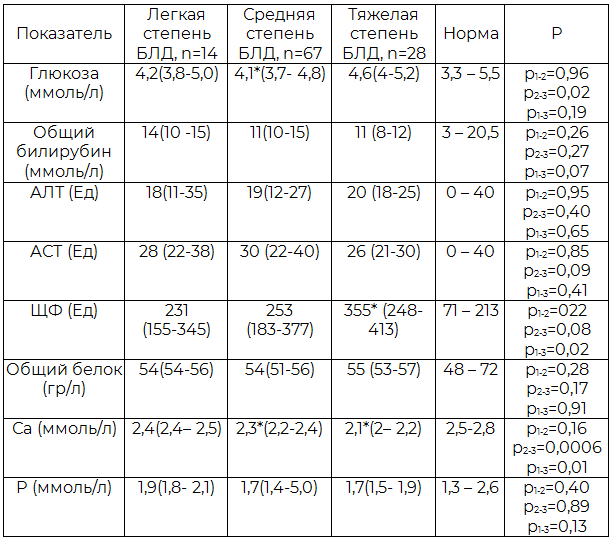
Примечание: здесь и далее *р – статистически значимая разница между группами при помощи критерия Манна-Уитни, p<0,05.
В биохимическом анализе крови в группе детей с тяжелой степенью БЛД отмечалось снижение уровня кальция (р=0,01), уровень ЩФ (р=0,02) повышался, что вероятно, связано с наличием у данной категории развития остеопении недоношенных.
Таблица 7. Показатели кислотно-основного равновесия крови недоношенных детей в зависимости от степени тяжести БЛД (Ме (25-75 перцентили))
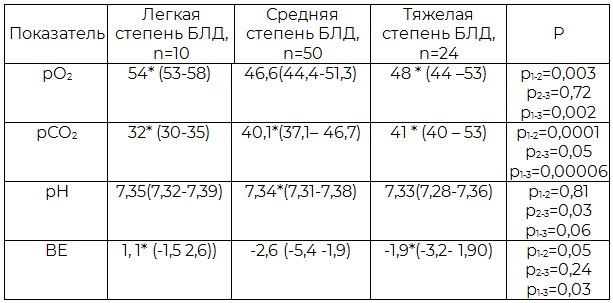
У детей с тяжелой степенью БЛД сохранялись метаболические нарушения (гиперкапния (р=0,00006), ВЕ (р=0,03)) респираторного характера, в условиях хронического воспаления в легочной ткани.
Дополнительные диагностические методы исследования имели ряд статистических отличий в зависимости от тяжести заболевания (таблица 8). У детей с тяжелой степенью заболевания по данным ЭКГ отмечались изменения: нагрузка на левый желудочек (ОР=1,86), синусовая тахикардия (ОР=2,00), изменения в миокарде (ОР=1,60) чаще метаболического и электролитного характера. Сохранение фетальных коммуникаций без гемодинамических проявлений у детей в возрасте 1 месяца подтверждает факт уточненной транзиторной кардиопатии у незрелых детей, статистически значимое ФОО (р=0,04, ОР=1,30) определялся у детей с тяжелой БЛД. Систолическое давление в легочной артерии в среднем при легкой степени составило 24,4±8,4 мм.рт.ст., при средней - 29,4±9,1 мм.рт.ст, при тяжелой степени 30,9±8,9 мм.рт.ст. (р=0,03), у 1/3 детей сохранялась умеренная гипертензия с тяжелой степенью БЛД (р=0,01).
Рентгенография органов грудной клетки у детей с клиникой тяжелой степени бронхолегочной дисплазии имела стойкие изменения в легких в виде интерстициального фиброза (р=0,003, ОР=7,00), подвздутия легких в латеральных отделах (ОР=2,32), обогащение легочного рисунка (ОР=1,86), неструкрурные изменения в корнях.
Стойкие неврологические симптомы у детей с тяжелой степенью БЛД подтверждались данными НГС, сохранялся перивентрикулярный отек (р=0,05, ОР=2,10), кисты (р=0,04, ОР=2,48), ПВЛ (р=0,01, ОР=3,73).
Таблица 8. Инструментальная диагностика БЛД в зависимости от степени тяжести абс. (%)
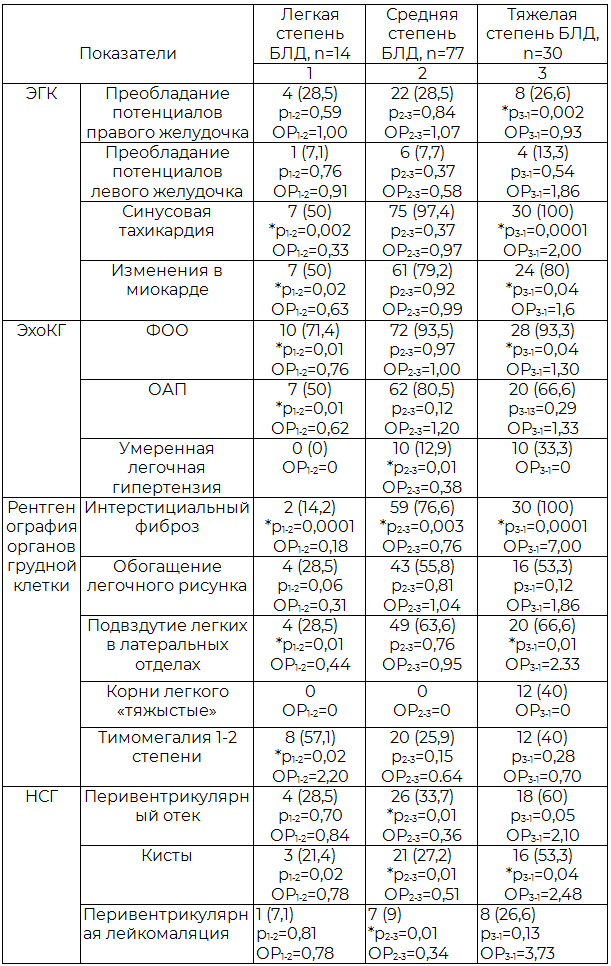
Примечание: здесь и далее ОР - отношение между группами, * р – статистически значимая разница между группами при использовании критерия χ2, p<0,05
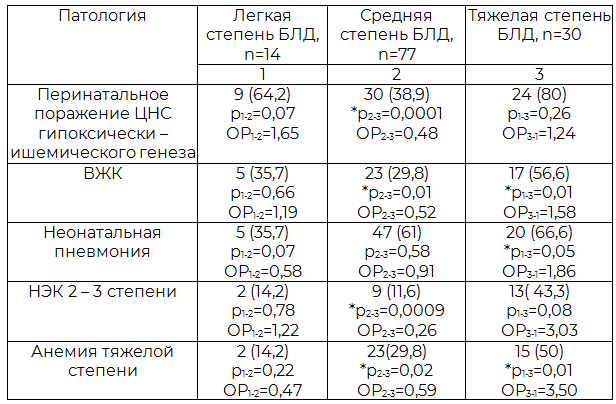
Тяжесть бронхолегочной дисплазии у детей в постнеонатальном периоде сочеталась (табл. 9) с поражением ЦНС (р=0,01, ОР=1,58), длительной пневмонией (р=0,05, ОР=1,86), некротическим энтероколитом (р=0,0009, ОР=3,03), анемией тяжелой степени (р=0,01, ОР=3,5).
Таблица 9. Коморбидная патология исследуемых групп, абс. (%)
Таким образом, проведенный анализ клинико-инструментальной картины бронхолегочной дисплазии в зависимости от степени тяжести заболевания показал, что для прогнозирования тяжелой БЛД возможно учитывать ряд значимых факторов риска:
- в антенатальном периоде: маловодие (ОР=1,4), многоводие (ОР= 2.33), неспецифический кольпит (ОР=1,86), ХФПН (ОР=1,69), гестоз (ОР=1,21), латентное течение ВПГ 1 типа (ОР=1,66), гестационную анемию (ОР=1,24), пиелонефрит (ОР=2,02), ЗВУР (ОР=2,33)
- в неонатальном периоде: РДС тяжелой степени (ОР=4,35), длительная ИВЛ (р=0,0002), пролонгированная оксигенотерапия (р=0,01), поражение ЦНС гипоксически – ишемического (ОР=1,24) и геморрагического (ОР=1,58) генеза, НЭК (ОР= 3,03), анемия (ОР=3,5), пневмония (ОР=1,86).
У детей с тяжелой бронхолегочной дисплазией при лабораторных и инструметальных методах исследования отмечалась гиповолемия (ОР=2,33), приглушение сердечных тонов (ОР=2,33), гипокальциемия (р=0,01), повышение ЩФ (р=0,02), гиперкапния (р=0,00006), гипоксемия (р=0,002), умеренная легочная гипертензия (р=0,03), изменения в легочной ткани при рентгенографии (интерсициальный фиброз (ОР=7,0), подвздутие легких в латеральных отделах (ОР=2,33), обогащение легочного рисунка (ОР=1,86)).
