Актуальность проблемы. Метаболический синдром (МС) - одна из самых актуальных проблем современной медицины, распространённость которого в общей популяции из года в год неуклонно растёт, приобретая характер настоящей эпидемии [1]. Так в экономически развитых странах как минимум 15-38% беременных страдают ожирением [6], из которых первородящие составляют 34-36%, повторнородящие - 52-64% случаев. Большее число тучных первобеременных (83-90%) страдает алиментарно-конституциональной формой ожирения с детского возраста [2].
Установлено, что при наличии МС у родителей резко возрастает риск его развития у их потомства [2].
В настоящее время, у 30 млн. детей и подростков выявлена избыточная масса тела, а 15 млн. уже страдают ожирением [3, 13]. Согласно прогнозу эпидемиологов, к 2025 году число лиц, страдающих МС, будет неуклонно расти и составит примерно 50% [4].
Известно, что нормально протекающая беременность сопровождается глубокими метаболическими изменениями организма матери, которые нередко переходят в патологические состояния.
При физиологически протекающей беременности происходит постепенное увеличение инсулинорезистентности (ИР), что выражается в снижении действия инсулина на 50% к концу III триместра [10]. Чтобы компенсировать это состояние, увеличивается функция β-клеток в три раза по сравнению с реакцией β-клеток на то же количество глюкозы до беременности [10].
Наличие физиологической ИР и сохранность компенсаторных механизмов обеспечивает нормальное развитие беременности. У женщин с наследственной неполноценностью инсулярного аппарата или при существовании каких-либо сбоев в механизмах компенсации увеличение степени ИР будет способствовать переходу физиологической ИР в патологическую, и приводить как к развитию осложнений беременности, так и к различным метаболическим нарушениям [5, 14].
Физиологически протекающей беременности свойственна выраженная гиперлипидемия, при этом имеется прямая корреляционная зависимость между содержанием липидов в крови и сроком беременности [6]. Максимальный рост липидных фракций отмечен во второй половине беременности, особенно в III триместре [7].
Второму триместру беременности соответствует анаболическая фаза с повышением уровня ХС ЛПНП, что свидетельствует об изменении метаболизма в целом с «переключением» белкового обмена на липидный как один из признаков адаптивного стрессорного состояния [6].
При беременности, протекающей на фоне МС, нередки такие осложнения родов, как дородовое излитие околоплодных вод, первичная и вторичная слабость родовой деятельности, угроза прерывания беременности, нередко гипотрофия плода, фетоплацентарная недостаточность, переношенная беременность, развитие гестозов вплоть до тяжёлой формы эклампсии и гибели плода [8, 9, 11, 12].
У пациенток с МС и ожирением III степени чаще развивается дистоция плечиков, хроническая внутриутробная гипоксия плода, аспирация околоплодных вод, ишемически-гипоксическое поражение ЦНС плода и новорожденного [11, 12].
При беременности, протекающей на фоне МС, которая отягощена изосерологической несовместимостью матери и плода, так же нередки осложнения родов [6, 8, 9, 11, 12].
Несмотря на значительные достижения перинатальной диагностики, заболеваемость и смертность новорожденных при групповой несовместимости до сих пор не удаётся предупредить полностью [15].
Цель исследования. Анализ биохимических и молекулярно-генетических показателей сыворотки крови рожениц с метаболическим синдромом и их новорождённых детей на фоне иммунологической несовместимости по антигену D системы Резус.
Материалы и методы. Было обследовано 67 человек: 31 роженица и 36 новорождённых детей (в том числе и двойни). В контрольную группу вошли 9 женщин без МС и их новорождённые дети. При сборе анамнеза основным критерием отбора в изучаемую группу было наличие у женщин диагноза МС разной степени тяжести, установленного до наступления беременности.
У всех обследуемых в сыворотке крови проведён биохимический анализ с исследованием углеводного, липидного, пигментного и белкового обменов, согласно стандартам обследования, на автоматическом биохимическом анализаторе Olympus AU 680 (Olympus Diagnostics, Германия).
Групповая принадлежность определялась двойной реакцией с цоликлонами и стандартными эритроцитами согласно действующему приказу.
Изучение роли полиморфизма генов проводили в лаборатории поликлиники Di-центра г. Саратова.
Материалом для генетического исследования служила венозная кровь. Генетические полиморфизмы определяли с использованием комплекта реагентов "Липидный обмен. Дополнительный профиль" с определением полиморфизмов АВСА1, АРОС3, LPL, PON1 методом пиросеквенирования.
Для математического и статистического анализа полученных результатов использовались пакеты компьютерных программ Statistica (StatSoft Inc.), SPSS 13.0 for Windows (SPSS Inc.), Microsoft Office Excel 2007.
Для определения вида распределения данных в выборках, использовались критерии Колмогорова-Смирнова и Шапиро-Уилка. В связи с тем, что распределение значений в выборках по данным перечисленных критериев отличалось от нормального, в процессе статистической обработки использовались методы непараметрического анализа. Анализ включал вычисление медианы, квартилей вариационного ряда, максимальных и минимальных значений, как критерий достоверности отличия между двумя независимыми группами использовался непараметрический критерий (U) Манна-Уитни. Как критерий достоверности различия между группами использовался непараметрический критерий Каскела-Уоллиса (Kruskel-Wallis).
Результаты и их обсуждение. В работе проведён анализ результатов обследования рожениц и их новорождённых детей за 2017 г. При распределении по групповой принадлежности выявилось, что с несовместимостью крови матери и плода родилось 9 детей от 8 матерей с МС, без развития гемолитической болезни новорождённых.
Таблица 1. Биохимические показатели рожениц с МС и их новорождённых детей
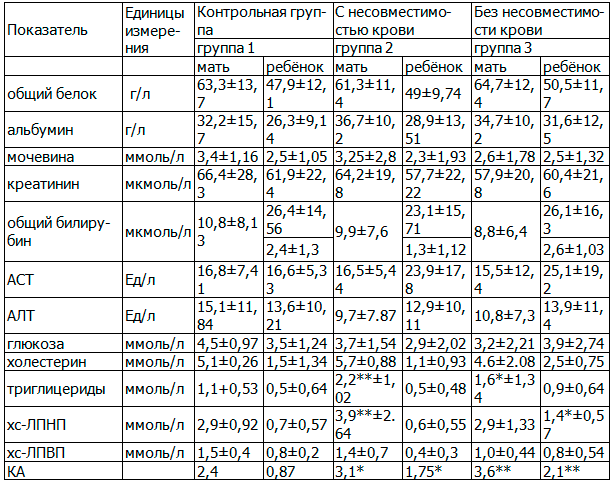
Примечание: результаты представлены в виде средних значений ± - стандартная ошибка; * - статистически значимое отличие (р<0,05) по сравнению с значениями группы сравнения; ** - статистически значимое отличие (р<0,01) по сравнению с значениями группы сравнения; *** - статистически значимое отличие (р<0,001) по сравнению с значениями группы сравнения.
Несмотря на изосерологический конфликт между матерью и ребёнком, в результате которого может быть снижена функция печени плода, уменьшения выработки белков в сыворотке крови относительно контрольной группы не наблюдается.
Уровень билирубина сыворотки крови у новорождённых в группе с несовместимостью меньше чем в контрольной группе и у детей, рождённых от матерей с МС без изосерологического конфликта. Причём, низкий уровень билирубина, относительно других изучаемых групп, наблюдается как при рождении детей, так и при их выписке.
Интересно проявляет себя липидный обмен, который также на фоне несовместимости даёт более благоприятные значения показателей сыворотки крови, чем в группе 3, но значительно ухудшаются относительно группы 1.
У рожениц и их новорождённых детей в группах 2 и 3, отмечается высокий уровень коэффициента атерогенности (КА). Это указывает на то, что состояние здоровья новорождённых детей в будущем может характеризоваться не очень благоприятным течением, особенно со стороны сердечно-сосудистой системы.
По мнению большинства авторов, до 50% всех «неблагоприятных» нарушений, и в частности липидного обмена, у детей может быть связано с генетическими факторами.
Первые исследования генетического профиля «Липидный обмен. Дополнительный профиль» методом пиросеквенирования у рожениц и их новорождённых детей в группах 2 и 3 показали, что у обследованных детей не выявлен защитный аллель в полиморфизме rs2230806 (вариант GG), что связано с риском кардиоваскулярных заболеваний, тогда как у матерей он присутствует. У рожениц и их новорождённых детей выявлен аллель риска в полиморфизме rs5128,гомозигота, что ассоциировано с развитием метаболического синдрома.
Не выявлен защитный аллель в полиморфизме rs328, что свидетельствует о возможном развитии ИБС, ишемического и атеротромботического инсульта. У детей выявлен аллель риска в полиморфизме rs662 в гетерозиготном состоянии – маркер повышенного риска кардиоваскулярных и атеросклеротических заболеваний, который отсутствует у матерей (таб. 2).
При сравнительном анализе наиболее часто встречающихся генотипов (таб. 2) матерей и детей, прослеживается тенденция к отсутствию у новорождённых детей защитных аллей и наличие аллелей риска, способствующие повышенному риску развития сердечно-сосудистой патологии.
Таблица 2. Профиль генетического исследования «Липидный обмен. Дополнительный профиль» рожениц
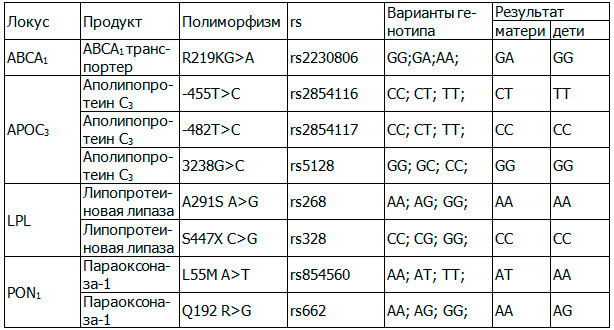
Ключевая роль среди изучаемых полиморфизмов, согласно данному исследованию, принадлежит полиморфизму Q192 R>G гена параоксоназы-1. Полученные результаты дают возможность разработать и внедрить в практику программу скринингового обследования, включающую медико-генетическое консультирование лиц с семейным анамнезом МС.
Есть основания полагать, что выявление полиморфных вариантов генов системы липидного обмена как генетических маркеров сердечно-сосудистых нарушений позволит существенно увеличить возможности проведения своевременной профилактики, адекватного патогенетического лечения, а также оценки риска развития кардиоваскулярных заболеваний и дальнейшего прогноза.
Выводы
1) Корректное и своевременное изосерологическое исследование беременной с метаболическим синдромом в анамнезе и новорождённого помогает установить и уменьшить развитие возможных осложнений.
2) Изменение показателей липидного обмена наблюдается как на фоне несовместимости крови матери с МС и её ребёнка, так и при отсутствии конфликта.
3) При выявлении у новорождённых детей аллелей риска или отсутствии защитных аллелей перечисленных выше полиморфизмов, необходимо отнести их в группу риска по возможности развития сердечно-сосудистой патологии.
