Актуальность. Проблема возникновения нежелательных реакций (далее - НР), обусловленных взаимодействием лекарственных средств (ЛС), стала широко освещаться в медицинской литературе к середине прошлого века, когда информация о клинически значимых лекарственных взаимодействиях начала появляться в медицинских журналах [13, 18]. В 1965 г. в Лондоне состоялся первый международный симпозиум, посвященный проблеме лекарственных взаимодействий и связанных с ними нежелательных реакций [18]. В 1970-х г. контрольно-разрешительные органы различных стран стали требовать от фармацевтических компаний ежегодно выпускать в обзорах обновленную информацию, касающуюся лекарственных взаимодействий и связанных с ними НР [17]. Количество публикаций, посвященных проблеме развития НР, возникших в результате лекарственных взаимодействий, постоянно возрастает - с 43 в 1970 г. до более 1400 публикаций в 1980 г. [17].
В настоящее время стало очевидным, что взаимодействия ЛС, приводящие к осложнениям фармакотерапии, являются серьезной проблемой здравоохранения, обуславливают возникновение НР и являются одной из причин госпитализации пациентов [4,21]. Каждый год из-за осложнений лекарственной терапии в США умирают от 100 до 200 тыс. человек, в трети случаев причиной смерти являлись НР, связанные с взаимодействием ЛС при применении потенциально опасных комбинаций ЛС [6, 11]. По данным разных авторов, от 17 до 23% назначаемых врачами комбинаций ЛС являются потенциально опасными, и у 6-8% больных развиваются серьезные НР, обусловленные взаимодействием назначенных ЛС [1-3, 11, 14].
НР, возникающие при применении потенциально опасных комбинаций, также представляют собой серьезную экономическую проблему, так как расходы на их лечение составляют половину затрат на терапию всех лекарственных осложнений [10, 12, 15-16, 19].
В связи с этим, все более актуальной становится проблема безопасности, связанная с применением нерациональных комбинаций ЛС, которые могут сопровождаться взаимодействием ЛС, приводящим не только к снижению эффективности фармакотерапии, но и к снижению ее безопасности [7-9, 20-22].
Цели. На основе анализа спонтанных сообщений о НР на ЛС, поступивших в отечественную базу данных, оценить масштаб проблемы возникновения лекарственных осложнений, связанных с взаимодействием ЛС. Апробировать и внедрить в практику отечественного фармаконадзора современный метод определения степени достоверности (СД) причинно- следственной связи (ПСС) между развившейся НР и конкретной комбинацией ЛС.
Материалы и методы. Проведенное исследование было спланировано как ретроспективное обсервационное описательное фармакоэпидемиологическое исследование.
В ходе настоящего исследования был проведен ретроспективный анализ спонтанных сообщений о НР, поступивших в отечественную базу данных АИС Росздравнадзора, для выявления в них информации о развитии НР в результате взаимодействия между ЛС. Оценивались спонтанные сообщения, поступившие в отечественную базу данных с 1 января 2010 г. по 31 марта 2011 г. включительно.
Карты-извещения о НР были заполнены по определенной форме и содержали информацию о НР, вызванных зарегистрированными ЛС и выявленных в период широкого использования этих ЛС в медицинской практике.
Спонтанные сообщения содержали следующие данные: фамилию, имя, отчество, пол, возраст пациента; дату начала НР, дату разрешения НР, описание НР; список подозреваемых в возникновении НР и сопутствующих ЛС, а так же информацию о применении каждого ЛС: показания к назначению, дозирование, способ введения и продолжительность терапии. Также была представлена информация об исходе НР, о результатах отмены ЛС, о результатах повторного назначения ЛС, о сопутствующих заболеваниях, о предпринятых мерах коррекции НР. В спонтанных сообщениях отмечались критерии серьезности НР; оценка причинно-следственной связи (ПСС), выставленная отправителями; оценка ПСС, выставленная специалистами Центра экспертизы безопасности лекарств ФГБУ «Научный центр экспертизы средств медицинского применения»; значимая дополнительная информация.
Для оценки каждого спонтанного сообщения, содержащего информацию о случае развития НР при назначении нескольких ЛС, необходимо было выяснить ПСС между развившейся НР и комбинацией ЛС, то есть определить степень причастности комбинации ЛС к развившемуся лекарственному осложнению. Для этой цели был применен модифицированный нами метод стандартизированной оценки СД ПСС- Шкала определения СД ПСС «НР- взаимодействие ЛС». Для определения достоверности ПСС между НР и комбинацией ЛС предусматривались 4 степени достоверности: определенная, вероятная, возможная и сомнительная.
Все спонтанные сообщения, содержащие информацию о применении двух и более ЛС, были проанализированы с помощью Шкалы определения СД ПСС «НР-взаимодействие ЛС» (табл. 1).
В табл. 2 представлены степени достоверности ПСС «НР-взаимодействие ЛС» в зависимости от суммы полученных баллов.
В исследование не входили повторные и дубликатные спонтанные сообщения о НР на ЛС, а также спонтанные сообщения о НР, вызванных применением вакцин.
Результаты и обсуждение. Всего было проанализировано 11761 спонтанное сообщение, из которых в 5665 (48,1%) извещениях было сообщено о НР, возникшей при терапии более чем 1 ЛС. Было установлено, что 4506 сообщений содержали информацию о 2-х и более ЛС, взаимодействие которых затруднительно.
Таблица 1. Шкала определения степени достоверности причинно-следственной связи «НР-взаимодействие ЛС»
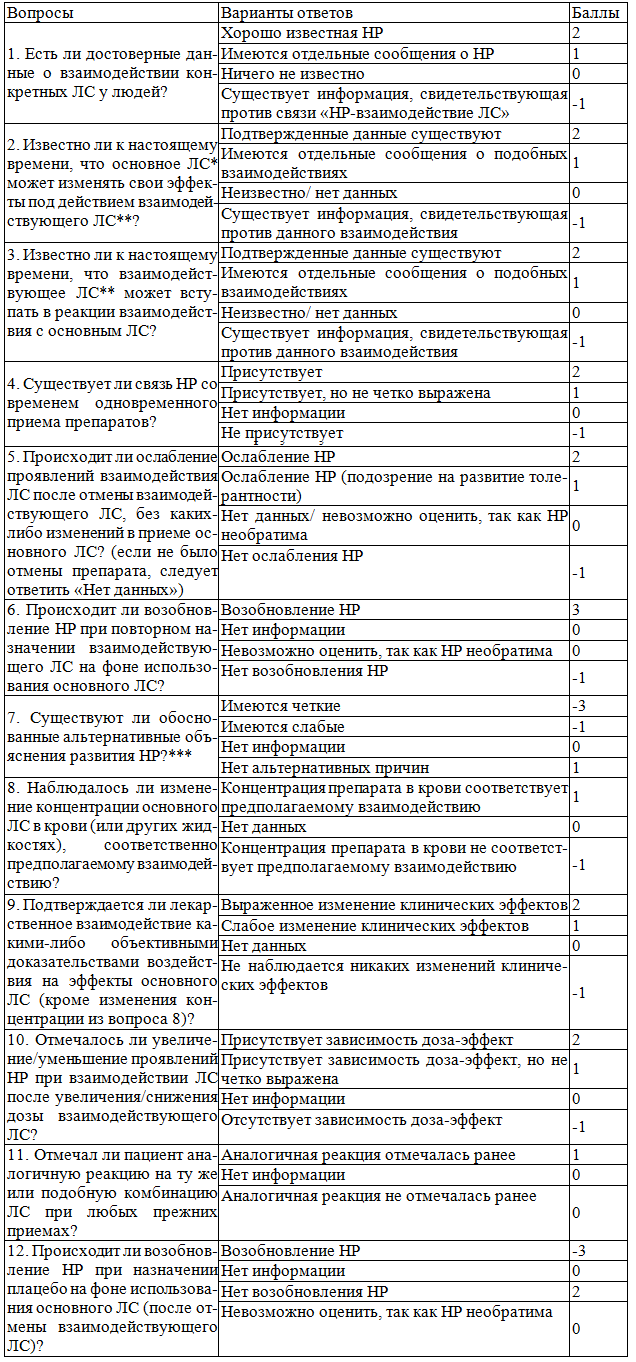
Примечания: * основной препарат - ЛС, оказывающее основное действие, которое изменяется на фоне взаимодействия; ** взаимодействующий препарат - ЛС, которое изменяет действие основного препарата; *** необходимо учитывать конкретную клиническую ситуацию и воздействие других факторов риска (возраст, неправильная дозировка ЛС и т.д.). Ответ «Нет альтернативных причин» предполагает, что полученная информация позволяет исключить другие причины развития НР. При недостаточности полученной информации, следует ответить «Нет информации»
Таблица 2. Cтепени достоверности ПСС «НР-взаимодействие ЛС» в зависимости от суммы полученных баллов

Потенциально опасные комбинации ЛС, имеющие повышенный риск развития лекарственных осложнений, связанных с взаимодействием ЛС, были выявлены в 1159 (20,5%) спонтанных сообщениях. К потенциально опасным комбинациям относятся те комбинации ЛС, при назначении которых существует высокий риск развития НР, в том числе и серьезных (создающих угрозу жизни, приводящих к госпитализации, стойкой нетрудоспособности и т.д.); научная доказанность взаимодействия между препаратами документально подтверждена в нескольких крупных контролируемых клинических исследованиях; информация о взаимодействии данной комбинации ЛС представлена в инструкциях по медицинскому применению препаратов.
В 230 сообщениях (из 1159) выявлены НР, связанные с взаимодействием ЛС. Спонтанные сообщения, содержащие информацию о НР, обусловленных взаимодействием ЛС, составляют 19,8% от числа спонтанных сообщений, содержащих потенциально опасные комбинации ЛС; 4,1% от числа спонтанных сообщений о применении более 1 ЛС; 1,95% от общего числа анализируемых спонтанных сообщений, полученных за 15 месяцев.
В 217 сообщениях (94,3%) НР были связаны с взаимодействием 1 пары ЛС, в 13 сообщениях (5,7%) НР были обусловлены взаимодействием 2-х пар ЛС.
В табл. 3 представлены распределение спонтанных сообщений по группам, в зависимости от числа используемых лекарственных средств.
Таблица 3. Группы спонтанных сообщений в зависимости от числа используемых лекарственных средств
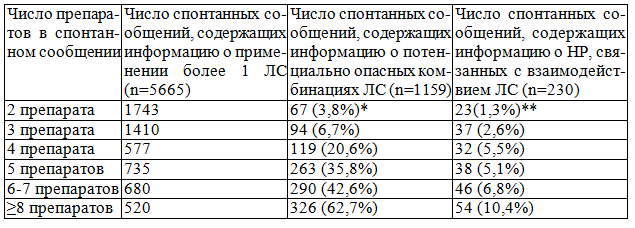
Примечания: * доля спонтанных сообщений, содержащих информацию о потенциально опасных комбинациях ЛС, от общего числа спонтанных сообщений, содержащих информацию о применении аналогичного числа препаратов; **доля спонтанных сообщений, содержащих информацию о НР, связанных с взаимодействием ЛС, от общего числа спонтанных сообщений, содержащих информацию о применении аналогичного числа препаратов
В 16 сообщениях, содержащих информацию о НР, вызванных взаимодействием ЛС, возраст пациентов составлял менее 18 лет, в 34 сообщениях - 18-45 лет, в 43 сообщениях - 45-64 года, в 137 сообщениях возраст пациентов был более 65 лет.
В 106 случаях (46,1%) НР, возникшие в результате взаимодействия ЛС, развивались у мужчин, в 124 случаях(53,9%)- у женщин.
В табл. 4 представлены основные данные спонтанных сообщений, содержащих информацию о НР, вызванных взаимодействием ЛС, и данные сообщений, содержащих информацию о потенциально опасных лекарственных взаимодействиях ЛС.
В 167 сообщениях (72,6%) НР, связанные с взаимодействием ЛС, были отнесены к серьезным: в 3 случаях НР завершились летальным исходом, в 65 случаях НР создали угрозу жизни пациента, в 99 случаях НР послужили причиной госпитализации или ее продления.
Спонтанные сообщения о НР, обусловленных взаимодействием ЛС, были отправлены лечащими врачами (55,7%), клиническими фармакологами (39,6%), фармкомпаниями (3,4%).
Таблица 4. Основные данные спонтанных сообщений, содержащих информацию о НР и содержащих информацию о потенциально опасных лекарственных взаимодействиях ЛС
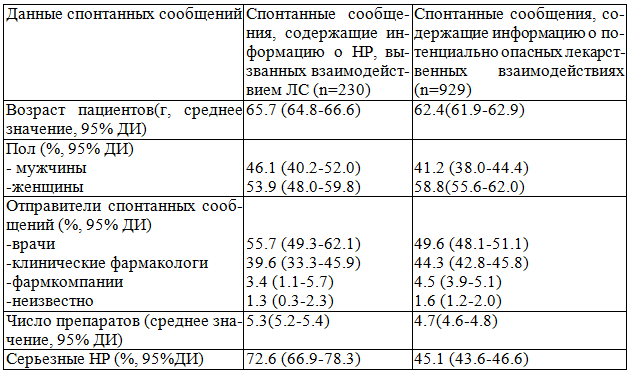
При анализе сообщений о НР, связанных с взаимодействием ЛС, весьма важным является определение степени достоверности (СД) причинно-следственной связи (ПСС) «НР-взаимодействие ЛС».
Определение СД ПСС «НР-взаимодействие ЛС» является одним из основных этапов оценки сообщений о НР, которые в настоящее время проводится в национальных и региональных центрах по контролю безопасности лекарств во многих странах мира, а так же в центре ВОЗ.
Широко используемая в фармаконадзоре шкала Наранжо не позволяет получить достоверные данные о СД ПСС «НР-взаимодействие ЛС», поскольку она была рассчитана на оценку взаимосвязи одного ЛС с развитием НР.
В большей степени решению данной проблемы отвечает предложенная в 2007 г. шкала John R. Horn и Philip D. Hansten [5].
Стандартизированные методы типа шкалы Horn-Hansten, широко применяемые в разных странах для оценки СД ПСС “НР-взаимодействие ЛС”, хорошо зарекомендовали себя, так как они обеспечивают унифицированный подход к анализу поступающих сообщений о подозреваемых НР, снижение вариабельности в суждениях.
В нашем исследовании была использована модифицированная нами Шкала определения СД ПСС «НР-взаимодействие ЛС», в основу которой легла шкала Horn-Hansten. К 10 вопросам указанной шкалы были добавлены 2 важных вопроса, позволяющих получить более полную информацию о НР, развившейся в результате взаимодействия ЛС, а также варианты ответов на вопросы, что позволяет исключить вероятность неоднозначных ответов, способных повлиять на оценку СД ПСС.
В практике отечественного фармаконадзора до сих пор не использовался данный методический подход для оценки взаимосвязи осложнений, связанных с взаимодействием ЛС. В связи с этим, целью нашего исследования было оценить значимость стандартизированной оценки СД ПСС «НР-взаимо-действие ЛС» в процессе анализа сообщений из отечественной базы данных о НР.
При анализе спонтанных сообщений было выявлено, что в спонтанных сообщениях о НР, вызванных взаимодействием ЛС, СД ПСС «НР-взаимо-действие ЛС» была определена отправителями как вероятная в 32 сообщениях, возможная - в 167 сообщениях, сомнительная - в 25 сообщениях, условная- в 31 сообщениях. Нами был проведен анализ спонтанных сообщений, содержащих информацию о НР, связанных с взаимодействием ЛС, с помощью модифицированной Шкалы определения СД ПСС «НР-взаимодействие ЛС», и были получены следующие результаты - в 25 сообщениях связь была определена как определенная, в 186 сообщениях как вероятная, в 18 сообщениях как возможная, в 1 сообщении как сомнительная.
Таким образом, использование нашей шкалы позволяет значительно улучшить качество рутинного анализа спонтанных сообщений и экспертную оценку безопасности комбинаций ЛС специалистами в области фармаконадзора, что необходимо для своевременной разработки рекомендаций и принятия административных мер, направленных на повышение безопасности комбинированной фармакотерапии.
В нашем исследовании было выявлено увеличение числа НР, вызванных взаимодействием ЛС, по мере увеличения возраста. В 137 случаях (59,6%) НР, вызванные взаимодействием ЛС, были выявлены у пациентов старше 65 лет, а средний возраст пациентов, у которых развились НР на фоне взаимодействия ЛС, составил 65,7 лет.
Основными отправителями сообщений были врачи (58,3%), что, возможно, является показателем того, что большинство лекарственных взаимодействий развивается в лечебных учреждениях, а так же того, что НР, вызываемые взаимодействием ЛС, являются серьезными и требуют госпитализации. Это подтверждается полученными в исследовании данными о том, что 72,6% НР, вызванных взаимодействием ЛС, являются серьезными.
В нашем исследовании серьезные НР, вызванные лекарственными взаимодействиями, чаще возникали при применении НПВС в 37,8 % случаев, гематотропных препаратов – в 15,9% , противомикробных ЛС – в 14,4%.
Большая часть НР была представлена в виде осложнений со стороны системы кроветворения и гемостаза (38,3%), со стороны ЦНС (13,8%) и со стороны желудочно-кишечного тракта (13,7%). Это связано с широким применением данных групп ЛС при большом спектре заболеваний, а так же с тем, что при их назначении часто не учитывается риск развития лекарственных взаимодействий.
В нашем исследовании выявлено, что только в 13 спонтанных сообщениях (5,7%), содержащих информацию о НР, связанных с взаимодействием ЛС, отправители спонтанных сообщений смогли идентифицировать лекарственные взаимодействия и вызванные ими НР. В остальных случаях лекарственные взаимодействия остались нераспознанными. Это может говорить как о низкой настороженности врачей в отношении лекарственных взаимодействий, так и об ограниченном доступе к имеющейся информации о безопасности комбинированной фармакотерапии.
Проведенное нами исследование подтвердило то, что использование спонтанных сообщений, а так же применение Шкалы определения СД ПСС «НР-взаимодействие ЛС» при обработке спонтанных сообщений является ценным инструментом для выявления НР, связанных с взаимодействием ЛС, в том числе и серьезных. Так, было выявлено, что 20,7% комбинаций ЛС являлись потенциально опасными, а НР в результате взаимодействия возникли в 19,8% случаев. Также при использовании модифицированной Шкалы определения СД ПСС «НР-взаимодействие ЛС» была получена более высокая степень достоверности причинно-следственной связи при анализе спонтанных сообщений о НР. Это говорит о более высоком качестве экспертной оценки и большей точности при анализе спонтанных сообщений с помощью данного метода, что позволяет на основании полученных результатов рекомендовать внедрение его в работу экспертных подразделений системы фармаконадзора. Это будет способствовать предупреждению и снижению рисков развития неблагоприятных последствий комбинированной лекарственной терапии, повышая ее эффективность и безопасность.
Выводы
1. Анализ спонтанных сообщений о НР, поступивших в отечественную базу данных, свидетельствует о том, что в 20,5% случаев имело место назначение потенциально опасных комбинаций ЛС. Из них НР, обусловленные взаимодействием ЛС, развились в 19,8% случаев или в 1,95% от общего числа проанализированных спонтанных сообщений.
2. Анализ и обработка спонтанных сообщений с помощью модифицированной Шкалы определения СД ПСС «НР-взаимодействие ЛС» позволяет повысить качество экспертной оценки спонтанных сообщений, что позволяет на основании полученных результатов разрабатывать и внедрять в практику меры, направленные на повышение эффективности и безопасности комбинированной фармакотерапии и снижение риска развития НР, развивающихся в результате взаимодействий ЛС.
3. Использование Шкалы определения СД ПСС «НР-взаимодействие ЛС» с целью определения степени достоверности взаимосвязи «НР-взаимодействие ЛС» можно считать целесообразным при анализе поступающих спонтанных сообщений о НР и проведении их экспертной оценки, так как эта шкала позволяет:
- получить более достоверные данные о взаимодействии препаратов и выявлять эти взаимодействия;
- использование шкалы способствует формированию современных и профессиональных навыков в экспертной оценке информации о НР, связанных с взаимодействием ЛС, которая требует высокого уровня квалификации специалиста, соответствующего современным требованиям;
- использование данной шкалы может быть полезным в подготовке доказательных публикаций о случаях лекарственных взаимодействий, приводящих к осложнениям, а так же при оценке уже опубликованных сообщений, особенно тех, которые не подвергались тщательной проверке.
4.Наибольшее количество лекарственных взаимодействий наблюдалось при применении НПВС, гематотропных препаратов, противомикробных ЛС.
5.Большинство НР, связанных с взаимодействием ЛС, являются серьезными и чаще случаются в лечебно-профилактических учреждениях или требуют госпитализации.
6.Учитывая низкий уровень распознавания лекарственных взаимодействий лечащими врачами, необходимо совершенствование системы подготовки и обучения медицинских кадров в области фармакотерапии, а так же предоставление специалистам здравоохранения информации о потенциально опасных лекарственных комбинациях и о повышенных рисках развития НР, связанных с взаимодействием ЛС.
