Введение. Туберкулез является одной из основных проблем общественного здравоохранения во многих странах. По данным Всемирной организации здравоохранения, ежегодно у более чем 9 миллионов человек по-прежнему развивается активный туберкулез, и почти 2 миллиона каждый год умирают от данной патологии [6]. Все большее значение приобретает устойчивость микобактерий туберкулеза к лекарственным препаратам, особенно множественная лекарственная устойчивость [5]. К тому же ни в одной стране мира нет достаточных средств для покрытия потребностей общественного здравоохранения. Ограниченные бюджетные ресурсы зачастую используются нерационально [3,4]. Наиболее уязвимым на сегодняшний день остается госпитальный сектор, так как лекарственное обеспечение стационарных больных напрямую зависит от объемов финансирования [2]. Это обуславливает необходимость постоянного мониторинга использования противотуберкулезных препаратов.
Цель исследования. Анализ частоты и структуры назначений противотуберкулезных препаратов (ПТП), а также замен и их причин.
Материалы и методы. Исследования проведены на базе Областного государственного бюджетного учреждения здравоохранения (ОГБУЗ) «Смоленский противотуберкулезный клинический диспансер» (ОГБУЗ СПКД). Была проанализирована выборка историй болезни (302 истории, выборка репрезентативна) за 2010-2012 г. Частота назначений (Чн) препарата в % рассчитывалась, как отношение числа назначений конкретного лекарственного препарата к общему числу назначений (количество проанализированных историй болезни). Частота замен (Чз) в % – как отношение числа замен препарата к общему числу его назначений.
Результаты исследования. Анализ историй болезни пациентов, проживающих на территории города Смоленска или направленных в ОГБУЗ СПКД на лечение районными тубдиспансерами или Центральными районными больницами, показал, что средний возраст больных туберкулезом составил 41,81 ± 11,04 лет. Из них мужчин – 71,8%, женщин – 28,2%.
В общем количестве случаев 97,4% пациентам был поставлен диагноз туберкулез органов дыхания, 2,6% – туберкулез почки и посттуберкулезный нефрит (1,4%), полиорганный туберкулез (0,3%), туберкулез позвоночника (0,6%), менингоэнцефалит туберкулезной этиологии (0,3%). В структуре клинических форм туберкулеза органов дыхания на протяжении всего периода изучения преобладал инфильтративный туберкулез легких (44,0%). Значительную группу составляли больные с диссеминированным туберкулезом легких (22,2%). Диагноз фиброзно-кавернозный туберкулез легких поставлен 17,2% поступивших на лечение в стационар, туберкулема легких – 6,6%, экссудативный плеврит туберкулезной этиологии – 3,3%, казеозная пневмония – 2,6%, цирротический туберкулез – 1,6%, очаговый туберкулез – 1,3%, милиарный туберкулез – 0,3%.
Наиболее часто пациентам назначались препараты основного ряда: изониазид и его гомологи (Чн=66%), рифампицин (65%), пиразинамид (58%), этамбутол (58%), стептомицин (39%). При этом следует отметить, что в 81,6% случаев – это пероральные лекарственные формы (ЛФ) (таблетки, капсулы). Для обеспечения контролируемой терапии при назначении рифампицина в 20,4% случаев и изониазида в 18,3% случаев в дополнение к пероральным применялись инъекционные формы. Назначение изониазида и рифампицина только в инъекционной форме отмечено в одной из историй болезни (0,03%). Новый противотуберкулезный препарат рифапекс присутствовал в структуре назначений 2% пациентов только в 2012 г. по результатам анализа выборки историй болезни.
Среди резервных препаратов наибольшее значение частоты назначения имели фторхинолоны (Чн=39%). Номенклатура прописанных пациентам препаратов данной группы включала офлоксацин (офлоксацин, офлокс), левофлоксацин (ремедиа, левотек, левофлоксацин), ломефлоксацин (ломефлоксацин, ломфлокс), спарфлоксацин, гатифлоксацин (зарквин, гатиспан), ципрофлоксацин. На втором месте по частоте назначений среди препаратов резервного ряда находился канамицин (Чн=23%). В схемах лечения больных туберкулезом с лекарственной устойчивостью успешно используется парааминосалициловая кислота (ПАСК) (Чн=19%) [1]. Капреомицин назначался в 10% случаев, протионамид и циклосерин в 8% и 7% случаев соответственно. Наименьшее значение частоты назначений соответствовало рифабутину (Чн=4%).
Среди комбинированных ПТП наибольшую частоту назначений имели протикомб (18%) и ломекомб (9%), что объясняется преобладанием данных препаратов в структуре закупок по сравнению с другими комбинированными препаратами: фтизоактив (Чн=1%), цикло плюс и изопаск (Чн=0,7%).
Зачастую в процессе лечения возникает необходимость замены или отмены препаратов ввиду лекарственной устойчивости (ЛУ), плохой переносимости, отсутствия препарата или других причин.
Изониазид был замен в 11% случаев его назначения. Большинство замен (10 из 19) было произведено на производные гидразида изоникотиновой кислоты – гомологи изониазида – фтивазид, феназид и комбинированный препарат изониазида с пиридоксина гидрохлоридом (фтизоактив). При этом на фтивазид изониазид был заменен ввиду плохой переносимости, в частности возникновения рвоты, судорог при применении препарата. Причины замен на феназид и фтизоактив установлены не были. После определения лекарственной устойчивости к изониазиду данный препарат заменялся другими препаратами первого ряда (пиразинамидом, этамбутолом) и резервными ПТП (ПАСК, циклосерином, протионамидом). Частота замен фтивазида составила 28%. При этом вместо данного препарата назначались только феназид и изониазид. Пиразинамид заменялся в 3% случаев его назначения. На препараты первого ряда (изониазид и этамбутол) замены осуществлялись в 3 случаях ввиду возникновения аллергической реакции (сыпь) и перевода курса терапии в другую фазу после операции. Замены этамбутола при изучении выборки историй болезни осуществлялись при назначении его 8% пациентов. Среди препаратов первого ряда вместо этамбутола в схему химиотерапии включался пиразинамид (из-за возникновения рвоты) или его комбинация с рифампицином (причина не установлена). В большинстве же случаев (7 из 9) этамбутол врачами заменялся на препараты резерва: преимущественно на протионамид (3% от общего количества назначений этамбутола) ввиду предположения о лекарственной устойчивости к данному препарату (отрицательной динамики заболевания по данным рентгенологического обследования), а также доказанной резистентности к препарату. Из ПТП резервного ряда вместо этамбутола назначались ПАСК, канамицин и циклосерин ввиду установления резистентности к препарату и перевода курса терапии в другую фазу после операции. Стрептомицин до полного курса получили 84% пациентов, которым он был назначен (Чз=15%). В 3 случаях стрептомицин был заменен на препараты первого ряда (пиразинамид и этамбутол) ввиду возникновения аллергической реакции (сыпь). Большая часть замен стрептомицина осуществлялась на канамицин или его комбинацию с протионамидом из-за нарушения обменных процессов в миокарде, отеков стоп, голеней, снижения аппетита и жидкого стула. Одному пациенту стрептомицин был заменен на капреомицин (причина не установлена). Стоит отметить, что после окончания курса химиотерапии стрептомицином 19% пациентов получали канамицин, 6% – этамбутол, 1% – офлоксацин. Большая часть замен рифампицина (Чз=9%) осуществлялась на препараты второго ряда (15 замен из 18). При этом 6 пациентов получали рифабутин вместо рифампицина ввиду возникновения болей в ногах, жалоб на плохой сон, слабости и головокружения при назначении последнего. Пяти пациентам рифампицин был заменен на ПАСК по причине установленной устойчивости к препарату и появления побочных эффектов (жидкого стула, болей в ногах, кистях рук, невозможности сосредоточить внимание, головокружение). Замены рифампицина на фторхинолоны (офлоксацин, ломефлоксацин) произведены 4 пациентам ввиду плохой переносимости, рвоты, аллергической реакции и перевода курса химиотерапии в другую фазу после операции. Стоит отметить, что замены осуществлялись и по лекарственным формам рифампицина: капсулы на инъекционную форму ввиду возникновения рвоты и поноса а, наоборот, из-за отсутствия в стационаре парентеральной формы. Наиболее длительный по действию среди рифампицинов – рифапекс был заменен на рифампицин при лечении одного из них (Чз=14%). Необходимо отметить, что применение рифапекса наиболее оправдано в условиях амбулаторного лечения для повышения комплаентности к терапии.
Таким образом, причины замен препаратов основного ряда установлены в 61,8% случаев. Для большинства пациентов поводом послужили возникшие побочные эффекты, плохая переносимость препарата (44,7% числа установленных причин замен препаратов основного ряда), ввиду установленной лекарственной устойчивости препараты заменялись в 34,2% случаев, предполагаемой лекарственной устойчивости (отрицательная динамика или отсутствие положительной динамики заболевания) в 10,5%, отсутствия препарата или перевода курса химиотерапии в другую фазу – 5,3% (рис. 1).

Рис. 1. Причины замен противотуберкулезных препаратов основного ряда.
Наибольшее значение частоты замен среди препаратов резервного ряда характерно также для фтохнолонов (Чз =22%). Большая доля замен препаратов данной группы осуществлялась ввиду их отсутствия в стационаре (в 76% случаев замен). При этом в основном осуществлялись замены одного фторхинолона на другой, имеющийся в наличии в данный момент. Полный курс протионамидом получили 87% пациентов, которым данный препарат был назначен (Чз=13%). На этамбутол протионамид был заменен ввиду установленной лекарственной устойчивости, на циклосерин – по причине появления тошноты и жидкого стула. Капреомицин в процессе терапии заменялся в большинстве случаев на препараты основного ряда – этамбутол и фтивазид. Среди препаратов резервного ряда замена осуществлялась на циклосерин (Чз=10%). После получения полного курса капреомицина 6% пациентов продолжали лечение пасконатом и этамбутолом. Циклосерин был заменен на пиразинамид и капреомицин ввиду появления аллергической реакции (кожного зуда) (Чз=9%). Замена рифабутина производилась только у одного пациента по результатам изучения выборки историй болезни на рифампицин по причине возникновения жидкого стула. Канамицин в процессе лечения был заменен на другие препараты резервного ряда – амикацин, капреомицин (ввиду отсутствия канамицина) и циклосерин (появление звона в ушах) у 4% пациентов. После окончания курса лечения канамицином 3 пациента продолжали лечение капреомицином, его комбинацией с циклосерином и рифампицином. Препараты ПАСК в процессе лечения заменялись дважды: на циклосерин и таблетированной формы на пасконат – раствор для инъекций, для контролируемости лечения (Чз=3%).
Таким образом, причины замен препаратов резервного ряда установлены в 74,4% случаев. Из них большая часть связана с отсутствием препарата в стационаре (62,5%), побочные эффекты явились причиной замен в 28,1% случаев, предполагаемая лекарственная устойчивость – 6,3%, установленная лекарственная устойчивость – 3,1% (рис. 2).
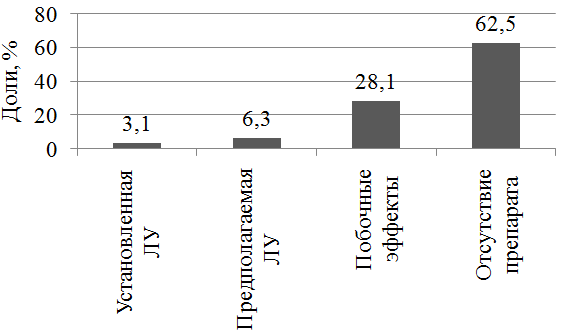
Рис. 2. Причины замен противотуберкулезных препаратов резервного ряда.
Комбинированные ПТП в большинстве случаев заменялись на сочетание отдельных препаратов основного и резервного ряда. Только ломекомб в 8 случаев из 15 был заменен на протиокомб и в 1 – на фтизоактив с другими ПТП (Кз=56%). Частота замен препарата изопаск составила 50%, протиокомб – 35%. Причинами совершенных замен послужили: установленная лекарственная устойчивость к компонентам препарата (18,8%), побочные эффекты: токсико-аллергическое состояние при приеме препарата, слабость, головокружение, плохая переносимость, тошнота, рвота, жидкий стул, аллергия (62,5%), отсутствие препарата (12,5%), отсутствие положительной динамики заболевания от назначенной терапии (6,3%).
Выводы. Результаты проведенного частотного анализа позволили определить широту применения противотуберкулезных препаратов в стационаре и выявить наиболее часто и редко использующиеся. Установлено, что высокое значение частоты назначений характерно для наиболее эффективных препаратов первого ряда изониазида и его гомологов и рифампицина, среди ПТП резервного ряда – фторхинолонов, канамицина и ПАСК. По частоте совершенных замен среди препаратов первого ряда на первом месте также изониазид и его гомологи, далее стрептомицин и рифампицин, резервного ряда – фторхинолоны, протионамид и капреомицин. Наиболее частыми причинами замен препаратов основного ряда явились побочные эффекты и установленная лекарственная устойчивость к препарату, резервного ряда – отсутствие препарата и возникновение побочных эффектов. Значительная доля замен препаратов резерва, связанная с отсутствием препаратов обусловлена тем, что стоимость ряда препаратов данной группы в десятки раз превышает стоимость препаратов основного ряда. Это не позволяет лечебным учреждениям закупить их в должном количестве, соответственно пройти полный курс данными препаратами получают возможность не все пациенты. Полученные результаты могут быть использованы для расчета потребности в противотуберкулезных препаратах и затрат на лечение в фармакоэкономическом анализе.
